Clear Sky Science · pt
Atividades sinérgicas antipersister, inibidoras de efluxo e antibiofilme de pós-bióticos derivados de Lactobacillus vaginal contra UPEC: rumo a uma nova terapia para ITUs
Por que infecções urinárias persistentes importam
As infecções do trato urinário (ITUs) estão entre as infecções bacterianas mais comuns, especialmente em mulheres, e muitas pessoas as experimentam repetidamente apesar do uso de antibióticos. Este estudo explora uma nova abordagem que poupa antibióticos para enfrentar essas infecções recorrentes e difíceis: aproveitar bactérias vaginais benéficas e seus subprodutos químicos para impedir que E. coli problemáticas se estabeleçam, se ocultem e retornem.
Os sobreviventes ocultos por trás das infecções repetidas
Antibióticos padrão podem eliminar a maior parte das bactérias, mas uma pequena subpopulação conhecida como “células persister” sobrevive entrando em um estado dormente de baixa atividade. Esses dormintes não são geneticamente resistentes, mas toleram doses muito altas de antibióticos e podem despertar mais tarde, impulsionando ITUs crônicas e recorrentes. Os pesquisadores trabalharam com uma cepa comum causadora de ITU, E. coli UTI89, e mostraram que antibióticos potentes como colistina e meropenem facilmente desencadeiam essas células persister. Em testes de laboratório que imitam a urina, pequenas frações de E. coli sobreviveram à exposição extrema a antibióticos, confirmando como persisters surgem com facilidade e por que os regimes padrão frequentemente não proporcionam alívio duradouro.
Transformando bactérias vaginais amigas em tratamento
Uma vagina saudável é normalmente dominada por espécies de Lactobacillus, que ajudam a manter micróbios nocivos sob controle. Em vez de usar bactérias vivas “probióticas”, este estudo focou no sobrenadante livre de células — essencialmente o coquetel de moléculas que elas secretam, chamado pós-bióticos. A partir de cepas de Lactobacillus vaginal isoladas de mulheres saudáveis, a equipe separou e analisou esses compostos secretados. Dois metabólitos-chave, anidrido itacônico e (−)-terpinen-4-ol, destacaram-se por sua capacidade de atuar em conjunto e reduzir drasticamente o número de células persister de E. coli quando combinados com antibióticos. Um terceiro composto, triptamida, previamente demonstrado capaz de desagregar a matriz viscosa de biofilme que as bactérias constroem para proteção, foi adicionado para reforçar a ação antibiofilme.
Como a nova mistura enfraquece bactérias difíceis de matar
Os cientistas descobriram que essas moléculas derivadas de Lactobacillus atacam os persisters de E. coli em vários pontos ao mesmo tempo. Primeiro, elas aumentam a produção de espécies reativas de oxigênio — formas de oxigênio quimicamente reativas que danificam componentes bacterianos — tornando os antibióticos muito mais letais para células dormentes. Quando antioxidantes foram adicionados, esse efeito bactericida diminuiu, ressaltando o papel do estresse oxidativo. Segundo, os compostos tornam a membrana externa bacteriana mais “permeável”, conforme demonstrado por corantes fluorescentes que entram nas células mais facilmente após o tratamento. Terceiro, inibem as “bombas de efluxo” celulares, minúscimas máquinas de exportação que normalmente expulsam antibióticos para fora da célula. Com as bombas bloqueadas, mais medicamento permanece dentro das bactérias e menos persisters sobrevivem. Juntas, essas mudanças reduziram biofilmes pré-formados de E. coli em até dez ordens de magnitude em testes de laboratório, sem prejudicar células imunológicas de mamíferos nas doses testadas.
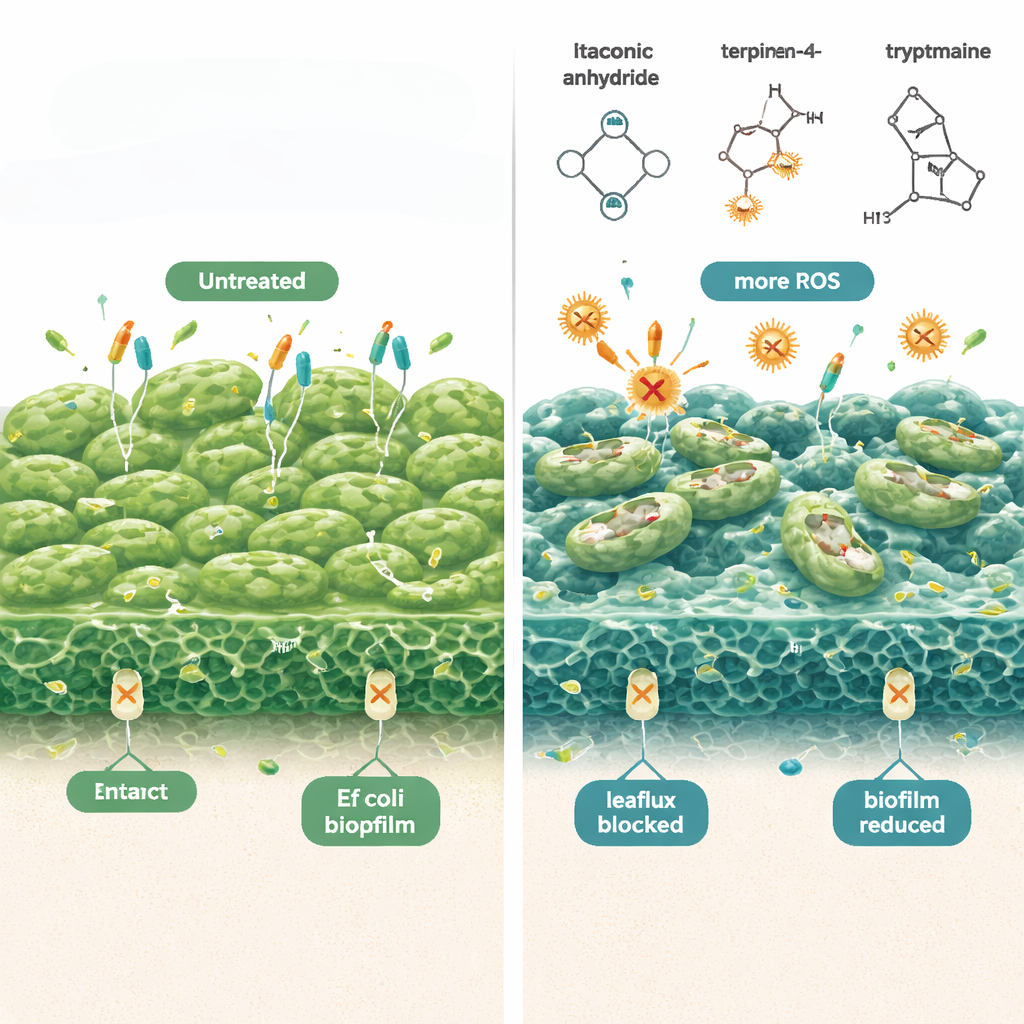
Do banco de laboratório para um enxágue vaginal prático
Para transformar essas descobertas em algo utilizável no dia a dia, a equipe projetou um enxágue vaginal personalizado usando uma base em gel termossensível chamada poloxamer 407. À temperatura ambiente ele se comporta como um fluido para aplicação fácil, e depois engrossa suavemente à temperatura corporal para melhorar o contato com as paredes vaginais. O gel carrega uma combinação definida e segura de anidrido itacônico, (−)-terpinen-4-ol e triptamida. Em placas de laboratório, essa formulação funcionou em uma faixa de pH semelhante às condições vaginais, suprimindo fortemente a formação de biofilmes de E. coli e reduzindo o número de bactérias viáveis em cerca de nove ordens de magnitude. Permaneceu estável e biologicamente ativa por pelo menos três meses em armazenamento refrigerado e também mostrou ação ampla contra outras bactérias problemáticas como Klebsiella, MRSA e Pseudomonas.
Testando segurança e proteção em camundongos
Em seguida, os pesquisadores avaliaram o enxágue em um modelo murino de infecção vaginal por E. coli. Camundongos foram inoculados com E. coli marcadas com GFP (fluorescentes) e então tratados com o enxágue de metabólitos personalizado, um enxágue probiótico contendo Lactobacillus vivo, um enxágue vaginal comercial ou uma base placebo. Os animais que receberam o enxágue de metabólitos personalizado mostraram inflamação vaginal marcadamente menor, mantiveram o peso corporal e apresentaram contagens bacterianas drasticamente menores no fluxo vaginal em comparação com os outros grupos. Mais impressionante, os camundongos tratados não tinham E. coli detectável na urina, bexiga, rins ou tecido vaginal e mantiveram função renal normal, indicando que a formulação não apenas reduziu a infecção local, mas também preveniu a disseminação para o trato urinário superior.
O que isso pode significar para pessoas com ITUs recorrentes
O estudo conclui que um enxágue vaginal construído a partir de metabólitos precisos produzidos por espécies de Lactobacillus naturalmente protetoras pode enfraquecer E. coli causadoras de ITU de várias maneiras: reduzindo populações persister, interrompendo biofilmes e tornando antibióticos padrão mais eficazes. Como a abordagem se baseia em moléculas não vivas em vez de bactérias vivas ou cursos longos de drogas sistêmicas, pode ser mais segura, mais estável e mais fácil de regulamentar. Embora sejam necessários ensaios em humanos, esse enxágue à base de metabólitos aponta para um futuro em que ITUs recorrentes sejam prevenidas não apenas por antibióticos mais fortes, mas por reforçar de forma inteligente as defesas microbianas naturais do corpo na origem.
Citação: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Palavras-chave: infecção do trato urinário, microbioma vaginal, pós-bióticos de Lactobacillus, tolerância a antibióticos, biofilmes bacterianos