Clear Sky Science · pt
Redesenho racional de DNAzima G-quádruplex de alta atividade por meio do emolduramento e das alças de nucleobases
Pequenas máquinas de DNA com grande potencial
Imagine substituir enzimas proteicas frágeis por filamentos minúsculos de DNA que resistem ao calor, a produtos químicos e ao manuseio brusco, mas que ainda realizam química útil. Este estudo explora exatamente essa ideia. Os pesquisadores ajustam estruturas especiais de DNA para que se comportem como enzimas em miniatura, capazes de usar peróxido de hidrogênio para gerar um sinal forte. Essas “máquinas” de DNA mais resistentes e rápidas podem tornar futuros testes médicos, sensores ambientais e diagnósticos portáteis mais baratos, mais confiáveis e mais fáceis de usar fora do laboratório.
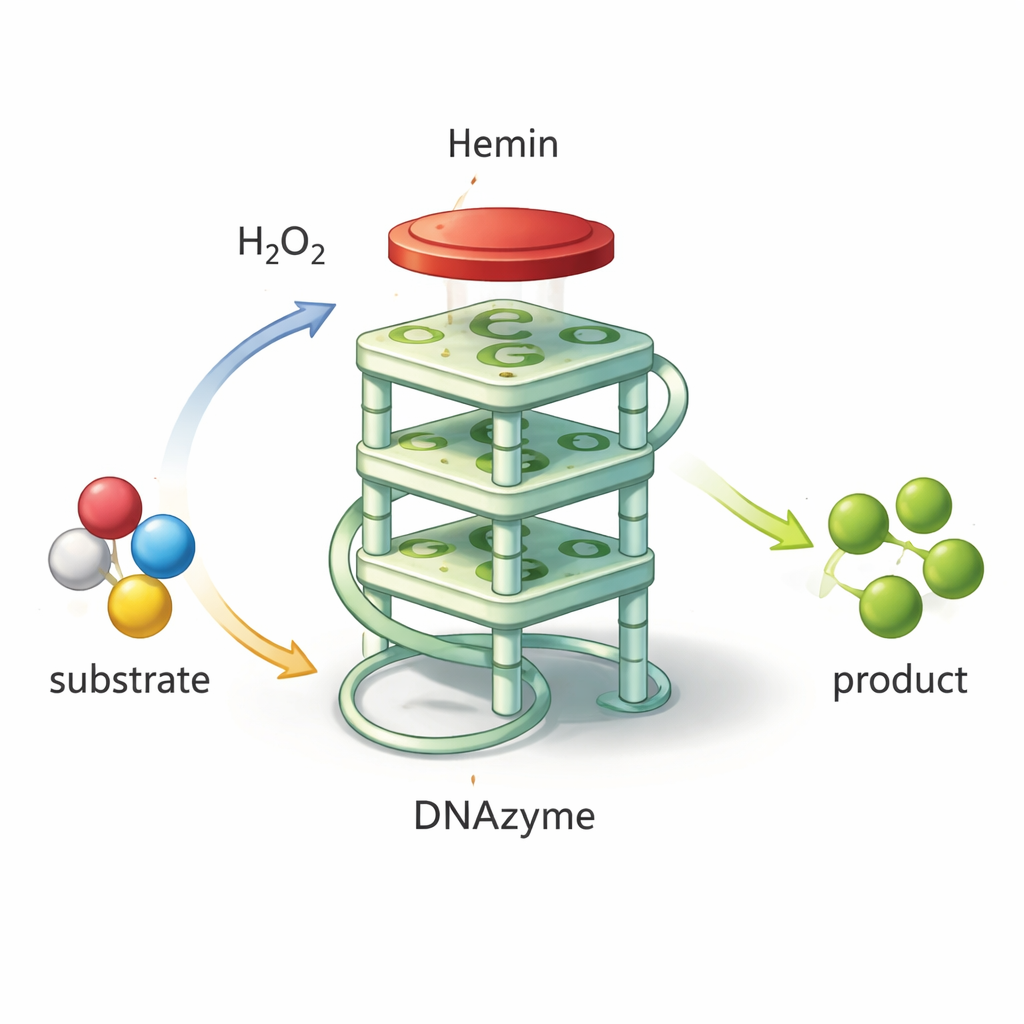
Transformando DNA em uma pequena ferramenta química
Nem todo DNA é apenas um transportador passivo de informação genética. Certas sequências curtas podem se dobrar em formas incomuns que capturam moléculas específicas ou até aceleram reações químicas. Uma dessas formas é o G‑quádruplex, em que DNA rico em guanina se dobra em uma pilha compacta de quatro camadas. Quando uma pequena molécula contendo ferro chamada hemina se posiciona sobre essa pilha, o par atua como uma “DNAzima”: um catalisador à base de DNA que imita enzimas peroxidases naturais. Ele pode usar peróxido de hidrogênio para oxidar um composto que forma cor, produzindo um forte sinal esverdeado fácil de medir. Como essas DNAzimas são baratas de produzir, altamente estáveis e fáceis de redesenhar, elas são blocos promissores para biossensores que detectam patógenos, toxinas ou marcadores de doenças.
Por que as enzimas de DNA atuais precisam de aperfeiçoamento
Apesar de seu potencial, a maioria das DNAzimas ainda é mais lenta e menos eficiente que enzimas proteicas encontradas na natureza. Biossensores existentes frequentemente precisam amplificar o alvo com técnicas como PCR ou adicionar produtos químicos auxiliares, o que aumenta custo e complexidade. Tentativas anteriores de melhorar DNAzimas incluíram ligar duas unidades de DNA, prender hemina de forma permanente ou cercar o sítio reativo com grupos químicos extras. Esses artifícios às vezes ajudam, mas também podem introduzir volume que atrapalha ou exigir química elaborada. Uma questão em aberto tem sido como mudanças simples nas bases de DNA próximas — especialmente aquelas que não rompem a forma central do G‑quádruplex — poderiam ajustar a atividade de maneira previsível e “projetável”.
Redesenhando uma DNAzima de alto desempenho
A equipe concentrou-se em uma DNAzima particularmente ativa conhecida como B730, que já está entre os melhores catalisadores G‑quádruplex não modificados. Eles alteraram sistematicamente o DNA logo fora de seu núcleo, adicionando ou reposicionando bases comuns como adenina, timina e citosina nas regiões de alça e cauda. Uma versão redesenhada, chamada B730‑1.2, combinou adeninas adicionadas nas alças com um par curto timina–citosina em uma das extremidades da cadeia. Em condições moderadas de peróxido de hidrogênio, essa variante triplicou a velocidade inicial da reação e aumentou em cerca de quatro vezes a quantidade total de produto colorido em comparação com a B730 original. Também superou claramente duas outras DNAzimas bem conhecidas, AS1411 e CatG4, quando testadas lado a lado.
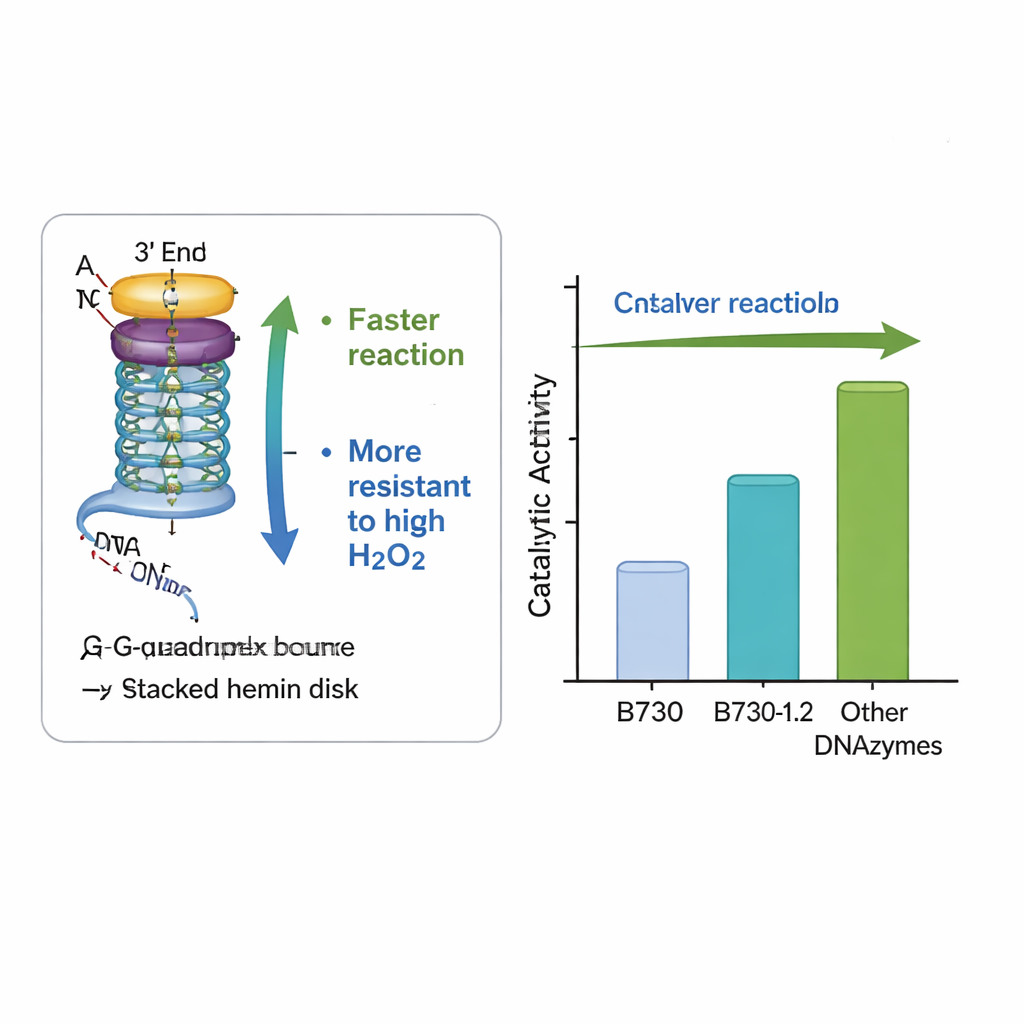
Projetada para resistir a condições severas
Um obstáculo prático importante tanto para peroxidases naturais quanto artificiais é que níveis elevados de peróxido de hidrogênio, o próprio ingrediente que impulsiona a reação, podem destruir a enzima e encerrar o processo. A DNAzima redesenhada B730‑1.2 mostrou notável resiliência: manteve e até aumentou sua atividade em níveis de peróxido que normalmente inativam sistemas semelhantes. Medições de absorção de luz confirmaram que o DNA modificado ajudou a formar o intermediário reativo chave — o chamado Composto I — mais rapidamente, sem perturbar a forma geral do G‑quádruplex. Em outras palavras, mudanças sutis nas bases circundantes criaram um ambiente local mais favorável para a química, acelerando as etapas úteis enquanto ajudavam a proteger o centro catalítico da autodestruição.
O que isso significa para sensores futuros
Para um não especialista, a mensagem é direta: ao ajustar cuidadosamente apenas algumas “letras” de cada lado de uma DNAzima já eficiente, os autores produziram uma versão que funciona mais rápido e continua operando em condições mais severas. A estratégia deles de modificar bases flanqueantes e de alça oferece uma receita simples e de baixo custo para construir catalisadores à base de DNA mais potentes sem recorrer a modificações químicas complexas. DNAzimas robustas e eficientes assim podem ficar no coração de tiras de teste e dispositivos portáteis de próxima geração que rapidamente transformam sinais biológicos invisíveis — como vestígios de vírus ou poluentes — em mudanças de cor fáceis de ler.
Citação: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Palavras-chave: DNAzima G-quádruplex, mimético de peroxidase, biossensoriamento, engenharia de aptâmeros, catalise do peróxido de hidrogênio