Clear Sky Science · pt
Investigação de líquidos iônicos à base de Acoramidis como potenciais estabilizadores da transtirretina usando cálculos DFT, docking molecular e estudos ADMET
Por que é tão difícil desenvolver um comprimido para uma doença cardíaca rara
A amiloidose por transtirretina (ATTR) é uma doença grave em que uma proteína sanguínea se acumula no coração e nos nervos, danificando-os lentamente. Um novo medicamento, o Acoramidis, pode ajudar a interromper esse acúmulo, mas há um problema prático: o fármaco tem baixa solubilidade em água, o que dificulta sua absorção pelo organismo quando administrado como comprimido. Este estudo explora uma abordagem inteligente para redesenhar o Acoramidis em novas formas semelhantes a sais, chamadas líquidos iônicos, que poderiam tornar o medicamento mais fácil de administrar e mais eficaz.
Transformando um fármaco promissor em uma forma ingerível
Para que um comprimido funcione, ele precisa primeiro se dissolver nos fluidos aquosos do estômago e dos intestinos e, em seguida, atravessar a parede intestinal até a corrente sanguínea. O Acoramidis é eficaz em estabilizar a proteína transtirretina (TTR), o que ajuda a prevenir agregados proteicos nocivos associados à ATTR, mas possui baixa solubilidade e fraca biodisponibilidade oral. Os pesquisadores buscaram enfrentar esse desafio combinando quimicamente o Acoramidis com diferentes moléculas parceiras carregadas, criando três novas versões em forma de líquido iônico (IL1, IL2 e IL3). Essas versões foram projetadas para se comportar mais como sais fluidos do que como cristais rígidos, potencialmente melhorando a solubilidade e a distribuição do fármaco no organismo. 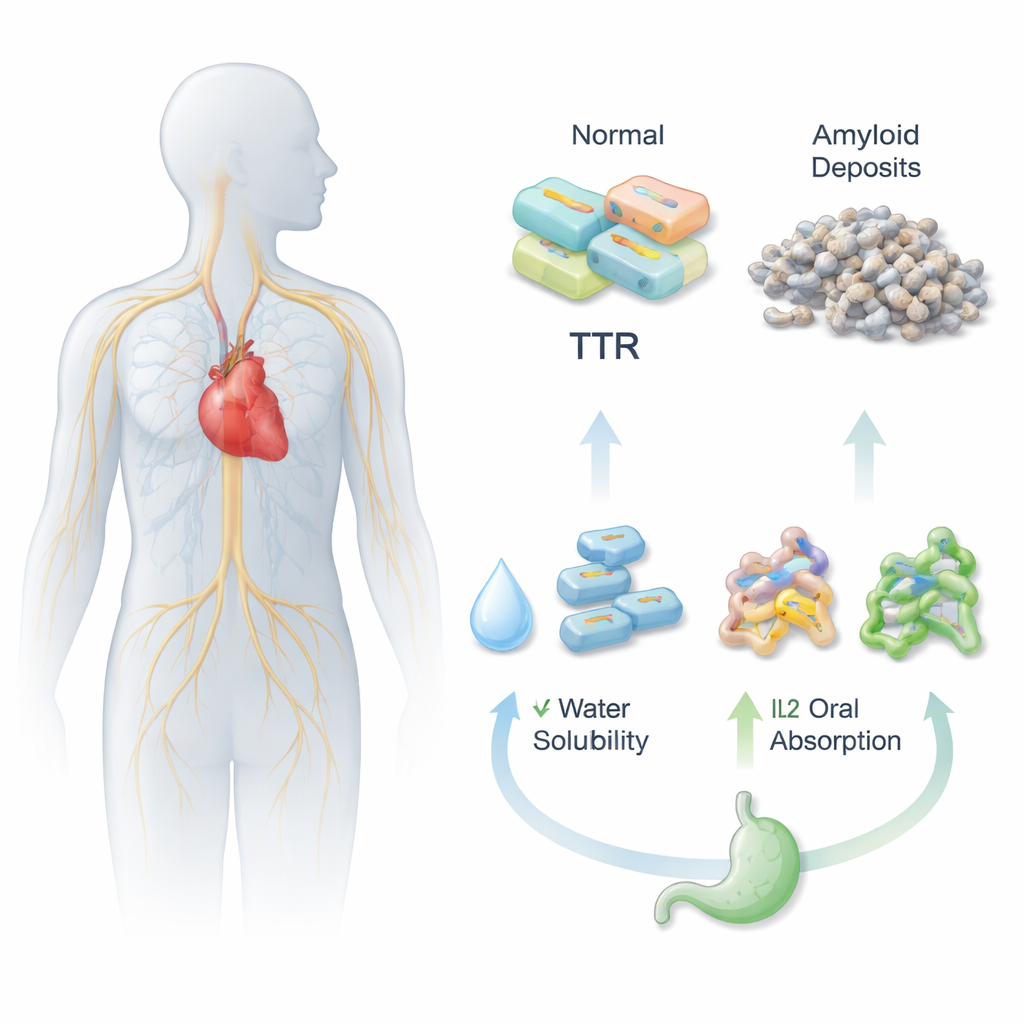
Investigando as novas moléculas no computador
Em vez de ir diretamente a testes em animais ou humanos, a equipe utilizou métodos computacionais avançados para prever como essas novas formas se comportariam. Cálculos de química quântica estimaram quão polares são as moléculas — um indicador chave da solubilidade em água — e quão facilmente seus elétrons se deslocam, o que se relaciona com possíveis interações com proteínas. O IL1 destacou-se por ter o maior momento dipolar e a maior responsividade eletrônica, indicando que deve dissolver-se melhor em água e formar contatos mais fortes e flexíveis com seus alvos. Os cálculos energéticos também sugeriram que o IL1 é mais estável termicamente do que o fármaco original e as outras duas formas iônicas, o que significa que tende a se decompor menos antes de atingir seu destino.
Quão firmemente o fármaco consegue se ligar ao seu alvo
Em seguida, os pesquisadores utilizaram docking molecular, um teste virtual de “chave-fechadura”, para ver quão bem o Acoramidis e suas três formas iônicas se encaixam no canal de ligação da proteína TTR. Todos os quatro compostos se acoplaram na região correta da TTR, mas o IL1 formou a ligação mais firme, com a energia de ligação mais favorável e vários contatos estabilizantes — particularmente ligações de hidrogênio — com aminoácidos-chave da proteína. Essa ligação mais forte sugere que o IL1 pode ser ainda melhor que o fármaco original em manter a TTR em sua estrutura segura de quatro subunidades, ajudando a prevenir a decomposição e o desdobramento que levam aos depósitos amiloides.
O corpo vai absorver e eliminar essas novas formas?
Por fim, a equipe usou ferramentas farmacológicas online para investigar como o organismo poderia processar esses compostos — quão bem eles se dissolvem, atravessam a parede intestinal, circulam no sangue e são eventualmente eliminados. As três formas iônicas foram previstas como mais solúveis em água do que o Acoramidis, com o IL3 exibindo a maior solubilidade bruta. Medidas de permeabilidade intestinal e absorção oral geral melhoraram para os três líquidos iônicos, com IL1 e IL2 oferecendo o melhor equilíbrio entre penetração intestinal e biodisponibilidade prevista. A ligação a proteínas no sangue, as taxas de depuração e as meias-vidas também se alteraram de formas que sugerem que as formas em líquido iônico poderiam proporcionar exposição mais estável após administração oral, com o IL1 novamente mostrando um perfil particularmente favorável. 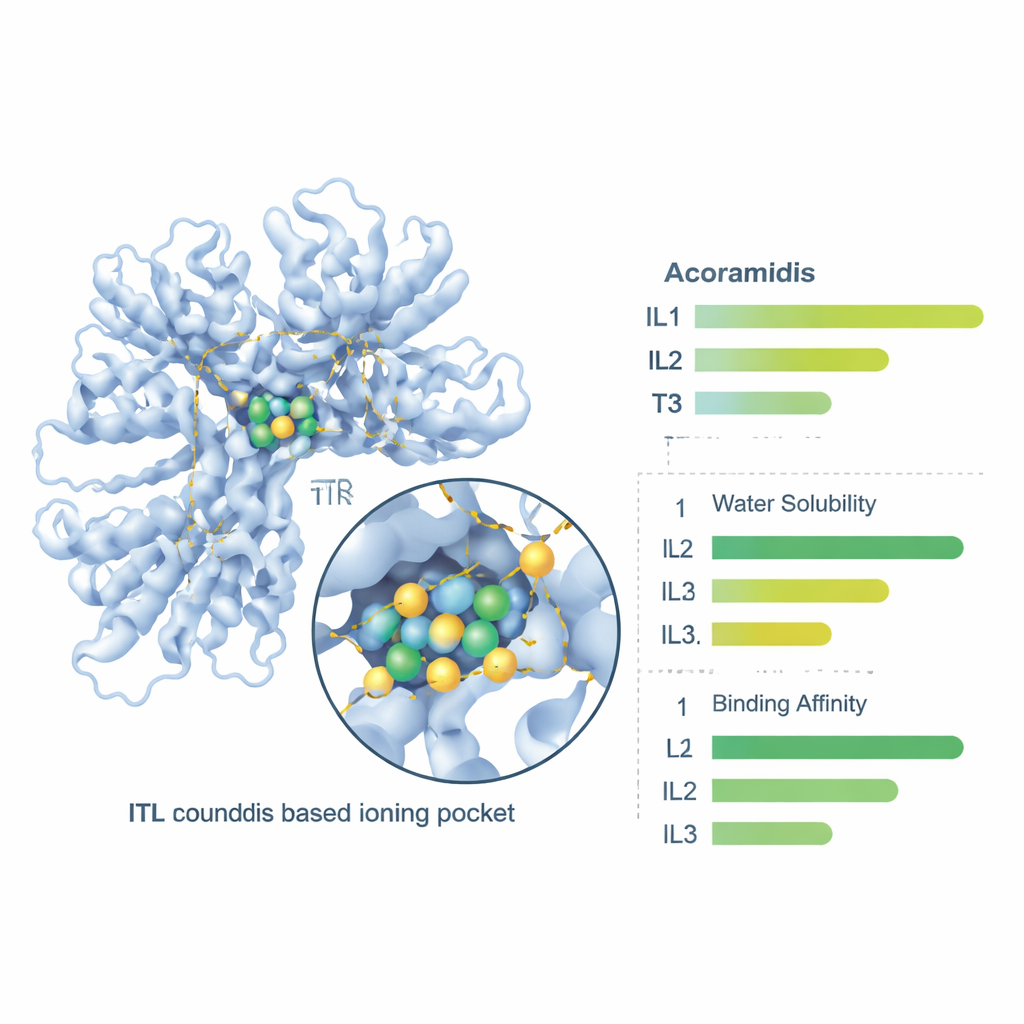
O que isso pode significar para tratamentos futuros da ATTR
Para um público não especializado, a principal mensagem é que o Acoramidis já parece promissor para tratar uma doença rara, porém séria, do coração e dos nervos, mas sua baixa solubilidade limita sua eficácia por via oral. Ao transformar o Acoramidis em líquidos iônicos projetados, este estudo demonstra — inteiramente por meio de testes computacionais — que pode ser possível criar versões que se dissolvem melhor, se ligam mais fortemente ao alvo proteico e são absorvidas de forma mais eficiente. Entre os três candidatos, o IL1 parece oferecer o melhor equilíbrio entre estabilidade, força de ligação, solubilidade e absorção oral prevista, tornando-o um forte candidato para desenvolvimento laboratorial e clínico futuro, com o objetivo de fornecer tratamentos mais eficazes e fáceis de administrar para a ATTR.
Citação: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Palavras-chave: amiloidose por transtirretina, Acoramidis, líquidos iônicos, desdobramento proteico, administração oral de fármacos