Clear Sky Science · pt
Projeto in silico de uma vacina multiepítopo direcionada a DENV-1 e DENV-3
Por que vacinas contra dengue ainda importam
A febre da dengue deixou de ser uma doença tropical rara; hoje ameaça bilhões de pessoas em mais de 100 países e frequentemente sobrecarrega hospitais em partes da Ásia, da América Latina e além. Mesmo com duas vacinas licenciadas no mercado, a proteção é desigual, especialmente em pessoas que nunca tiveram dengue antes e em regiões onde vários sorotipos virais circulam simultaneamente. Este estudo faz uma pergunta atual: o desenho assistido por computador pode nos ajudar a construir uma vacina mais segura e precisa, voltada especificamente para coinfecções perigosas por dois sorotipos de dengue que frequentemente aparecem juntos?
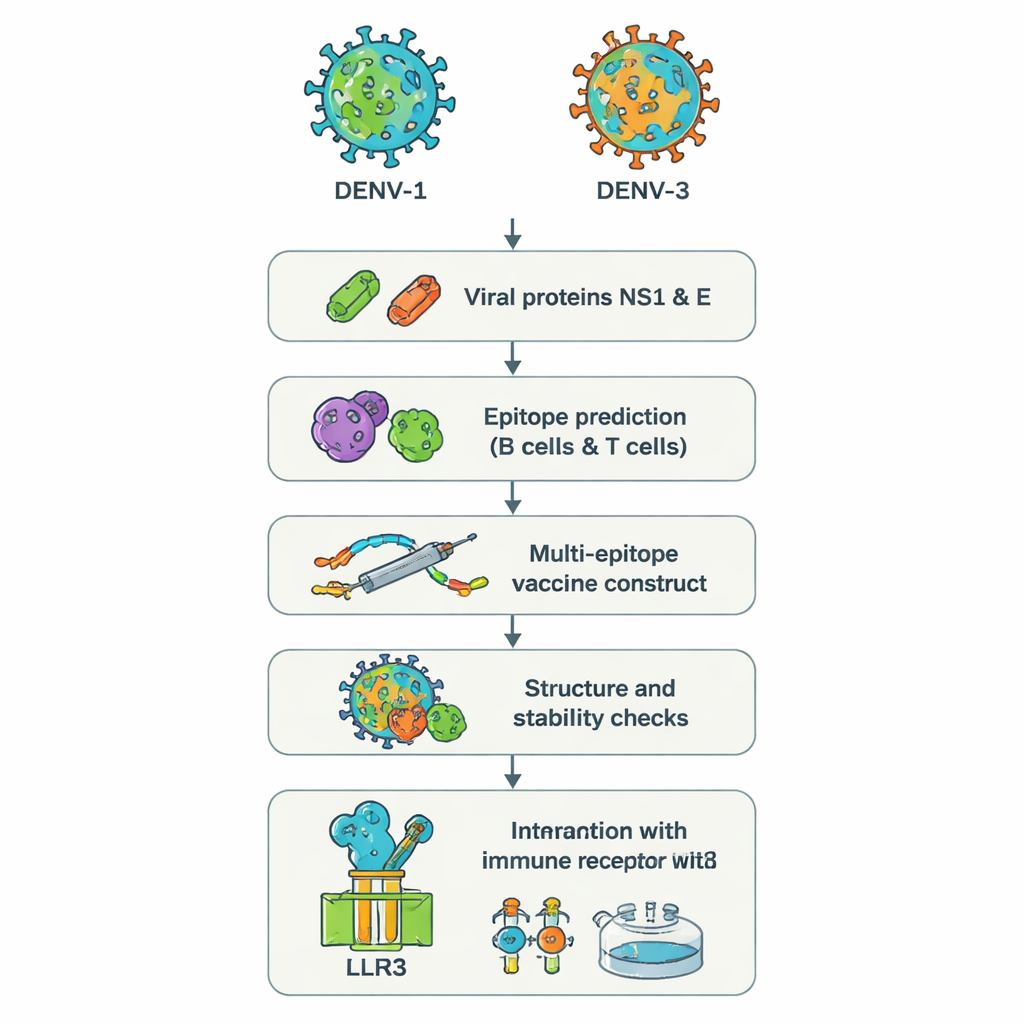
Dois sorotipos sorrateiros e por que eles são um problema
O vírus da dengue ocorre em quatro versões, chamadas sorotipos DENV‑1 a DENV‑4. A infecção por qualquer um pode causar febre alta, dor intensa e, em alguns casos, hemorragia ou choque potencialmente fatais. Preocupa o fato de que adoecer uma segunda vez com um sorotipo diferente às vezes pode agravar a doença em vez de protegê-la, porque anticorpos pré-existentes podem facilitar a entrada do novo vírus nas células, um processo chamado aprimoramento dependente de anticorpo. Em surtos recentes, médicos relataram pacientes infectados simultaneamente por DENV‑1 e DENV‑3, uma combinação associada a doença mais grave e a resultados laboratoriais confusos. As vacinas atuais não protegem de forma confiável todas as faixas etárias e todos os sorotipos, especialmente em pessoas sem exposição prévia, deixando uma lacuna perigosa nas defesas.
Projetando uma vacina desde a molécula
Em vez de cultivar vírus inteiros em laboratório, os pesquisadores usaram uma abordagem às vezes chamada de “vacinologia reversa”. Eles partiram das sequências genéticas de duas proteínas da dengue, NS1 e E, de DENV‑1 e DENV‑3. Essas proteínas são fundamentais para a forma como o vírus invade células e como o sistema imune o reconhece. Ferramentas poderosas baseadas na web escanearam as sequências proteicas para localizar pequenos trechos — epítopos — que têm maior probabilidade de ser reconhecidos por células B humanas (que produzem anticorpos) e células T (que matam células infectadas e coordenam respostas). De centenas de candidatos, a equipe selecionou um conjunto reduzido previsto como altamente visível ao sistema imune, compartilhado entre os dois sorotipos e capaz de desencadear sinais antivirais úteis, como interferon-gama.
Construindo uma única molécula vacinal de múltiplas finalidades
Os epítopos escolhidos foram então costurados digitalmente em uma única proteína artificial longa, uma vacina “multiepítopo”. Pequenos conetores de aminoácidos atuam como espaçadores flexíveis para que cada epítopo mantenha sua conformação e permaneça acessível às células imunes. Um trecho extra, baseado em um peptídeo antimicrobiano humano natural chamado beta-defensina, foi adicionado como adjuvante para potencializar a resposta geral. A análise computacional previu que o constructo final, contendo 575 aminoácidos, seria estável, hidrofílico (e portanto mais fácil de dissolver) e pouco provável de agir como alergeno. Ferramentas adicionais de predição estrutural geraram um modelo tridimensional e verificaram que a maioria dos blocos construtores ocupava posições realistas, semelhantes às observadas em estruturas proteicas conhecidas.
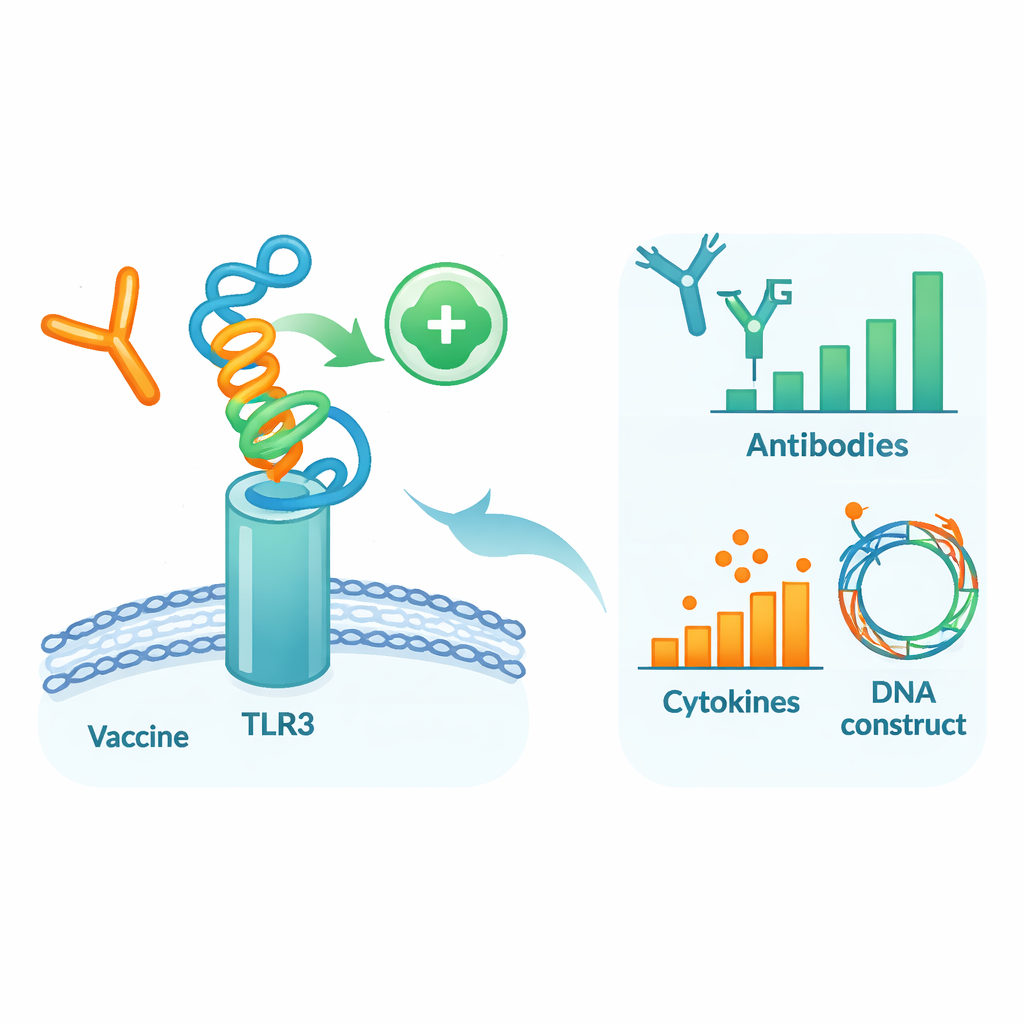
Testando o candidato dentro de um corpo virtual
Para ver como essa proteína projetada poderia se comportar em um ambiente semelhante ao humano, os autores executaram uma série de simulações computacionais detalhadas. Primeiro, eles acoplaram o modelo vacinal ao TLR3, uma proteína sensor em células imunes que detecta material viral e ajuda a disparar defesas iniciais. Simulações de dinâmica molecular — filmes virtuais de átomos em movimento — sugeriram que a vacina e o TLR3 formam um complexo estável, suportado por energias de ligação favoráveis e numerosas ligações de hidrogênio. Análises adicionais de movimento e energia apontaram regiões específicas de ambas as moléculas que atuam como “pontos quentes” de contato. Em seguida, um simulador do sistema imune foi usado para imitar três doses da vacina ao longo de vários meses. O sistema imune virtual produziu fortes ondas de anticorpos IgG protetores, memória duradoura de células B e T e moléculas sinalizadoras consistentes com uma resposta antiviral robusta.
Do modelo computacional a um plano pronto para laboratório
Finalmente, os pesquisadores adaptaram o código genético da vacina para produção eficiente em microrganismos de uso comum em laboratório e inseriram com sucesso essa sequência de DNA otimizada em um plasmídeo de expressão padrão, pronto para testes experimentais futuros. Em termos simples, o trabalho entrega um projeto detalhado para uma nova vacina contra dengue que mira pedaços cuidadosamente escolhidos de DENV‑1 e DENV‑3, é prevista como estável e segura, e deve envolver fortemente ambos os ramos do sistema imune. Embora esses resultados sejam puramente computacionais e precisem ser confirmados em células, animais e, eventualmente, em pessoas, eles mostram como a bioinformática moderna pode gerar rapidamente candidatos vacinais sob medida para problemas complexos como a coinfecção por dengue.
Citação: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Palavras-chave: vacina contra dengue, multi-epítopo, DENV-1, DENV-3, imunoinformática