Clear Sky Science · pt
Análise integrativa de proteômica e metabolômica revela distúrbio no metabolismo de aminoácidos em células de leucemia mieloide aguda resistentes à adriamicina
Por que alguns medicamentos contra leucemia deixam de funcionar
A quimioterapia transformou o tratamento da leucemia mieloide aguda (LMA), um câncer sanguíneo de crescimento rápido. Ainda assim, muitos pacientes veem a doença reaparecer porque as células cancerígenas aprendem a sobreviver aos próprios medicamentos destinados a matá‑las. Este estudo parte de uma pergunta simples, porém crucial: o que muda dentro das células leucêmicas quando elas se tornam resistentes à adriamicina, um dos fármacos padrão da quimioterapia, e essas mudanças poderiam indicar novas formas de restaurar a eficácia do medicamento?
Espiando dentro das células leucêmicas
Para investigar isso, os pesquisadores compararam uma linhagem humana comum de LMA, chamada HL60, com uma linhagem irmã que foi tornada resistente à adriamicina (HL60/R). Em vez de examinar um único gene ou proteína por vez, eles usaram duas abordagens amplas e complementares. A proteômica mediu milhares de proteínas diferentes — as moléculas executoras que realizam a maior parte das tarefas na célula. A metabolômica mediu centenas de pequenas moléculas que compõem o metabolismo celular, incluindo lipídios, açúcares e aminoácidos. Ao combinar essas camadas “ômicas”, a equipe construiu um panorama detalhado de como as células resistentes diferem de suas congêneres ainda sensíveis.
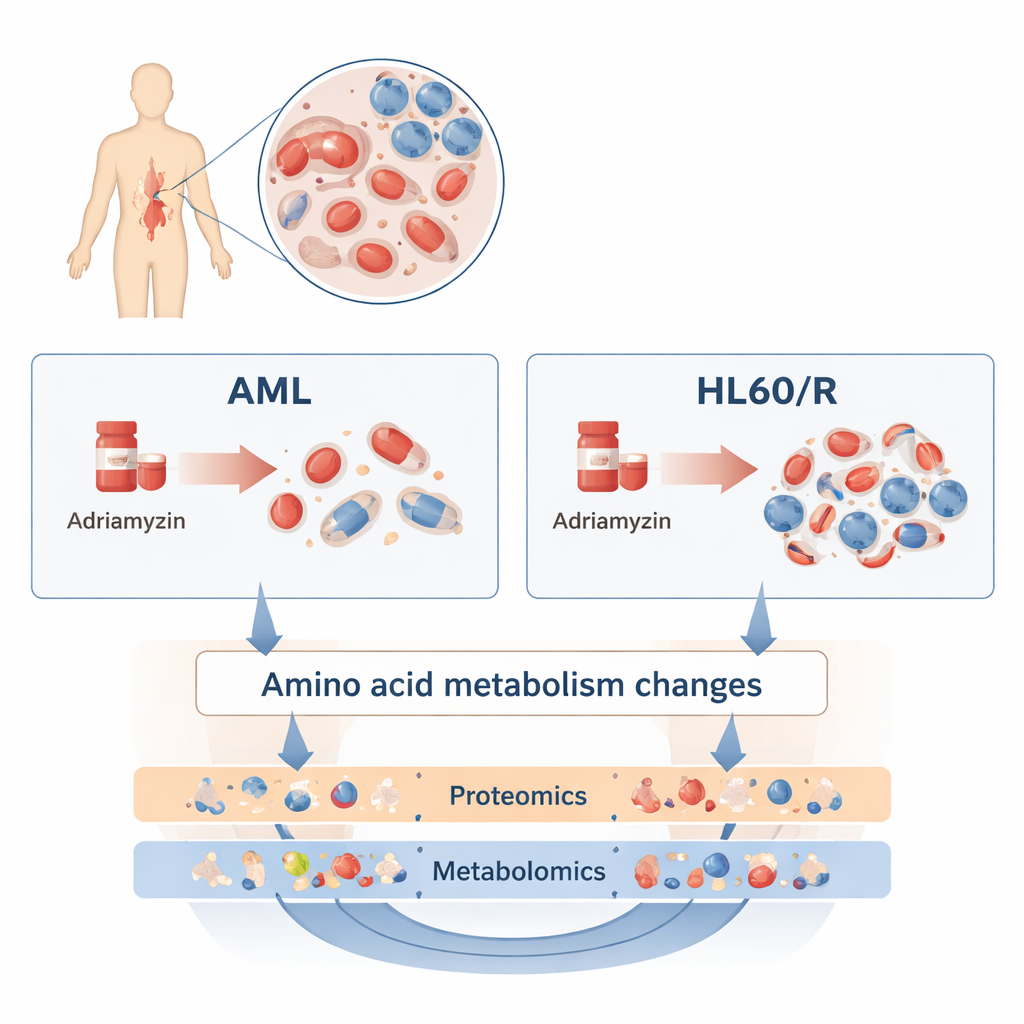
Reconfiguração massiva da maquinaria celular
A investigação proteômica revelou mudanças abrangentes: mais de 3.200 proteínas apresentaram níveis maiores ou menores nas células resistentes à adriamicina em comparação com as células HL60 normais. Muitas dessas proteínas se agruparam em vias que controlam como as células usam energia e respondem ao estresse. Em particular, proteínas das vias de sinalização do AMP cíclico (cAMP), da via HIF‑1 (que ajuda as células a lidar com baixo oxigênio) e da fosforilação oxidativa (um processo-chave de produção de energia nas mitocôndrias) foram alteradas. Essas alterações sugerem que as células leucêmicas resistentes reprogramam como respiram, crescem e se comunicam para suportar a quimioterapia.
Metabolismo desloca-se para aminoácidos
A análise metabolômica contou uma história complementar. De cerca de 1.400 metabólitos detectados, 260 mudaram de forma significativa nas células resistentes. Modelos estatísticos separaram claramente as células resistentes das não resistentes, indicando uma assinatura metabólica consistente de resistência. Quando os metabólitos alterados foram mapeados em rotas bioquímicas conhecidas, várias vias se destacaram. Muitas das rotas mais afetadas estavam ligadas aos aminoácidos, os blocos de construção das proteínas — especialmente aquelas envolvendo alanina, aspartato, glutamato, cisteína, metionina e glutationa. Outras redes, como o metabolismo de purinas e pirimidinas (importante para DNA e RNA) e o manejo de certos lipídios, também foram perturbadas, ressaltando que a resistência está associada a uma ampla remodelação metabólica.
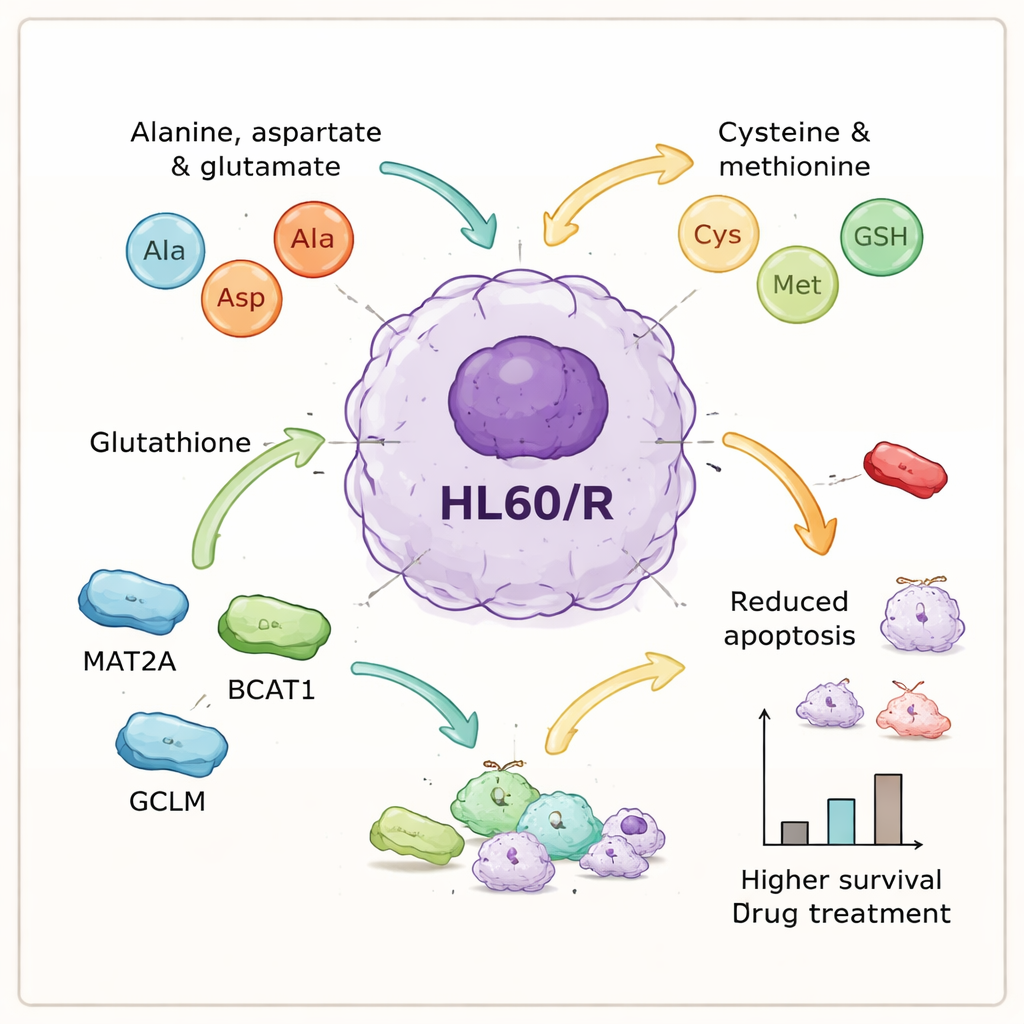
Principais moléculas que ajudam as células cancerígenas a resistir
Ao integrar os dados de proteínas e metabólitos, os autores focaram em um conjunto de processos relacionados a aminoácidos que pareciam centrais para a resistência. Selecionaram seis proteínas ligadas a essas vias — GOT1, GPX1, AHCY, MAT2A, BCAT1 e GCLM — para inspeção mais detalhada. Testes de laboratório confirmaram que cinco delas eram mais abundantes nas células resistentes, consistente com a ideia de que o processamento de aminoácidos está intensificado, enquanto uma enzima antioxidante, GPX1, estava reduzida. Para sondar causa e efeito, a equipe usou RNAs de interferência pequena para reduzir a expressão de três das proteínas reguladas para cima — MAT2A, BCAT1 e GCLM — nas células resistentes. Quando essas proteínas foram silenciadas, as células apresentaram muito mais morte celular programada após o tratamento, ou seja, perderam grande parte de sua proteção conquistada contra a adriamicina.
O que isso significa para tratamentos futuros
Em conjunto, esses achados sugerem que as células de LMA resistentes à adriamicina sobrevivem não apenas por mutações isoladas, mas porque remodelam sua química interna, com o metabolismo de aminoácidos atuando como um centro-chave. Ao direcionar mais recursos para vias específicas de aminoácidos e glutationa, as células parecem mais aptas a gerenciar estresse, reparar danos e evitar a morte quando expostas à quimioterapia. Para não especialistas, a mensagem principal é que a resistência não é aleatória: segue padrões identificáveis que podem ser medidos e, potencialmente, alvo de intervenção. A longo prazo, fármacos que interfiram em proteínas específicas do processamento de aminoácidos, como MAT2A, BCAT1 ou GCLM, poderiam ser combinados com adriamicina ou agentes similares, oferecendo aos clínicos novas ferramentas para prevenir ou contornar a resistência em pacientes com leucemia mieloide aguda.
Citação: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Palavras-chave: leucemia mieloide aguda, resistência a medicamentos, adriamicina, metabolismo de aminoácidos, multi-ômica