Clear Sky Science · pt
Um modelo celular funcional e robusto para triagem em larga escala de moduladores de Piezo1
Por que sensores de pressão minúsculos em nossas células importam
Cada vez que o sangue corre pelos nossos vasos ou simplesmente caminhamos por um cômodo, nossas células sentem forças mecânicas minúsculas. Uma proteína chave de “sensor de pressão” chamada Piezo1 ajuda as células a traduzir essas forças em sinais elétricos e químicos que mantêm os tecidos saudáveis. Como o Piezo1 participa do crescimento de vasos sanguíneos, da força óssea, da imunidade e de doenças genéticas raras, desenvolvedores de medicamentos querem encontrar moléculas que possam ajustar sua atividade. O artigo descrito aqui apresenta uma maneira nova e mais rápida de buscar essas moléculas usando células geneticamente modificadas e leituras baseadas em luz, em vez de técnicas lentas e trabalhosas.
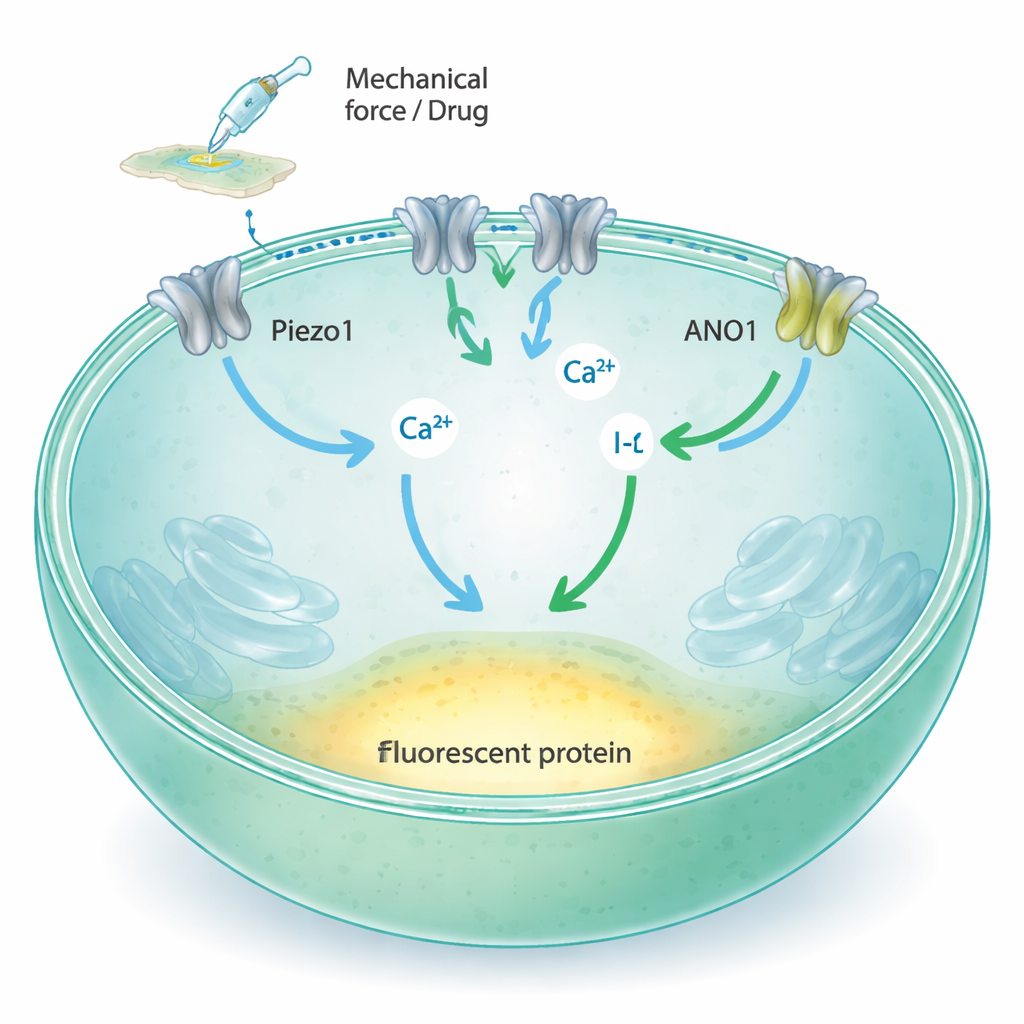
Transformando toque em um sinal luminoso
O Piezo1 é um canal na membrana celular que se abre quando a membrana é esticada ou pressionada, permitindo que cálcio e outros íons carregados entrem na célula. Métodos tradicionais para estudar esses canais dependem de microeletrodos de vidro ou repórteres fluorescentes especializados, que são poderosos, mas difíceis de escalonar para as dezenas de milhares de testes necessários na descoberta moderna de fármacos. Os autores propuseram converter a atividade do Piezo1 em uma simples variação de luz que um leitor de placas pode medir rapidamente em muitas amostras ao mesmo tempo. A ideia foi ligar o Piezo1 a dois componentes adicionais: ANO1, outro canal iônico que responde ao cálcio, e uma proteína fluorescente amarela modificada que perde brilho quando exposta a íons iodeto.
Construindo uma célula-teste responsiva
Os pesquisadores começaram com células de tireoide de rato Fischer (FRT), que produzem Piezo1 naturalmente e aderem bem a placas plásticas padrão. Eles confirmaram que essas células expressam Piezo1, mas não seu parente próximo Piezo2, e demonstraram que o Piezo1 nessas células responde ao fluxo de fluido e à sondagem mecânica permitindo a entrada de cálcio. Em seguida, introduziram o canal ANO1 e a proteína fluorescente sensível a iodeto (YFP‑H148Q/I152L) nas células. Quando o cálcio aumenta dentro da célula, o ANO1 se abre e permite a entrada de iodeto; a proteína fluorescente então fica mais apagada à medida que o iodeto se acumula ao seu redor. Microscopia, citometria de fluxo e registros elétricos mostraram que tanto o ANO1 quanto o sensor fluorescente estavam presentes em níveis elevados e funcionando conforme esperado.
Da ação de um fármaco a um brilho mensurável
Com esse sistema tripartido em funcionamento, a equipe criou uma cadeia simples de causa e efeito: se uma molécula de teste ativa o Piezo1, o cálcio entra, o ANO1 se abre, o iodeto entra em massa e o sinal de fluorescência cai; se uma molécula bloqueia o Piezo1, o sinal permanece brilhante. Eles validaram essa lógica usando ativadores bem conhecidos do Piezo1 (Yoda1, Jedi1, Jedi2) e bloqueadores (Ruthenium Red, GsMTx4). Os ativadores produziram reduções dependentes da dose na fluorescência, com valores de sensibilidade compatíveis com dados previamente relatados. Os bloqueadores causaram o padrão oposto, reduzindo a resposta conforme sua concentração aumentava. O ensaio funcionou somente quando cálcio e iodeto estavam presentes, ressaltando que o sinal dependia verdadeiramente da entrada de cálcio provocada pelo Piezo1 e do subsequente influxo de iodeto mediado pelo ANO1. Medidas estatísticas como o fator Z e a razão sinal‑ruído indicaram que o método é estável e confiável o suficiente para triagens em escala industrial.
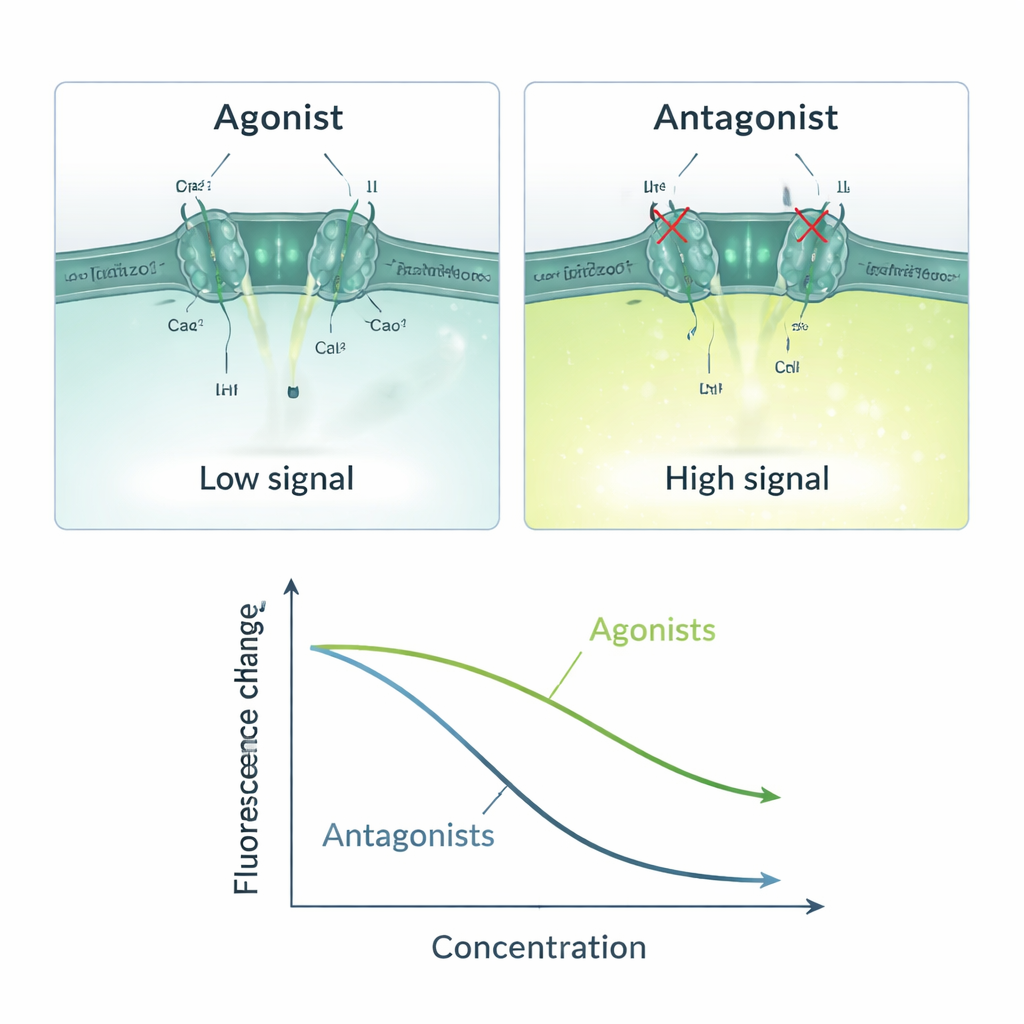
Testes rápidos e escaláveis, com algumas ressalvas
O novo modelo celular pode concluir uma medição de poço em cerca de 14 segundos e escanear uma placa de 96 poços em aproximadamente 22 minutos, e pode ser adaptado a instrumentos que leem centenas de poços simultaneamente. As células modificadas permanecem estáveis por muitas gerações sob seleção por antibiótico, permitindo experimentos repetidos ao longo do tempo. Como a leitura é óptica e usa equipamentos padrão de microplacas, a abordagem é relativamente de baixo custo e acessível. Entretanto, os autores observam que o teste é indireto: qualquer composto que atue em etapas anteriores ou posteriores ao Piezo1 na cadeia de sinalização — como o próprio ANO1 ou outras proteínas que lidam com cálcio — pode gerar um falso positivo. Por essa razão, os resultados promissores dessa triagem ainda precisam ser confirmados com métodos mais diretos, como a eletrofisiologia.
O que isso significa para tratamentos futuros
Em termos cotidianos, os pesquisadores construíram um “alarme de fumaça” de bancada que pisca mais fraco sempre que um composto empurra o Piezo1 para abrir, e permanece brilhante quando o Piezo1 está bloqueado. Esse alarme é sensível, rápido e fácil de executar em grande número, tornando‑o bem adequado para a triagem inicial na busca por fármacos que ajustem os sensores mecânicos do corpo. Embora não substitua testes de acompanhamento mais detalhados, esse modelo celular fornece um ponto de partida poderoso para descobrir moléculas que, um dia, podem ajudar a tratar distúrbios vasculares, doenças ósseas, problemas imunológicos e outras condições ligadas à forma como nossas células sentem e respondem à força física.
Citação: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Palavras-chave: Canais Piezo1, canais iônicos mecanossensíveis, triagem em larga escala, ensaio em células, descoberta de fármacos