Clear Sky Science · pt
Resposta quimiossensória a quimioterápicos à base de Pt via receptores do gosto amargo in vitro revela um novo mecanismo para distúrbios do paladar amargo
Por que os remédios contra o câncer podem, de repente, fazer tudo ter gosto horrível
Pacientes com câncer frequentemente relatam que a comida começa a ter um gosto estranhamente amargo ou metálico logo após o início da quimioterapia. Isso vai além de estragar as refeições: pode reduzir o apetite, promover perda de peso e afetar a qualidade de vida justamente quando o paciente mais precisa de força. Este estudo faz uma pergunta aparentemente simples, mas de grande consequência prática: como exatamente os medicamentos quimioterápicos comuns à base de platina interferem em nosso sentido do paladar, e esse efeito pode ser reduzido com segurança sem enfraquecer o tratamento?
O papel oculto dos “sensores de amargor” na boca e no intestino
Nossas línguas e trato digestivo estão pontilhados de receptores do gosto amargo, projetados para nos avisar sobre substâncias potencialmente nocivas. Esses sensores, conhecidos como TAS2Rs, não se limitam às papilas gustativas; também são encontrados em células do estômago. Os pesquisadores usaram uma linhagem celular gástrica humana (HGT-1) que funciona como um detector de amargor in vitro: quando os receptores amargos são ativados, as células bombeiam mais prótons (ácido), o que pode ser medido como uma mudança em um índice chamado índice de prótons intracelulares. Ao expor essas células a dois fármacos oncológicos amplamente usados à base de platina — carboplatina e cisplatina — a equipe pôde sondar com segurança o quão “amargos” esses fármacos parecem para células humanas sem jamais pedir que uma pessoa prove um composto tóxico. 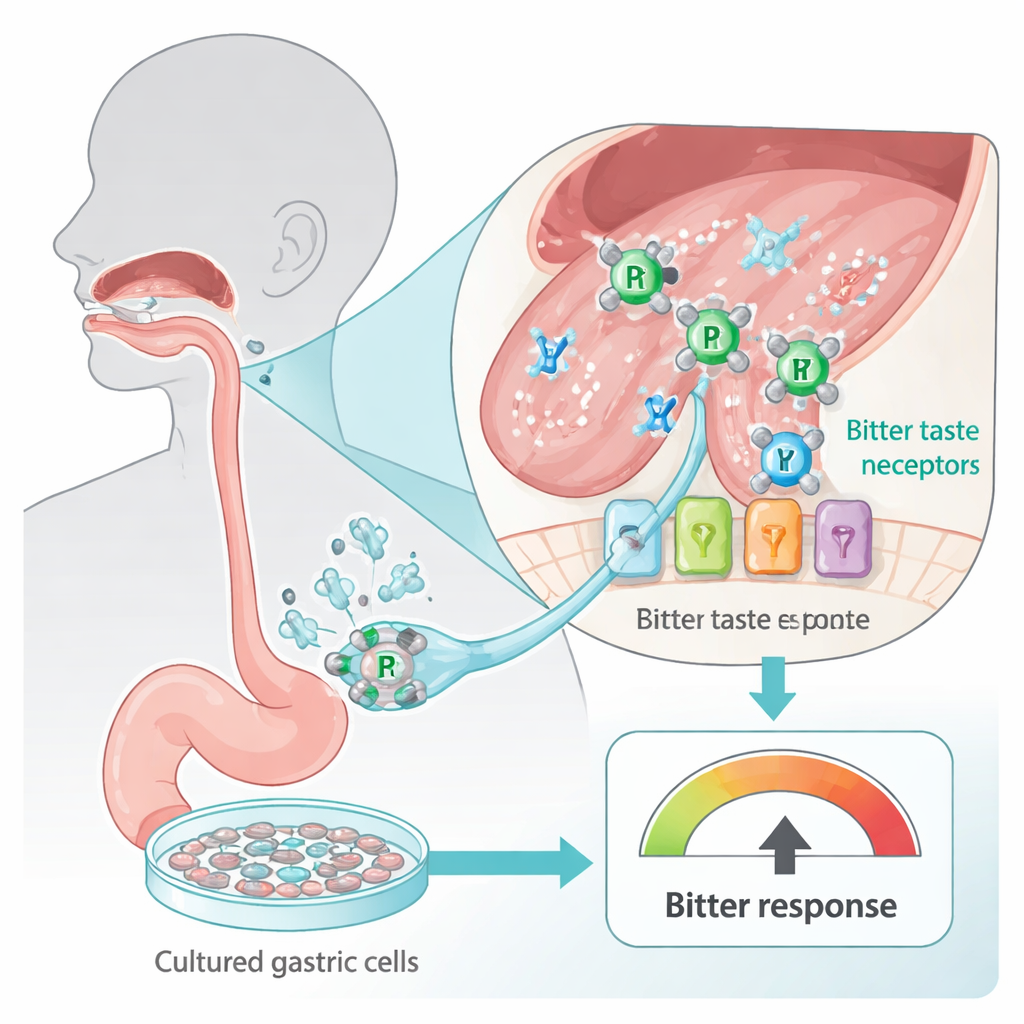
Fármacos de quimioterapia que soam amargos para as células
Quando as células gástricas foram tratadas com concentrações clinicamente relevantes de carboplatina e cisplatina, ambos os fármacos desencadearam uma resposta semelhante ao amargor, dependente da dose: quanto maior a dose, mais intensa a reação celular. A cisplatina, no entanto, produziu uma resposta mais intensa do que a carboplatina quando se considerou a relação de dose terapêutica usual entre eles (cerca de 1:4), sugerindo que ela pode contribuir de forma mais significativa para os problemas de gosto amargo em pacientes. No nível genético, a exposição a esses fármacos alterou a atividade de múltiplos genes de receptores amargos nas células, indicando que os compostos de platina não atuam em um único “interruptor do amargor”, mas remodelam amplamente o sistema de detecção do amargor. Entre esses receptores, TAS2R4 e TAS2R5 destacaram-se por serem altamente ativos e fortemente afetados pelo tratamento.
Desativando sinais de amargor e testando um bloqueador natural do amargor
Para identificar quais receptores importam mais, a equipe desativou seletivamente receptores amargos específicos. Eliminar TAS2R4 ou reduzir a expressão de TAS2R5 diminuiu a resposta semelhante ao amargor provocada pela carboplatina e pela cisplatina, confirmando que esses receptores ajudam a detectar os fármacos. Os cientistas então testaram uma contramedida promissora: o sal de sódio do homoeriodictyol (Na-HED), um flavanona originalmente isolada da planta norte-americana Herba Santa e já conhecida por mascarar o amargor de outros compostos. Quando Na-HED foi adicionado juntamente com os fármacos de platina, atenuou marcadamente a resposta celular ao amargor — em cerca de três quartos para ambos carboplatina e cisplatina — sem prejudicar as células por si só. Isso mostra que Na-HED pode agir diretamente sobre os receptores amargos para enfraquecer o sinal desencadeado pelos medicamentos de quimioterapia.
Quando detecção de amargor e captação do fármaco se cruzam
Além de explicar por que a quimioterapia à base de platina pode ter gosto amargo, o estudo revela uma reviravolta inesperada: os mesmos receptores do amargor também parecem influenciar o quanto desses fármacos entram nas células. Usando espectrometria de massa altamente sensível, os pesquisadores mediram o teor de platina dentro das células após o tratamento. Células sem certos receptores, como TAS2R4 ou TAS2R43, acumularam mais platina do que células normais, sugerindo que receptores intactos ajudam a limitar a captação ou retenção celular desses agentes tóxicos. Na-HED não alterou a captação de carboplatina, mas reduziu a quantidade de cisplatina que entrou nas células e mostrou interação molecular direta com cisplatina em solução. Isso sugere que um composto mascarador de amargor pode, em alguns casos, também modular o quanto um fármaco afeta tecidos locais, como células gustativas ou glândulas salivares. 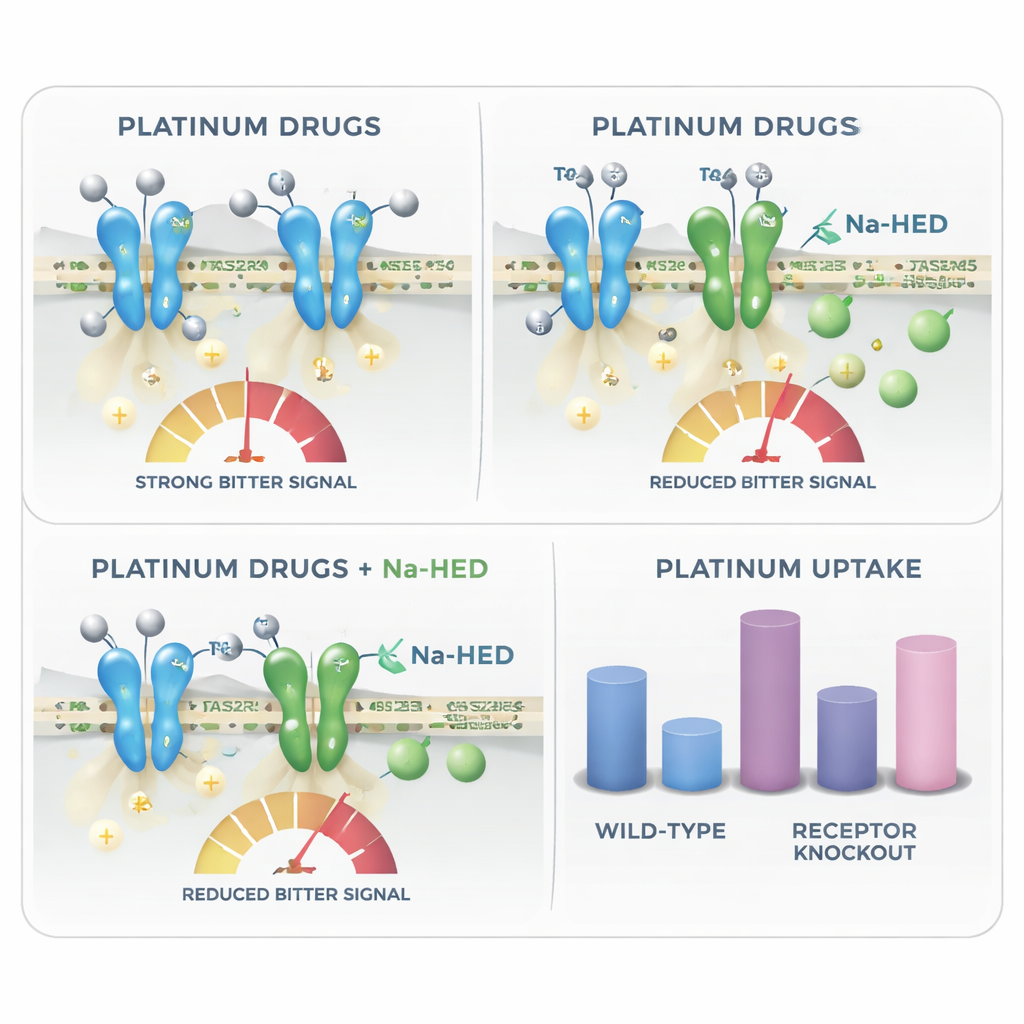
Rumo a experiências gustativas mais suaves durante a quimioterapia
Para os pacientes, a principal conclusão é esperançosa: a quimioterapia à base de platina parece desencadear problemas de gosto amargo ao ativar diretamente receptores do amargor que existem não apenas na língua, mas também em células semelhantes às do trato gastrointestinal. A cisplatina mostra-se particularmente potente nesse aspecto. O estudo demonstra que Na-HED pode reduzir substancialmente esse sinal amargo em um sistema celular controlado e pode também limitar a captação local de cisplatina. Embora essas descobertas precisem ser confirmadas em humanos, elas apontam para futuros tratamentos bucais de “bochecho e cuspir” contendo Na-HED que poderiam suavizar sensações amargas e metálicas sem interferir na ação antitumoral dos medicamentos em todo o corpo.
Citação: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Palavras-chave: alterações do paladar por quimioterapia, receptores do gosto amargo, cisplatina e carboplatina, compostos mascaradores de amargor, nutrição de pacientes com câncer