Clear Sky Science · pt
Cálculo DFT da complexação de Ac3+ e Bi3+ com o quelante híbrido 3p-C-DEPA para terapia alfa direcionada
Por que esta pesquisa importa para o tratamento do câncer
A medicina moderna do câncer depende cada vez mais de fármacos radioativos capazes de localizar tumores célula a célula. Uma abordagem poderosa, chamada terapia alfa direcionada, usa partículas extremamente energéticas que podem matar células cancerosas individuais com notável precisão. Mas para entregar essas partículas com segurança, o metal radioativo precisa ser preso em uma pequena “gaiola” molecular para não migrar para tecidos saudáveis. Este estudo explora uma nova molécula gaiola, 3p‑C‑DEPA, projetada para acomodar metais especialmente desafiadores, como actínio‑225 e bismuto‑213, e pergunta: ela consegue prendê‑los com mais firmeza que o quelante padrão atual, DOTA?
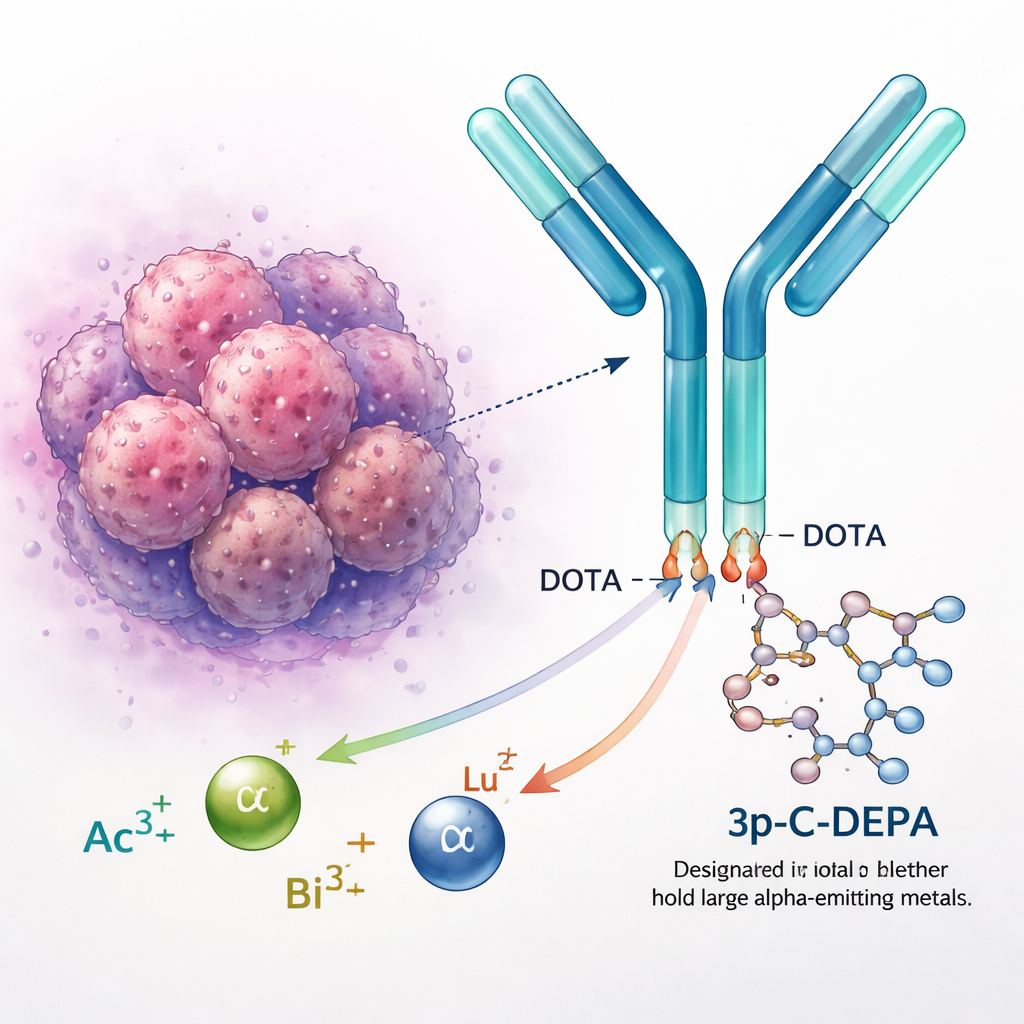
Fixando metais radioativos com segurança
Metais radioativos como actínio, bismuto e lutécio são usados no diagnóstico e tratamento do câncer. Sozinhos, porém, esses íons metálicos carregados positivamente interagiriam livremente com o corpo, podendo danificar órgãos saudáveis. Químicos, portanto, os ligam a “quelantes”, moléculas em forma de anel que envolvem o metal e o mantêm no lugar. O quelante padrão DOTA é usado em vários medicamentos aprovados, mas tem dificuldade com íons maiores e mais difusos, como o actínio‑225. Esses metais podem escapar ao longo do tempo, gerando preocupações sobre a segurança a longo prazo e limitando o uso mais amplo da terapia alfa direcionada.
Uma gaiola híbrida construída para átomos maiores
O novo quelante, 3p‑C‑DEPA, combina características de dois projetos estabelecidos: a estrutura rígida e anelar do DOTA e a arquitetura mais flexível e aberta de outro quelante chamado DTPA. Essa arquitetura híbrida confere ao 3p‑C‑DEPA dez “mãos” de ligação fortes (átomos de nitrogênio e oxigênio) em comparação com as oito do DOTA, além de uma cavidade mais espaçosa que pode acomodar melhor íons metálicos grandes. Trabalhos laboratoriais anteriores sugeriram que o 3p‑C‑DEPA pode marcar anticorpos rapidamente a temperaturas moderadas e manter radionuclídeos à base de bismuto estáveis em soro sanguíneo. O estudo atual avança um passo, usando cálculos em nível quântico para comparar sistematicamente quão bem 3p‑C‑DEPA e DOTA ligam lutécio‑177, bismuto‑213 e actínio‑225.
Olhando para o aperto molecular
Como trabalhar diretamente com emissores alfa de vida curta é difícil, os pesquisadores recorreram à teoria do funcional da densidade (DFT), um método computacional poderoso que estima como os elétrons estão arranjados em moléculas e quão fortemente os átomos se atraem. Eles modelaram cada íon metálico em água, depois seu complexo com DOTA ou com 3p‑C‑DEPA, e calcularam a variação de energia livre quando o metal passa da água para a gaiola do quelante. Essa mudança de energia é traduzida em uma “constante de estabilidade”: quanto maior o valor, mais firmemente o quelante segura o metal. Duas abordagens DFT diferentes e dois modelos de solvação foram usados para simular condições realistas de solução e verificar que as tendências eram robustas e não artefatos de uma única configuração computacional.
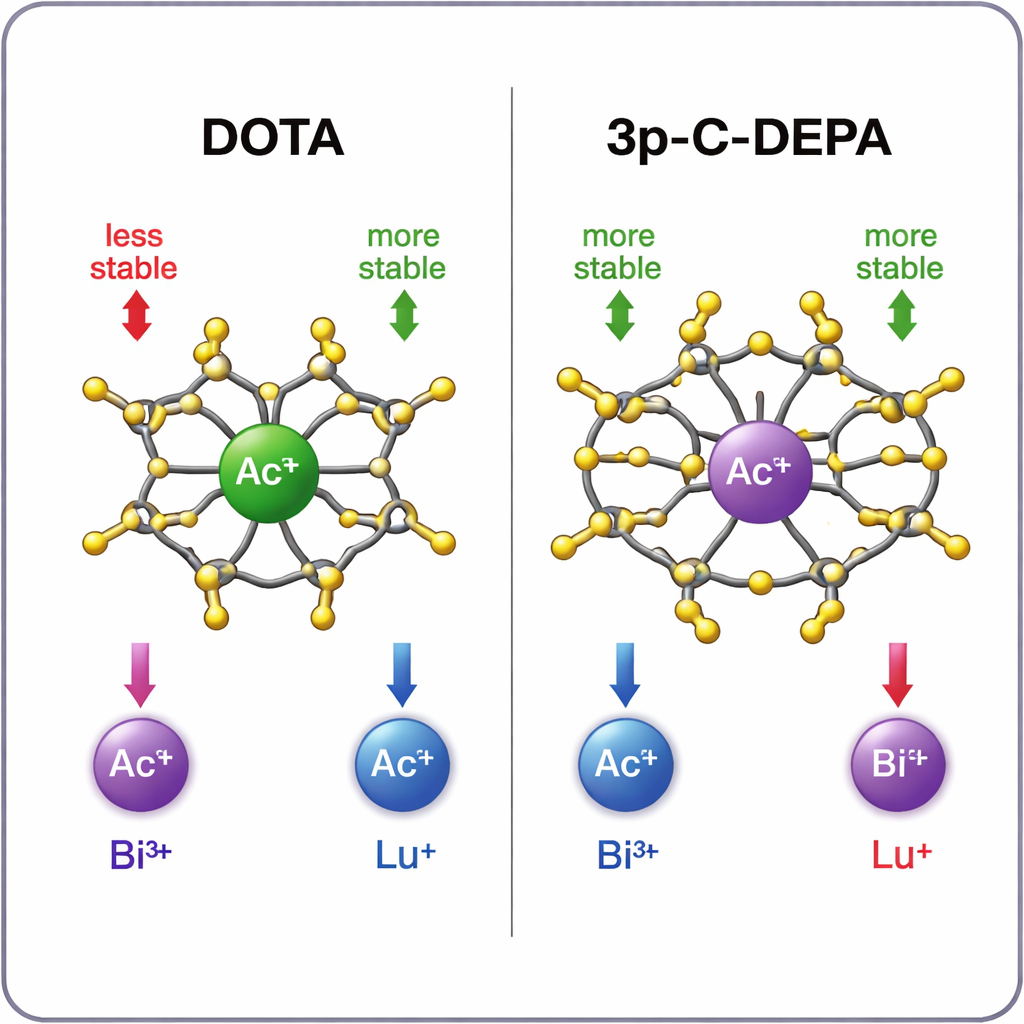
Qual gaiola segura melhor cada metal?
As simulações mostram um padrão claro. Para o grande íon de actínio, o 3p‑C‑DEPA forma um complexo marcadamente mais estável que o DOTA, graças à sua cavidade maior e ao maior número de doadores de oxigênio que conseguem agarrar o metal. O bismuto‑213 também é bem acomodado pelo 3p‑C‑DEPA, beneficiando‑se tanto do seu tamanho quanto de sua natureza de aceitador de elétrons, que casa com os grupos doadores de elétrons do quelante. Em contraste, o menor lutécio‑177 se ajusta mais confortavelmente ao ambiente mais apertado e de oito “braços” do DOTA. No 3p‑C‑DEPA, grupos doadores em excesso se amontoam em torno do pequeno íon, gerando interações repulsivas que parecem retardar a marcação e enfraquecer ligeiramente o complexo final. As tendências de estabilidade calculadas concordam bem com os dados experimentais disponíveis e os rendimentos de radiomarcação, conferindo credibilidade às previsões teóricas.
O que isso significa para futuras terapias contra o câncer
Em termos práticos, o estudo sugere que o DOTA não é uma gaiola única para todos: ele funciona muito bem para metais menores como o lutécio, mas é subótimo para emissores alfa mais volumosos, como o actínio‑225. O 3p‑C‑DEPA, por sua vez, comporta‑se como um suporte sob medida para esses íons maiores, agarrando‑os com mais firmeza e sob condições mais suaves, compatíveis com moléculas de direcionamento delicadas como anticorpos. Embora sejam necessários mais trabalhos experimentais e clínicos, os cálculos indicam o 3p‑C‑DEPA como uma plataforma promissora para terapias alfa direcionadas mais seguras e eficazes — potencialmente expandindo o acesso a tratamentos oncológicos altamente potentes que podem erradicar tumores preservando o tecido saudável ao redor.
Citação: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Palavras-chave: terapia alfa direcionada, radiofármacos, projeto de quelantes, actínio-225, teoria do funcional da densidade