Clear Sky Science · pt
Investigação experimental e correlação termodinâmica da solubilidade da clordiazepóxido em CO₂ supercrítico
Por que dissolver um fármaco conhecido de uma nova forma importa
Muitos medicamentos modernos são eficazes, mas difíceis de formular de maneira eficiente: podem não se dissolver facilmente, degradar durante a fabricação ou exigir grandes quantidades de solventes orgânicos. Este estudo investiga a clordiazepóxido, um medicamento usado há muito tempo para ansiedade, e faz uma pergunta prática com impacto amplo: quão bem ela se dissolve em dióxido de carbono supercrítico, um solvente mais limpo e ajustável que poderia ajudar a produzir partículas farmacêuticas mais seguras e eficazes?
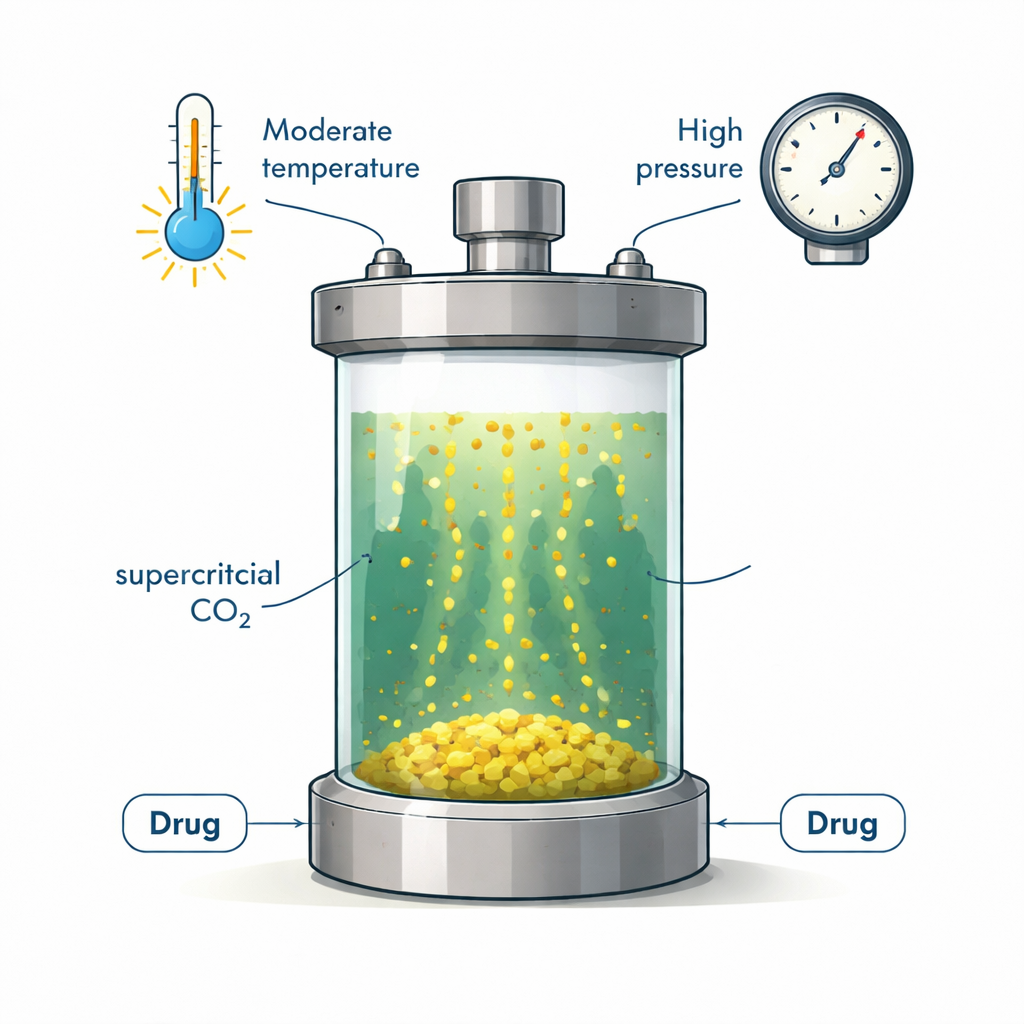
Um fluido verde que se comporta como gás e líquido
O dióxido de carbono supercrítico é o CO₂ levado acima de uma certa pressão e temperatura até que não seja nem um gás típico nem um líquido comum. Nesse estado ele flui como um gás, mas tem densidade semelhante à de um líquido e pode dissolver muitas substâncias. A indústria já o usa para descafeinar café e extrair aromas e óleos. Para produtos farmacêuticos, o CO₂ supercrítico é atraente porque é não tóxico, aceito pelos reguladores, barato e fácil de reciclar. Pode ajudar a criar partículas de fármaco pequenas e uniformes e reduzir a necessidade de solventes orgânicos agressivos — se, e somente se, o fármaco realmente se dissolver nele em extensão útil.
Medindo como um ansiolítico se comporta sob pressão
Os autores propuseram medir, pela primeira vez, quanto clordiazepóxido se dissolve em CO₂ supercrítico puro dentro de uma janela prática de processamento. Colocaram pó sólido do fármaco em uma célula de alta pressão e fizeram fluir CO₂ por ela a pressões entre 12 e 30 megapascais e temperaturas entre 308 e 338 kelvin (aproximadamente 35–65 °C). Após permitir que o sistema atingisse o equilíbrio, amostraram a fase de CO₂, expandiram-na rapidamente em um solvente e usaram absorção no ultravioleta-visível para determinar quanto fármaco havia sido dissolvido. A solubilidade total variou de cerca de 20 a 576 partes por milhão, correspondendo a frações molares entre 0,0198×10⁻³ e 0,576×10⁻³, valores em linha com muitos outros fármacos moderadamente solúveis em CO₂ supercrítico.
Como pressão e temperatura moldam a solubilidade
As medições revelaram padrões claros e intuitivos. A uma temperatura fixa, aumentar a pressão sempre elevou a solubilidade. Maior pressão aproxima as moléculas de CO₂, tornando a fase supercrítica mais densa e mais eficiente em envolver e transportar moléculas do fármaco. A temperatura teve um efeito mais sutil. Em pressões mais baixas, o aquecimento do sistema tendia a reduzir a solubilidade porque rarefazia o CO₂ e diminuiu seu poder de solvatação. Acima de uma pressão de cruzamento de aproximadamente 19 megapascais, a tendência se inverteu: temperaturas mais altas aumentaram a solubilidade porque favoreceram a tendência do fármaco de escapar do estado sólido para o fluido. Esse equilíbrio entre a densidade do fluido e a volatilidade do fármaco é uma marca dos sistemas supercríticos e é importante para escolher condições operacionais práticas.
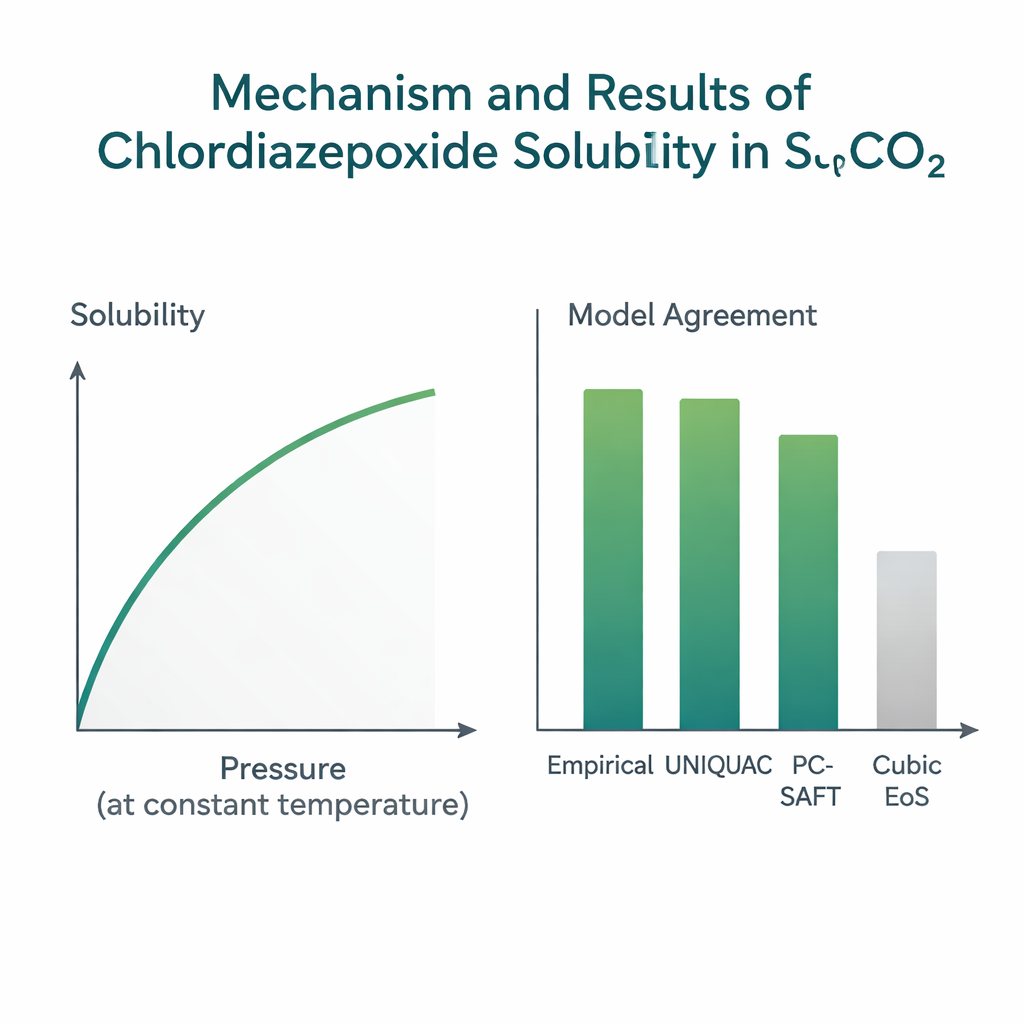
Ensinando modelos a prever o que o laboratório observa
Como realizar experimentos de alta pressão é lento e caro, engenheiros confiam em modelos matemáticos para prever a solubilidade em novas condições ou para fármacos relacionados. A equipe testou várias famílias de modelos usando seu novo conjunto de dados. Fórmulas empíricas simples “baseadas em densidade”, que vinculam a solubilidade diretamente à densidade do CO₂ e à temperatura usando apenas alguns parâmetros de ajuste, tiveram o melhor desempenho. Em particular, a correlação bem estabelecida de Chrastil ajustou-se aos dados com um desvio médio de cerca de 5%, e outras fórmulas semelhantes também se saíram bem. Uma abordagem fisicamente mais detalhada de “líquido expandido” chamada UNIQUAC, que leva em conta tamanho, forma molecular e energias de interação, alcançou precisão comparável, em torno de 6% de desvio. Em contraste, equações de estado cúbicas comumente usadas — fórmulas de uso geral para o comportamento de fluidos — mostraram desvios próximos de 20%, não capturando detalhes mais finos de como este fármaco específico interage com o CO₂.
O que isso significa para a fabricação futura de fármacos
Em termos simples, o estudo mostra que a clordiazepóxido se dissolve em CO₂ supercrítico em condições tecnologicamente relevantes, e que seu comportamento pode ser capturado muito bem com modelos relativamente simples e bem escolhidos. Isso fornece um mapa confiável para projetar processos mais verdes para fabricar novas formas sólidas ou nanopartículas do fármaco, o que pode melhorar sua estabilidade ou absorção no organismo. Mais amplamente, o trabalho oferece um raro conjunto de dados cuidadosamente medidos para um medicamento amplamente usado e demonstra quais ferramentas de modelagem são mais confiáveis ao planejar processos com CO₂ supercrítico — informação que pode orientar uma fabricação mais limpa e eficiente de muitos outros fármacos.
Citação: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Palavras-chave: dióxido de carbono supercrítico, solubilidade de fármacos, clordiazepóxido, processamento farmacêutico verde, modelagem termodinâmica