Clear Sky Science · pt
Uma abordagem de proteômica e proteômica redox para entender a heterogeneidade da SDRA
Por que isso importa para pessoas em unidade de terapia intensiva
A Síndrome do Desconforto Respiratório Agudo (SDRA) é uma forma potencialmente fatal de insuficiência pulmonar que pode acometer pessoas com infecções graves, traumas ou outras doenças críticas. Muitos pacientes com SDRA parecem semelhantes à beira do leito, ainda que alguns se recuperem enquanto outros não, e nenhum fármaco foi comprovado capaz de reverter especificamente a síndrome. Este estudo faz uma pergunta simples, mas importante: se examinarmos de perto as proteínas e as reações químicas dentro dos pulmões e do sangue de pacientes com SDRA, podemos revelar “tipos” biológicos ocultos da doença que expliquem por que os desfechos variam tanto?
O olhar dentro dos pulmões, não apenas na corrente sanguínea
Para investigar isso, os pesquisadores acompanharam 16 adultos em uma unidade de terapia intensiva que tinham SDRA e estavam usando ventilação mecânica. Nos primeiros três dias após o diagnóstico, coletaram sangue e uma amostra especial chamada líquido de lavado broncoalveolar (LBA), que é uma lavagem suave dos alvéolos pulmonares. Sempre que possível, repetiram essas coletas ao longo de vários dias. Usando espectrometria de massa de alta resolução, mediram centenas de proteínas em cada amostra (proteômica) e, de forma crucial, também examinaram o grau de oxidação de algumas dessas proteínas (proteômica redox), o que reflete quanto elas foram danificadas ou reguladas por espécies reativas de oxigênio — subprodutos quimicamente agressivos da inflamação.
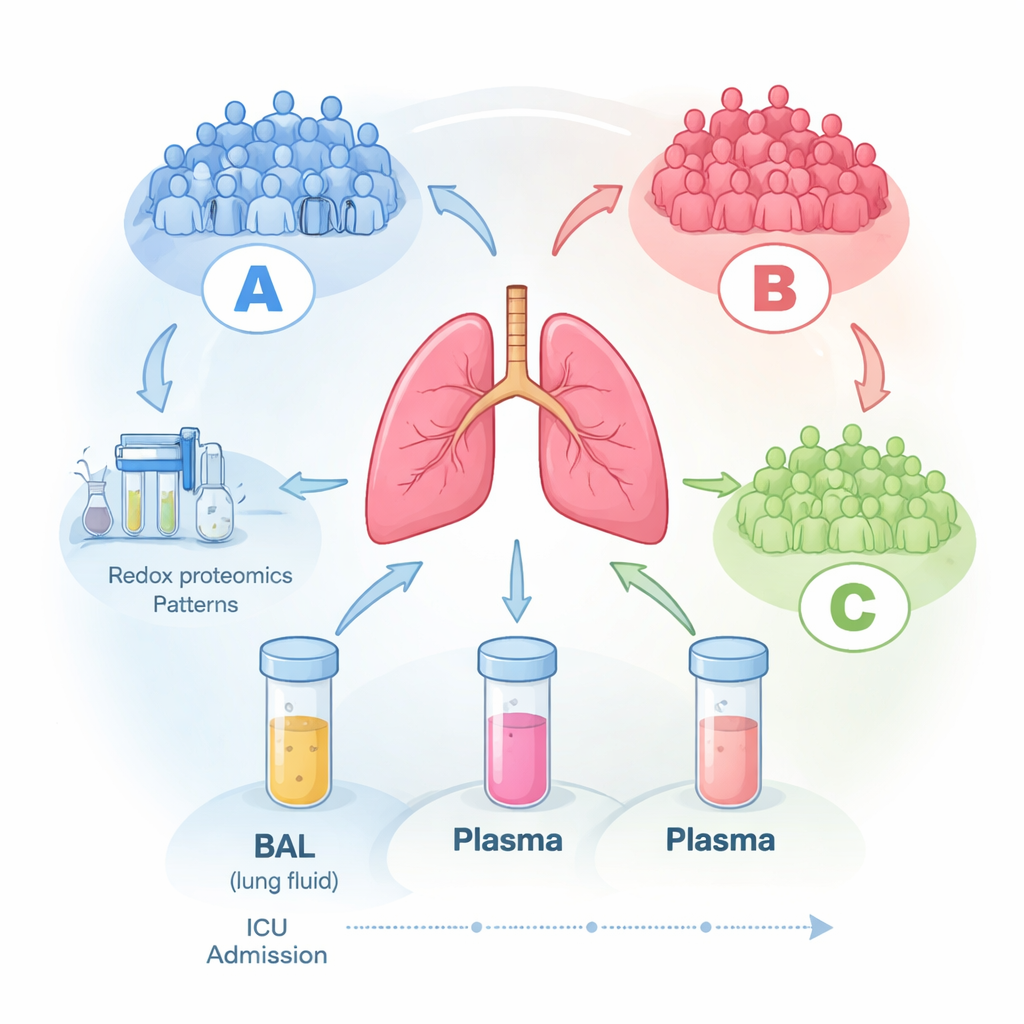
Surgem três grupos ocultos de pacientes
Quando a equipe deixou os dados se agruparem sem informar nada sobre os pacientes ao algoritmo, um padrão claro surgiu nas amostras do líquido pulmonar: três grupos moleculares distintos, rotulados A, B e C. Os pacientes do Grupo A tendiam a estar mais gravemente enfermos na entrada, enquanto os Grupos B e C apresentavam doença mais branda. De forma marcante, essas assinaturas moleculares permaneceram largamente estáveis por até seis dias na UTI, sugerindo que cada paciente se enquadra em um padrão biológico relativamente consistente, em vez de flutuar aleatoriamente dia a dia. Medidas clínicas padrão — como níveis de oxigênio, tempo de internação ou escores gerais de gravidade — não acompanharam bem esses agrupamentos moleculares, indicando que as ferramentas clínicas usuais deixam passar biologia importante que ocorre dentro dos pulmões.
Estresse oxidativo e as defesas do organismo
Um tema central nos dados foi o equilíbrio entre espécies reativas de oxigênio, que causam dano, e as defesas antioxidantes do organismo. No Grupo A, o mais grave, muitas proteínas pulmonares envolvidas na produção de energia e na manutenção celular estavam em níveis mais baixos. Ainda mais revelador, enzimas antioxidantes importantes, como peroxiredoxinas, proteínas relacionadas ao glutationa, tiorredoxina e catalase, estavam significativamente reduzidas. Em contraste, os Grupos B e especialmente C exibiram níveis mais altos dessas proteínas protetoras, sugerindo que seus pulmões estavam melhor equipados para desintoxicar oxidantes nocivos e limitar danos colaterais da inflamação. Padrões no estado de oxidação das proteínas adicionaram outra camada de informação, mostrando subconjuntos diferentes de proteínas oxidadas enriquecidas nos grupos mais e menos graves.
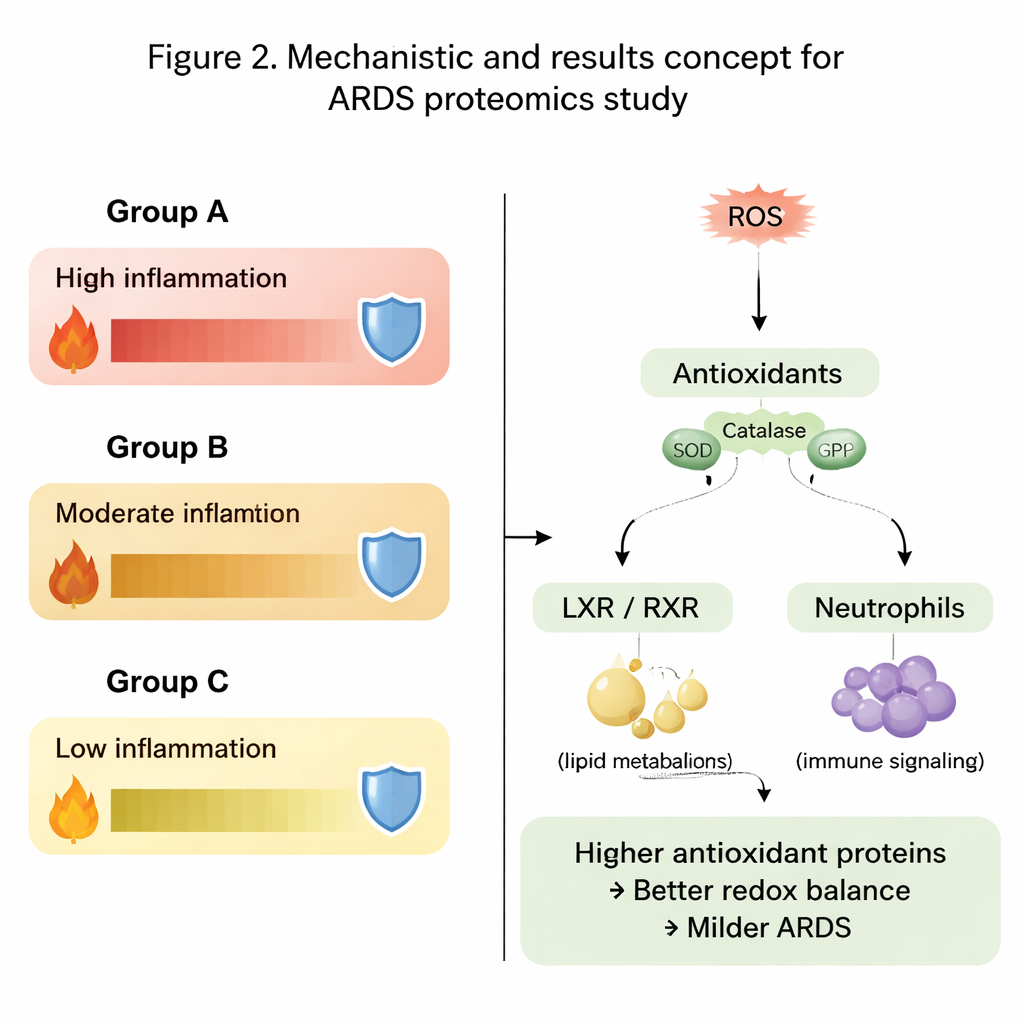
Vias de sinalização que moldam a inflamação
Além de proteínas isoladas, os autores examinaram vias biológicas inteiras. Eles descobriram que vias relacionadas à inflamação, ao manejo de colesterol e lipídios e à atividade de células imunes se comportaram de maneira diferente entre os três grupos. Sinais ligados à via do receptor X do fígado–receptor X retinoide (LXR/RXR) e a uma enzima chamada DHCR24, que juntas ajudam a regular metabolismo lipídico e respostas imunes, foram especialmente notáveis. No grupo mais grave, essas vias foram previstas como mais ativas, associadas a uma sinalização reduzida da interleucina-12, mensageiro imune. Ao mesmo tempo, vias envolvendo espécies reativas de oxigênio, sua desintoxicação e a atividade de neutrófilos (glóbulos brancos) mostraram padrões contrastantes entre o líquido pulmonar e o sangue, reforçando que o que ocorre localmente no pulmão pode diferir do observado na circulação.
O que isso pode significar para cuidados futuros
Este pequeno estudo exploratório não altera o tratamento hoje, e suas descobertas precisam ser confirmadas em grupos de pacientes muito maiores. No entanto, demonstra que, ao perfilar de forma aprofundada proteínas e seu estado redox diretamente no líquido pulmonar — em vez de confiar apenas em testes de sangue ou escores clínicos —, podemos distinguir subtipos biologicamente significativos de SDRA. Esses subtipos diferem em estresse oxidativo, capacidade antioxidante, metabolismo e sinalização imune, e permanecem relativamente estáveis nos primeiros dias críticos da doença. No futuro, essas impressões digitais moleculares poderiam ajudar médicos a classificar pacientes com SDRA em grupos mais precisos, escolher terapias direcionadas a cada padrão e desenhar ensaios clínicos mais inteligentes com maior chance de encontrar tratamentos realmente eficazes.
Citação: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Palavras-chave: síndrome do desconforto respiratório agudo, proteômica, estresse oxidativo, lavado broncoalveolar, cuidados intensivos