Clear Sky Science · pt
Nanoneedles de Co3O4 crescidos sobre óxido de grafeno como eletrocatalisador eficiente para eletrólise híbrida da água por meio de reações anódicas alternativas
Transformando Resíduos Frutíferos em Combustível do Futuro
O hidrogênio é frequentemente celebrado como um combustível limpo do futuro, mas sua produção normalmente exige muita eletricidade. Este estudo mostra como algo tão comum quanto cascas de laranja descartadas pode ajudar a mudar esse quadro. Ao transformar esse resíduo em um material de carbono especial e combiná-lo com um composto à base de cobalto, os pesquisadores criaram um catalisador de baixo custo que pode produzir hidrogênio consumindo muito menos energia do que os métodos convencionais de divisão da água. Paralelamente, eles também substituem uma etapa ineficiente na eletrólise da água por reações mais brandas que convertem compostos problemáticos em gases inofensivos.
Por Que a Separação Tradicional da Água Desperdiça Energia
Para dividir a água em hidrogênio e oxigênio, um eletrólito faz passar corrente elétrica por água contendo um sal ou base dissolvida. Em um dos eletrodos, o gás hidrogênio se forma com facilidade. No outro eletrodo, o oxigênio é produzido por uma reação lenta e exigente, porque envolve a transferência de quatro elétrons em etapas bem coordenadas. Essa etapa de formação de oxigênio, chamada reação anódica, é a que obriga os engenheiros a aumentar a tensão aplicada, elevando o custo energético. Pior ainda, o oxigênio gerado muitas vezes é simplesmente liberado e não aproveitado, o que significa que grande parte da energia elétrica fornecida ao sistema gera pouco valor prático.
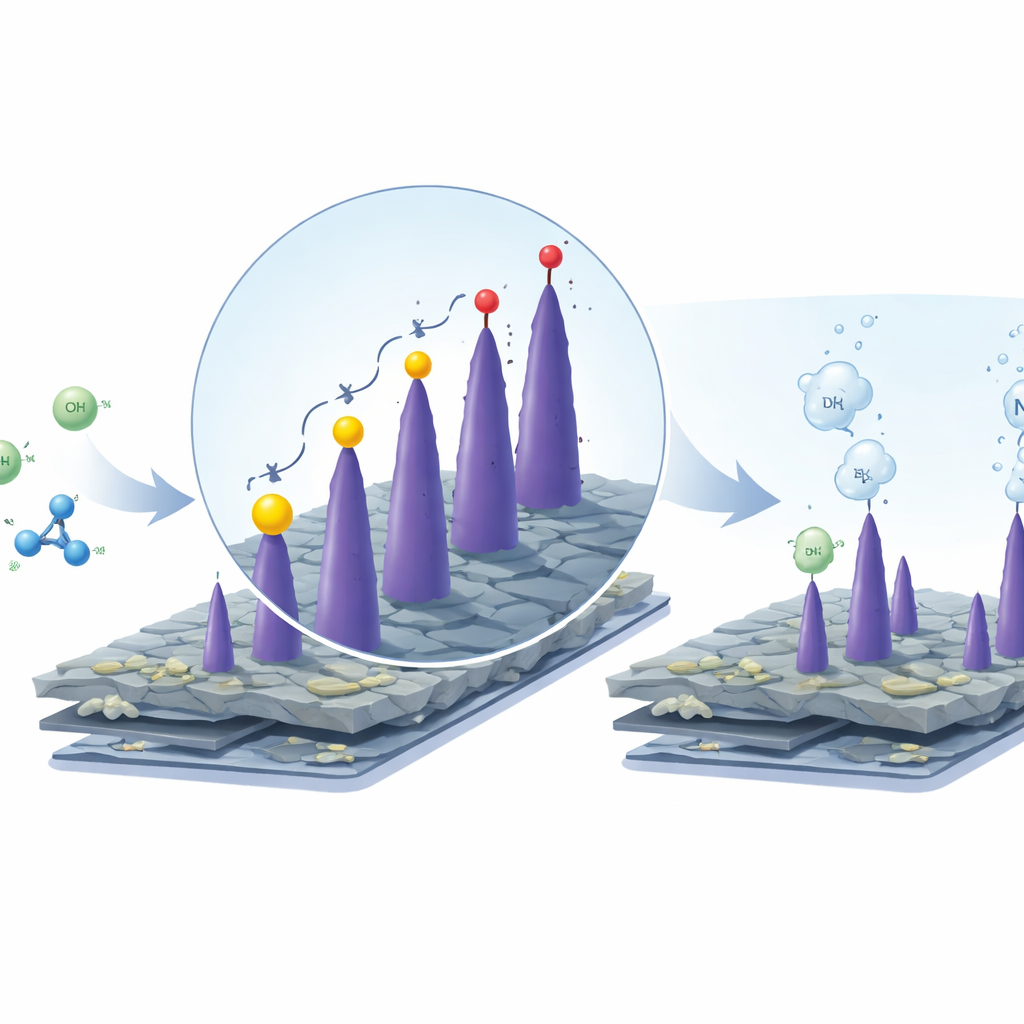
Substituindo um Consumidor de Energia por Reações Mais Brandas
A equipe enfrentou esse gargalo redesenhando o que ocorre no lado que consome mais energia da célula. Em vez de produzir oxigênio a partir da água, perguntaram-se: e se o sistema oxidasse outros químicos mais fáceis de manejar enquanto continua produzindo hidrogênio no eletrodo oposto? Eles escolheram dois compostos ricos em nitrogênio, ureia e hidrazina, comuns em efluentes e processos industriais. Quando essas moléculas são oxidadas em solução alcalina, elas se decompõem em gás nitrogênio, água e, no caso da ureia, dióxido de carbono. Crucialmente, essas reações começam em tensões muito menores do que a produção de oxigênio, o que significa que a mesma quantidade de hidrogênio pode ser gerada com bem menos energia elétrica.
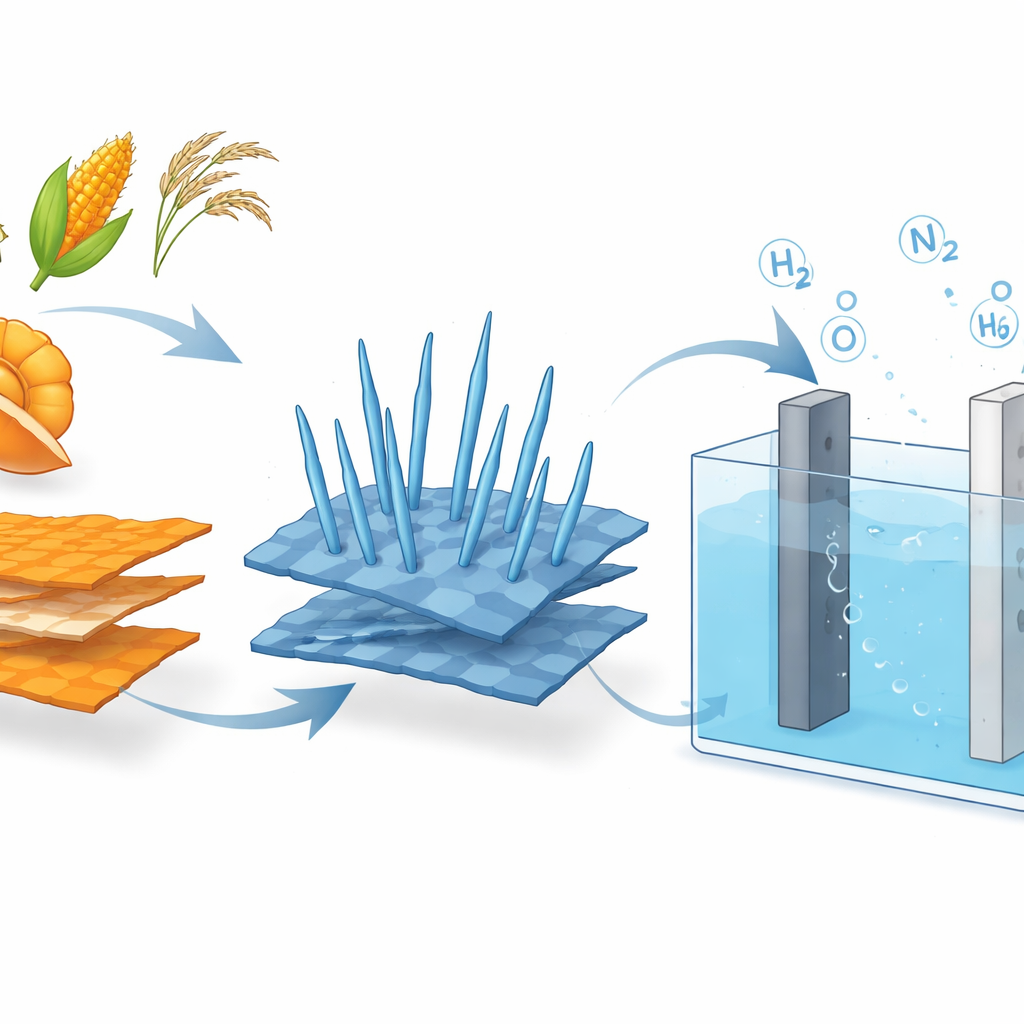
Das Cascas de Laranja a Eletrodos Inteligentes
Para tornar essa abordagem prática, os pesquisadores precisavam de um catalisador barato, robusto e ativo para três tarefas diferentes: produção convencional de oxigênio, oxidação de ureia e oxidação de hidrazina. Eles começaram convertendo cascas de laranja secas em óxido de grafeno, um material de carbono fino e condutor, usando um processo de aquecimento simples em vez de tratamentos químicos agressivos. Sobre essas lâminas, cresceram pequenas “nanoneedles” de óxido de cobalto em um vaso de pressão. O híbrido resultante — nanoneedles de óxido de cobalto sobre óxido de grafeno — forma uma superfície rugosa e esponjosa com muitos sítios reativos expostos e um trajeto fácil para os elétrons. As medições mostraram que o suporte de grafeno impede o agrupamento das partículas de cobalto e aumenta dramaticamente a área de superfície efetiva e a condutividade elétrica.
Como o Novo Catalisador Reduz a Conta de Energia
Quando testado em solução alcalina, o novo eletrodo alcançou uma corrente padrão de referência em tensões significativamente menores do que o óxido de cobalto puro. Para a produção convencional de oxigênio, seu desempenho foi comparável ao de alguns catalisadores comerciais à base de metais nobres. Com a adição de ureia, a tensão necessária caiu ainda mais, e com hidrazina a melhoria foi marcante: o eletrodo precisou de apenas um pequeno impulso acima do nível de referência natural para manter a mesma corrente. Em uma célula completa de dois eletrodos emparelhada com um eletrodo padrão à base de platina para produção de hidrogênio, a eletrólise assistida por hidrazina gerou hidrogênio a apenas 0,33 volts — cerca de 1,3 volts a menos do que a divisão tradicional da água nas mesmas condições. O sistema também se mostrou estável por muitas horas, com a estrutura e a composição do catalisador praticamente inalteradas.
O Que Isso Significa para o Hidrogênio Limpo
Para um público não especializado, a conclusão é simples: ao repensar tanto o material do eletrodo quanto a reação que nele ocorre, os pesquisadores demonstraram que o hidrogênio pode ser produzido usando muito menos eletricidade e com ingredientes de baixo custo. Resíduos de frutas tornam-se uma estrutura de carbono de alto desempenho; nanoneedles de óxido de cobalto fornecem sítios ativos; e substituir a formação de oxigênio pela oxidação de ureia ou hidrazina reduz drasticamente a tensão necessária. No caso da hidrazina, os subprodutos são principalmente nitrogênio e água, evitando emissões de carbono adicionais. Embora sejam necessários trabalhos adicionais para gerir o fornecimento químico e a segurança em escala, essa estratégia de eletrólise híbrida aponta para uma produção de hidrogênio mais limpa e barata que também valoriza correntes de resíduos e biomassa renovável.
Citação: Rahamathulla, N., Murthy, A.P. Co3O4 nanoneedles grown on graphene oxide as an efficient electrocatalyst for hybrid water electrolysis through alternative anodic oxidation reactions. Sci Rep 16, 8452 (2026). https://doi.org/10.1038/s41598-026-35522-5
Palavras-chave: produção de hidrogênio, eletrólise da água, óxido de grafeno, oxidação de hidrazina, catalisadores derivados de biomassa