Clear Sky Science · pt
Desenvolvimento apoiado estrutural e computacional de análogos 2,5-disubstituídos de 1,3,4-oxadiazol como inibidores ativos de LOX, urease e α-glucosidase
Novas ferramentas químicas para enfrentar doenças comuns
Muitos problemas de saúde do dia a dia — de úlceras e pedras nos rins a diabetes e inflamação crônica — são impulsionados por enzimas excessivamente ativas em nossos corpos. Este estudo explora uma família de pequenas moléculas recém-projetadas que atuam como freios minúsculos para três dessas enzimas. Ao ajustar suas estruturas e testá-las em laboratório e por meio de simulações computacionais, os pesquisadores buscam criar uma base para medicamentos futuros mais eficazes e seguros. 
Por que essas enzimas importam
A equipe concentrou-se em três alvos enzimáticos que desempenham papéis muito diferentes, porém igualmente importantes, na saúde. A urease ajuda a degradar a uréia; quando se torna hiperativa em certas bactérias ou tecidos, pode contribuir para úlceras gástricas e do trato urinário, pedras nos rins e até aumento da pressão arterial. A alfa-glucosidase fica na superfície das células intestinais e quebra carboidratos complexos em glicose; bloqueá-la é uma forma bem estabelecida de ajudar a controlar a glicemia no diabetes tipo 2. A lipoxigenase (LOX) converte lipídios em moléculas sinalizadoras que promovem inflamação, asma e alguns processos relacionados ao câncer. Assim, há grande interesse em fármacos que atenuem essas enzimas sem prejudicar outros sistemas do organismo.
Construindo uma biblioteca de moléculas candidatas
Para procurar esses fármacos, os pesquisadores sintetizaram uma série de 15 compostos relacionados baseados em um sistema de anel chamado 1,3,4-oxadiazol ligado a uma unidade piperidina. Esse esqueleto químico já aparece em diversos medicamentos modernos e é conhecido por interagir bem com alvos biológicos. A equipe variou as “decorações” ligadas a esse núcleo — pequenos grupos como metil, etil, metoxi, benzil e ciclohexil — em diferentes posições, criando uma pequena biblioteca de candidatos rotulada de 7a a 7o. Cada estrutura foi confirmada usando ferramentas analíticas padrão, como espectroscopia no infravermelho e ressonância magnética nuclear, garantindo que o que foi sintetizado correspondia ao projeto.
Testando a capacidade das moléculas de bloquear enzimas
Cada composto foi então testado contra LOX purificada, urease e alfa-glucosidase para avaliar o quanto podia reduzir a atividade enzimática. Várias moléculas se destacaram. Contra a alfa-glucosidase, os compostos 7a e 7n mostraram-se particularmente eficazes, superando o medicamento padrão para diabetes acarbose nos testes de laboratório ao alcançar altas porcentagens de inibição em baixas concentrações micromolares. Para LOX, os compostos 7a, 7h e 7n exibiram atividade muito forte, em alguns casos melhor do que o inibidor de referência natural quercetina. Nos ensaios de urease, os compostos 7a e especialmente 7l rivalizaram ou ligeiramente superaram o inibidor padrão tiouréia, sugerindo que eles possam um dia servir como candidatos iniciais para terapias anti-úlcera ou anti-pedras. 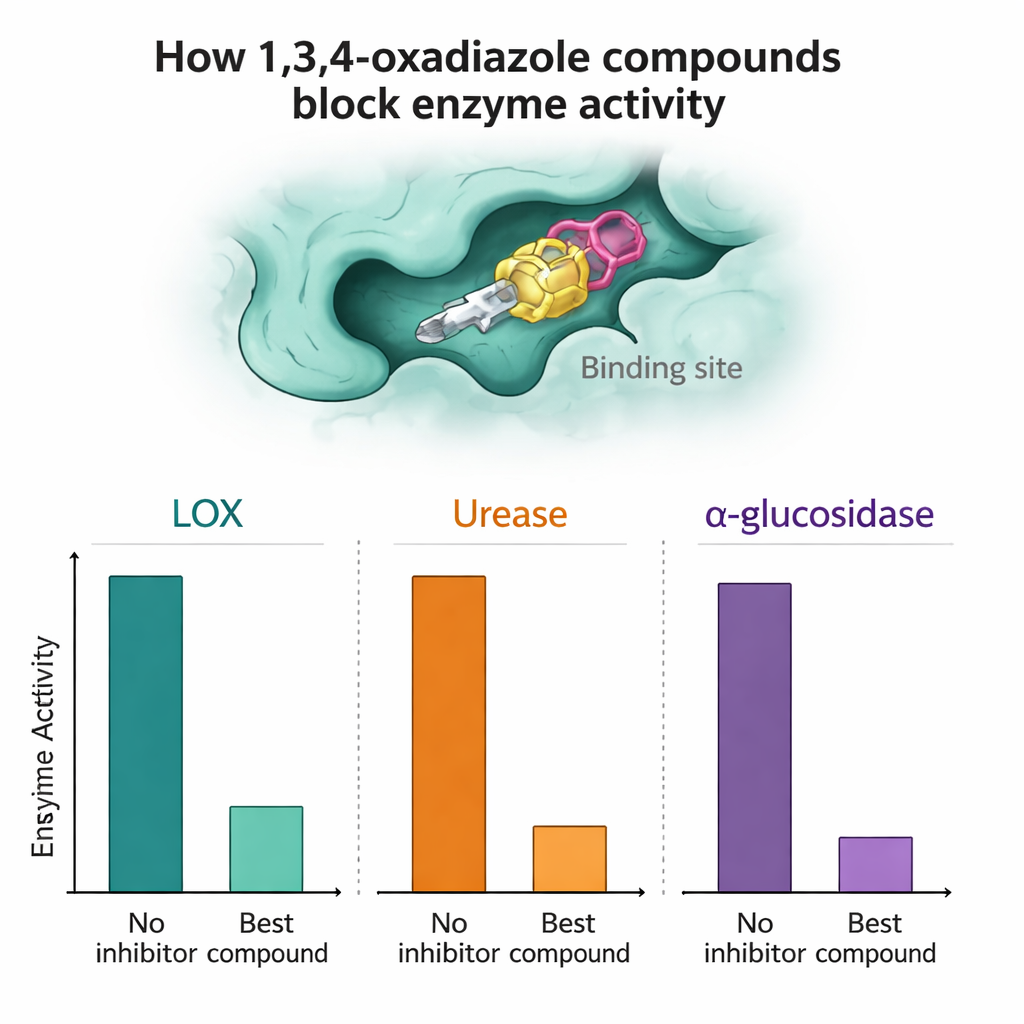
Ligando estrutura ao desempenho
Como as únicas diferenças entre os compostos 7a–7o são pequenas modificações ao redor do sistema de anel central, os pesquisadores puderam começar a traçar relações simples entre estrutura e atividade. Por exemplo, adicionar pequenos grupos ricos em carbono em certas posições “orto” de um anel ligado frequentemente aumentava a capacidade de bloquear a alfa-glucosidase ou a LOX. Outras substituições, como determinados grupos metoxi ou éster colocados em posições menos favoráveis, tenderam a enfraquecer a atividade. Para entender o porquê, a equipe usou simulações computacionais. Cálculos quântico-químicos mostraram que todas as moléculas eram termodinamicamente estáveis e suficientemente flexíveis para se adaptar aos bolsões enzimáticos. Estudos de docking — encaixe virtual de cada molécula em modelos tridimensionais das enzimas — revelaram que os compostos mais ativos faziam contatos mais estreitos por meio de uma combinação de ligações de hidrogênio e interações hidrofóbicas (semelhantes a óleo) em pontos-chave dos sítios ativos, enquanto candidatos mais fracos se encaixavam de forma menos ajustada ou não alcançavam pontos de contato críticos.
O que isso significa para futuros medicamentos
Em termos práticos, o estudo identifica um punhado de “chaves” promissoras que se encaixam bem em três “fechaduras” relacionadas a doenças e começa a explicar, em nível atômico, por que algumas chaves giram melhor que outras. Nenhuma dessas moléculas está pronta para ser um fármaco ainda — elas precisam passar por testes de segurança, otimização do comportamento no organismo e ensaios em animais e humanos. Mas o trabalho mostra que a estrutura 1,3,4-oxadiazol–piperidina é um ponto de partida fértil para tratamentos futuros voltados ao diabetes, condições inflamatórias e distúrbios relacionados à urease. A combinação de medidas laboratoriais cuidadosas com modelagem computacional detalhada fornece um roteiro para afiar esses candidatos rumo a fármacos mais precisos e eficazes.
Citação: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Palavras-chave: inibidores de enzimas, descoberta de fármacos, compostos oxadiazol, diabetes e inflamação, urease e lipoxigenase