Clear Sky Science · pt
SHP2 promove osteossarcoma regulando a sinalização STAT3/TET3/HOXB2
Por que este estudo sobre câncer ósseo importa
O osteossarcoma é o câncer ósseo primário mais comum em crianças e adolescentes e, apesar da quimioterapia moderna e da cirurgia, a sobrevida de pacientes com doença avançada ou recidivada mal melhorou nas últimas décadas. Este estudo investiga a fiação interna das células de osteossarcoma para identificar quais moléculas funcionam como “interruptores mestres” que ajudam os tumores a crescer, se espalhar e resistir ao tratamento. Ao revelar uma via de controle centralizada em uma proteína chamada SHP2, o trabalho aponta para novos alvos farmacológicos que podem, no futuro, tornar as terapias do osteossarcoma mais eficazes e precisas.
Seguindo as pistas na atividade gênica tumoral
Os pesquisadores começaram tratando o osteossarcoma como um problema de dados. Eles mineraram conjuntos públicos de expressão gênica comparando amostras tumorais com tecido ósseo normal e usaram ferramentas estatísticas para identificar genes que eram consistentemente ativados ou silenciados no câncer. Centenas de genes mostraram diferenças, muitos deles agrupados em vias cancerígenas bem conhecidas que impulsionam crescimento, sobrevivência e mobilidade celular. Entre esses, uma proteína, SHP2, destacou‑se como um hub fortemente ligado a várias outras: o fator de sinalização STAT3, a enzima modificadora de DNA TET3 e o regulador do desenvolvimento HOXB2. Isso sugeriu que essas moléculas poderiam formar uma cadeia conectada que ajuda as células de osteossarcoma a se comportarem de forma agressiva. 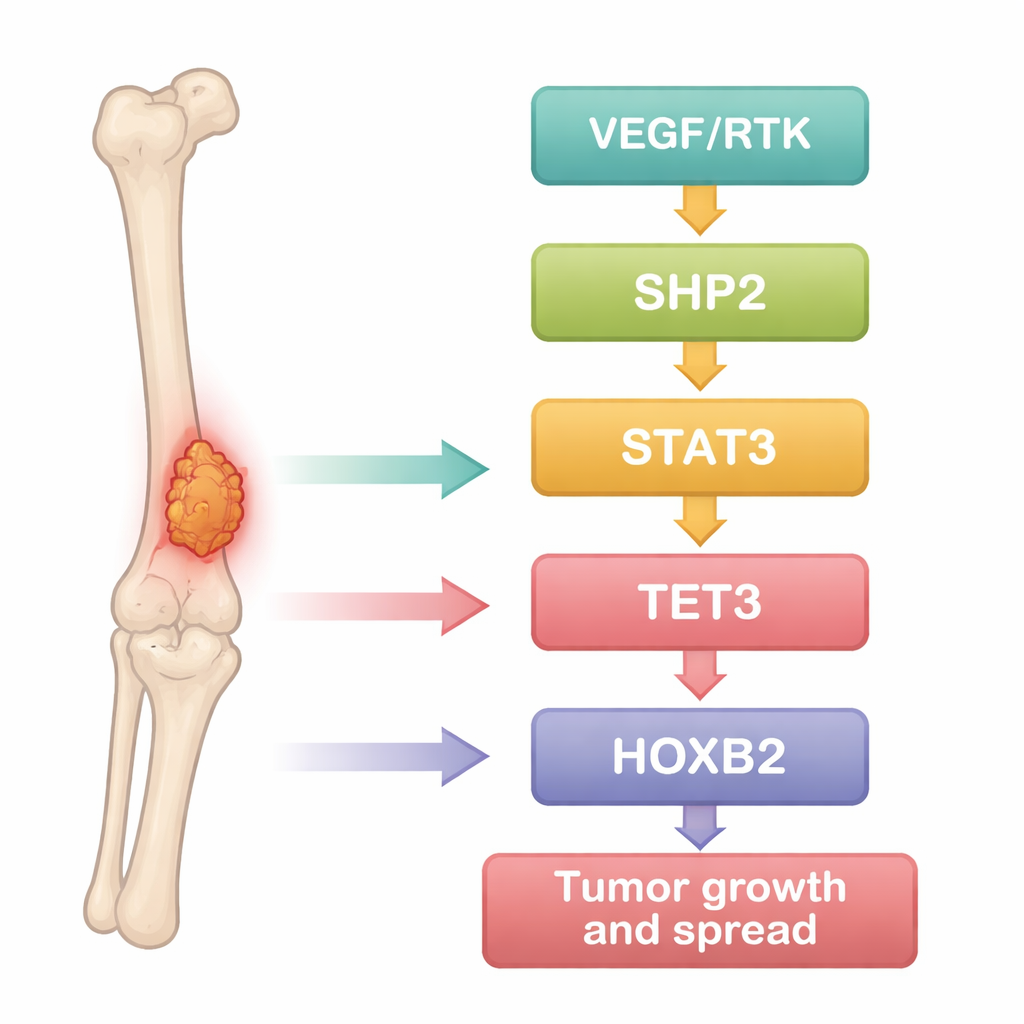
Testando o papel do SHP2 em células cancerosas
Para ir além das correlações, a equipe modificou linhagens humanas de osteossarcoma (143B e MG63) para reduzir ou aumentar a expressão de SHP2. Quando reduziram o SHP2, a capacidade das células de se multiplicar, migrar sobre uma superfície e invadir através de uma membrana diminuiu de modo perceptível. Os níveis das proteínas STAT3, TET3 e HOXB2, bem como marcadores ligados ao câncer como c‑Myc, NANOG e NUSAP1, também caíram. Quando reativaram STAT3 ou sobreexpressaram HOXB2, muitos desses efeitos foram revertidos, indicando que o SHP2 atua a montante de uma cadeia que, em última instância, alimenta genes que controlam divisão celular, características semelhantes a células‑tronco e a maquinaria da mitose.
Construindo uma via cancerígena passo a passo
Ao juntar os experimentos, os autores descrevem um modelo em etapas. No microambiente tumoral, altos níveis do fator de crescimento endotelial vascular (VEGF) estimulam tirosina‑quinases receptoras (RTKs) na superfície celular. Estas, por sua vez, ativam o SHP2 no interior da célula. O SHP2 ativo liga o STAT3, um fator de transcrição que se desloca ao núcleo e ajuda a aumentar a produção de TET3. O TET3 então edita as marcas químicas no DNA, removendo especificamente grupos metil da região do gene HOXB2. Essa desmetilação age como soltar um freio, permitindo que o HOXB2 seja mais fortemente expresso. HOXB2, um gene que normalmente orienta o desenvolvimento, passa a impulsionar a atividade de c‑Myc, NANOG e NUSAP1, que em conjunto alimentam o crescimento incessante das células tumorais, aumentam o comportamento invasivo e sustentam traços associados à metástase.
Do prato de cultura aos animais vivos
Para verificar se essa via era relevante em tumores inteiros, os cientistas implantaram células de osteossarcoma modificadas sob a pele de camundongos. Tumores formados por células que superexpressavam SHP2 cresceram maiores e mais pesados que os controles. Quando TET3 foi silenciado nessas células ricas em SHP2, o crescimento tumoral desacelerou e os níveis de HOXB2 caíram, mesmo com SHP2 e STAT3 permanecendo ativos. A reintrodução de HOXB2 restaurou o vigor do tumor. Ao longo do estudo, as medidas dos níveis proteicos no tecido tumoral espelharam os achados anteriores em cultura celular, fortalecendo a ideia de que SHP2, STAT3, TET3 e HOXB2 atuam como um eixo conectado que impulsiona o osteossarcoma para um comportamento mais maligno. 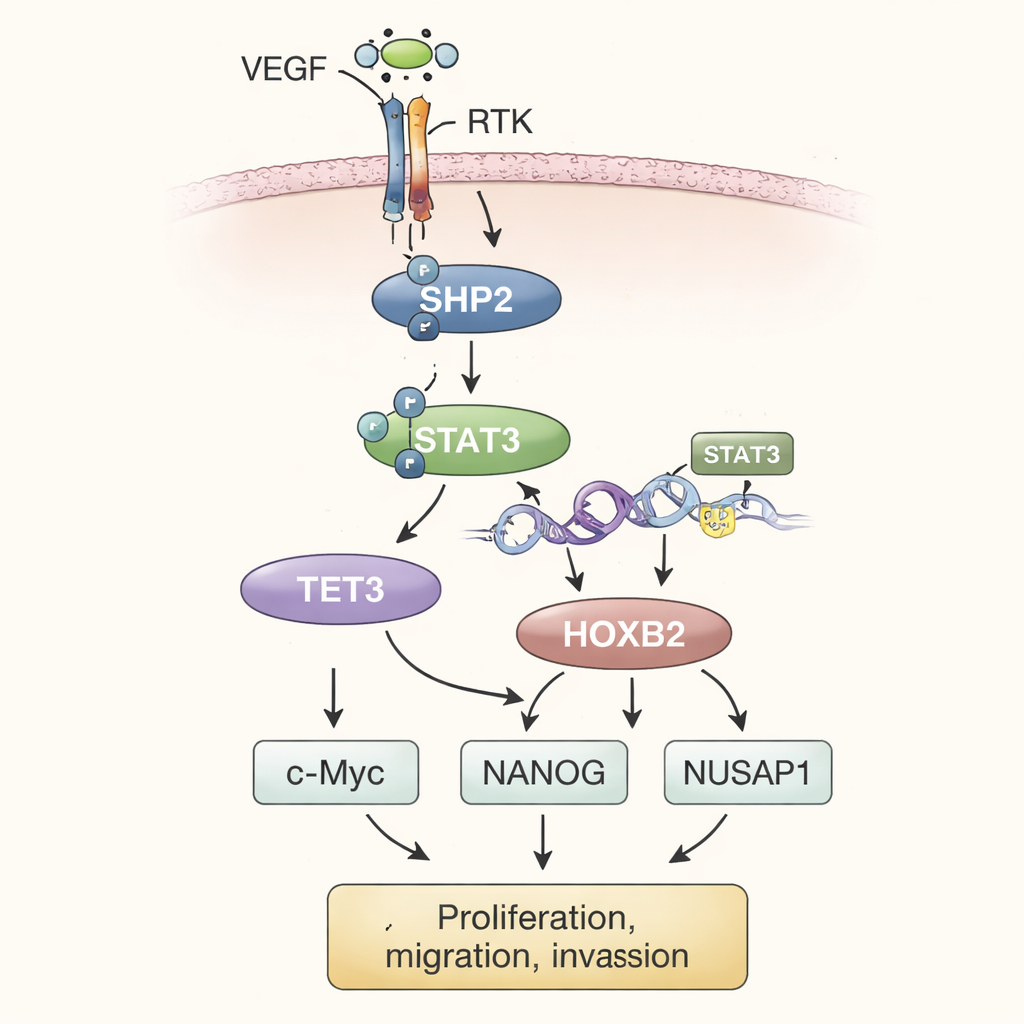
O que isso significa para tratamentos futuros
Para um leitor leigo, a mensagem principal é que os pesquisadores traçaram uma cadeia de sinal clara — desde o VEGF e seus receptores de superfície, passando por SHP2 e STAT3, até TET3, HOXB2 e vários genes potentes de crescimento — que ajuda a explicar por que o osteossarcoma pode crescer rapidamente e se espalhar cedo. Como SHP2 e STAT3 são enzimas que, em princípio, podem ser bloqueadas por pequenas moléculas, e TET3 e HOXB2 marcam passos posteriores na mesma rota, essa via oferece múltiplos pontos onde terapias futuras poderiam intervir. Embora o estudo tenha sido conduzido em linhagens celulares e em camundongos, fornece um mapa detalhado que desenvolvedores de medicamentos podem usar para projetar tratamentos combinados visando desligar os interruptores centrais do tumor em vez de apenas atacar seus efeitos finais.
Citação: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Palavras-chave: osteossarcoma, SHP2, via STAT3, sinalização tumoral, terapia direcionada