Clear Sky Science · pt
Desenvolvimento de um sistema global de triagem para detectar interações proteína–proteína por complementação de luminescência em levedura fission
Iluminando a Vida Oculta das Proteínas
Cada batida do coração, pensamento e respiração em nossos corpos depende de proteínas que se juntam dentro das células. Essas pequenas parcerias, chamadas interações proteína–proteína, controlam tudo, desde a leitura dos genes até a resposta das células ao estresse. Ainda assim, muitas dessas associações são fugazes ou delicadas, o que as torna difíceis de detectar com as ferramentas atuais. Este estudo descreve um novo sistema de triagem altamente sensível, baseado em luz, construído em um organismo modelo simples — a levedura fission — para revelar simultaneamente milhares dessas conexões proteicas ocultas.
Por Que as Parcerias de Proteínas São Tão Difíceis de Ver
Proteínas raramente atuam sozinhas. Elas se ligam a parceiros diferentes em momentos diferentes, às vezes apenas por instantes, e seu comportamento pode ser alterado por modificações químicas ou por sua localização na célula. Métodos tradicionais para estudar essas interações ou removem as proteínas de seu ambiente natural, ou dependem de artifícios genéticos que não capturam todos os pareamentos. Como resultado, os mapas existentes de quem interage com quem na célula são incompletos. Os autores buscaram melhorar esse panorama criando um sistema mais flexível e sensível, capaz de sondar quase todas as proteínas da levedura fission em células vivas.
Convertendo Toque em Luz
No cerne da nova abordagem está uma enzima dividida que emite luz. Uma parte, chamada LgBiT, é ligada a uma proteína "iscas" que os pesquisadores desejam estudar. A outra parte, SmBiT, é ligada a muitos possíveis parceiros "presas", um por linhagem de levedura. Sozinhos, esses dois fragmentos de enzima praticamente não interagem. Mas quando a proteína isca e a presa se ligam dentro da célula, os dois fragmentos se juntam novamente, reconstituindo uma enzima funcional que brilha na presença de um combustível químico. Medindo quanto cada linhagem de levedura emite de luz, a equipe pode identificar quais proteínas realmente se encontram dentro da célula e quão forte é a interação. Para evitar perder parceiros porque a etiqueta bloqueia a função normal, a proteína isca é feita em duas versões, com LgBiT preso a cada extremidade, aumentando consideravelmente as chances de que pelo menos uma orientação funcione. 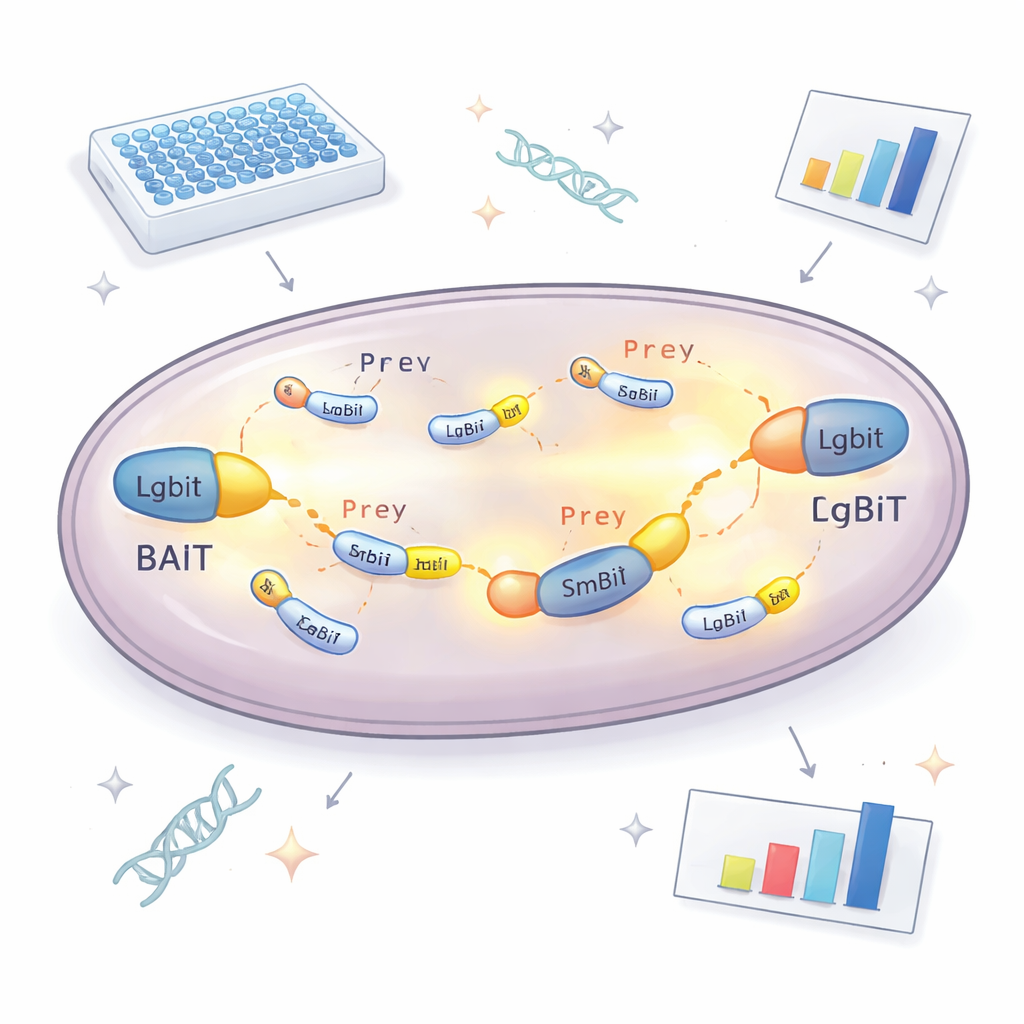
Projetando uma Biblioteca de Levedura e um Sistema de Cepas
Construir essa plataforma exigiu mais do que uma enzima engenhosa. Os pesquisadores também precisaram introduzir milhares de proteínas presa na levedura de maneira controlada e em cópia única. Eles projetaram um vetor de DNA especial para as proteínas presa que se insere em um ponto definido do genoma da levedura e carrega um marcador fluorescente vermelho. O brilho desse sinal vermelho reflete quantas cópias foram inseridas, permitindo que a equipe selecione facilmente colônias com exatamente uma cópia, o que é essencial para comparações confiáveis. Também criaram vetores dedicados para a isca que posicionam o LgBiT no início ou no fim da proteína isca, separados por elos flexíveis para que a proteína ainda possa se dobrar e se mover normalmente. Cepas de levedura cuidadosamente engenheiradas foram então construídas para hospedar duas construções de isca e uma de presa ao mesmo tempo, usando marcadores nutricionais para garantir que apenas células corretamente combinadas sobrevivam.
Colocando o Sistema à Prova
Para verificar se o desenho realmente melhorou a detecção, os cientistas primeiro examinaram proteínas com parceiros bem conhecidos. Confirmaram que a intensidade do sinal dependia fortemente de onde a etiqueta emissora de luz estava anexada: algumas interações só apareciam quando o LgBiT estava em uma extremidade da isca, e não na outra. Expressar ambas as versões juntas aumentou a emissão de luz, provando que a estratégia de isca dupla facilita a captura de interações fracas ou sensíveis à orientação. O sistema também detectou contatos envolvendo proteínas de membrana, uma classe notoriamente difícil para métodos tradicionais de two-hybrid em levedura. Com essa validação, a equipe escalou para uma triagem em escala genômica, usando uma proteína relacionada à transcrição chamada Tfs1 como isca. Triando mais de 4.600 proteínas presa, encontraram 31 candidatos fortes, incluindo vários parceiros já conhecidos e muitos novos, alguns localizados fora do núcleo em áreas como mitocôndrias e superfície celular. 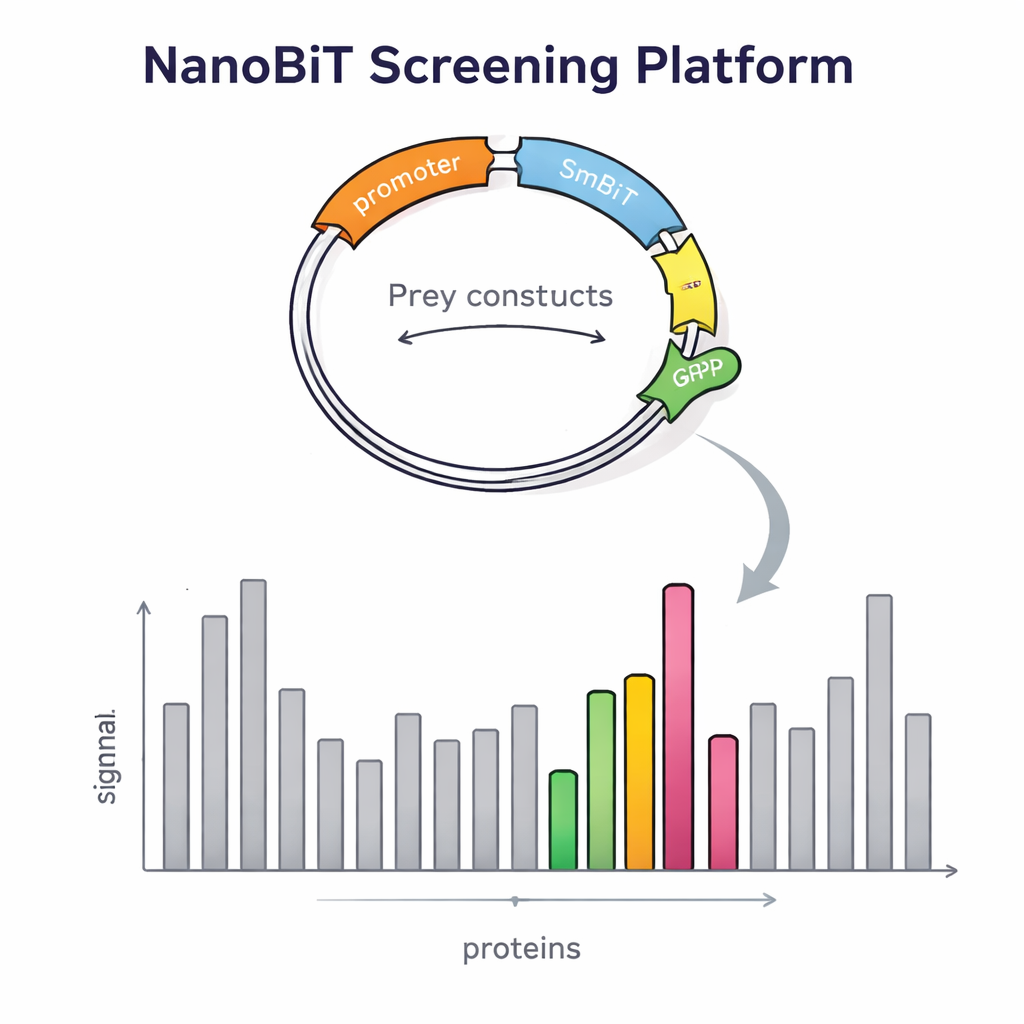
O Que Isso Significa para a Biologia e a Descoberta de Fármacos
Para um não especialista, a mensagem principal é que os autores construíram um "radar de interações" mais sensível dentro de células de levedura. Ao converter apertos de mão proteicos breves em flashes mensuráveis de luz, e ao organizar inteligentemente a genética para que três proteínas etiquetadas possam ser expressas juntas, seu sistema revela parceiros proteicos conhecidos e anteriormente invisíveis. Embora sejam necessários checagens adicionais com outras técnicas para confirmar cada novo pareamento, essa plataforma preenche lacunas importantes em nossos mapas de redes celulares. Como as linhagens também foram projetadas para serem mais sensíveis a pequenas moléculas, o mesmo sistema pode ser adaptado para buscar fármacos que interrompam parcerias proteicas prejudiciais ou estabilizem as benéficas, oferecendo uma nova ferramenta poderosa tanto para a biologia básica quanto para a descoberta de fármacos em estágio inicial.
Citação: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Palavras-chave: interações de proteínas, levedura fission, ensaio de luminescência, triagem de alto rendimento, ferramentas para descoberta de fármacos