Clear Sky Science · pt
Secretoma dependente da partícula de reconhecimento de sinal em humanos
Como as Células Decidem Quais Proteínas Saem da Célula
Nossas células constantemente exportam proteínas que formam hormônios, anticorpos e a matriz entre os tecidos. Mas nem toda proteína está destinada a viajar. Este estudo investiga uma pergunta básica, ainda sem resposta completa: como as células humanas decidem quais proteínas dependem de um ajudante-chave chamado partícula de reconhecimento de sinal (SRP) para alcançar o centro interno de embarque da célula, e quais podem chegar lá sem ela? Ao mapear essa decisão em milhares de proteínas ao mesmo tempo, os autores revelam quem depende da SRP, quem não depende, e o que acontece quando esse sistema falha — um tema relevante para muitas doenças associadas a proteínas secretadas mal direcionadas ou ausentes.
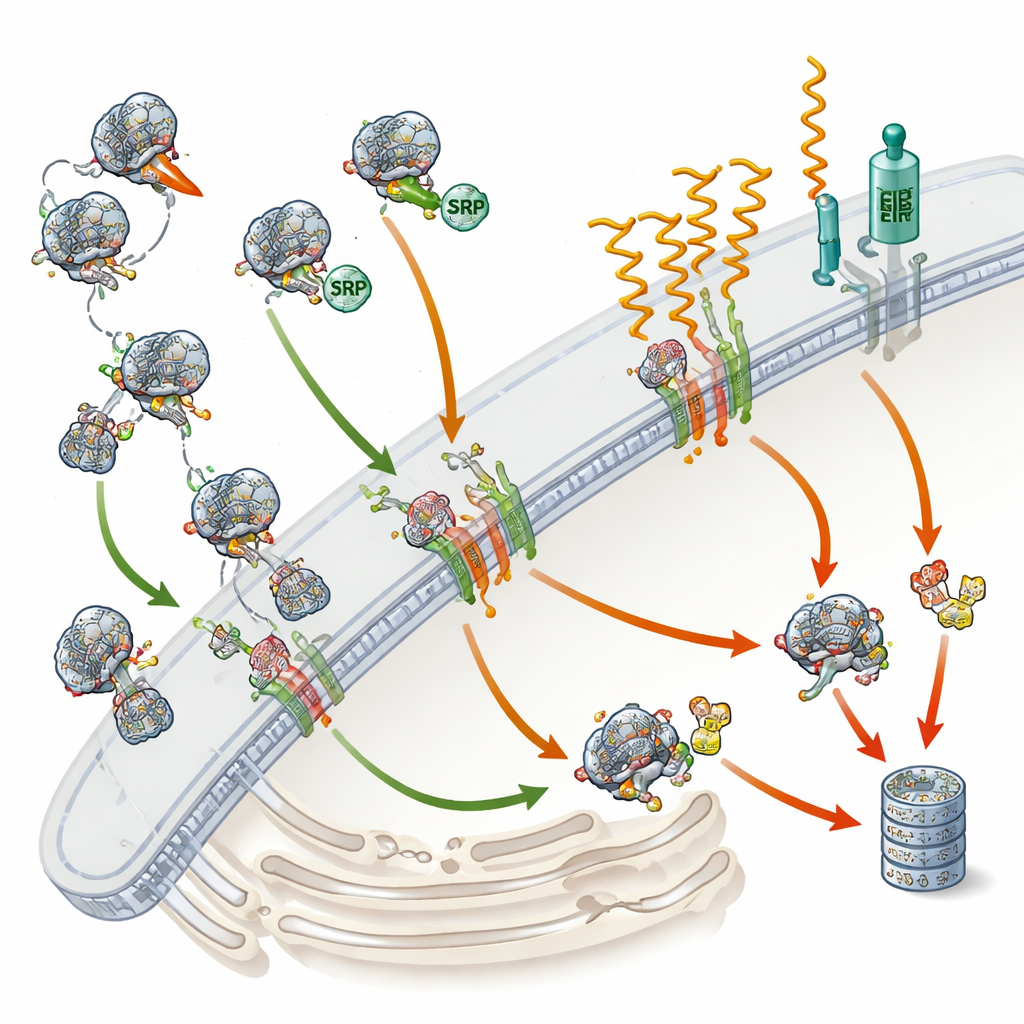
O Cais de Embarque da Célula e Seu Guia Principal
Roughly one out of every three human proteins is destined either for the cell surface, cellular membranes, or for release outside the cell. Para alcançar o lugar certo, a maioria dessas proteínas deve primeiro entrar em uma rede de membranas internas chamada retículo endoplasmático, o cais de embarque da célula. A SRP atua como um guia: ela reconhece uma pequena “etiqueta de endereço” no início das proteínas recém-sintetizadas e pausa temporariamente sua produção. Essa pausa dá tempo ao ribossomo — a máquina que fabrica proteínas — para ancorar no retículo endoplasmático, onde a produção é retomada e a proteína em crescimento é inserida na membrana ou atravessa-na. Algumas proteínas, entretanto, usam rotas alternativas que não exigem SRP, especialmente proteínas muito pequenas ou aquelas ancoradas pelas suas extremidades finais. Até agora, os cientistas não sabiam, em escala global, quais proteínas humanas realmente requerem a SRP e quais podem contorná-la.
Reduzindo a SRP para Ver o que Se Rompe
Para responder a isso, os pesquisadores reduziram seletivamente os níveis de um componente essencial da SRP, o SRP54, em células HeLa humanas. Em seguida, usaram uma técnica sensível chamada espectrometria de massas para medir mais de 6.000 proteínas dentro das células e quase 2.000 proteínas presentes no líquido circundante, conhecido como meio condicionado. Comparar células com SRP54 normal com aquelas com SRP54 reduzida permitiu ver quais proteínas ficaram menos abundantes, quais aumentaram e quais permaneceram inalteradas. Uma queda acentuada no nível de uma proteína — especialmente tanto dentro da célula quanto no meio — foi interpretada como sinal de que essa proteína depende da SRP para ser sintetizada e encaminhada corretamente.
Quem Depende da SRP e Quem se Vira sem Ela
A análise mostrou que a maioria das proteínas normalmente secretadas para o meio depende claramente da SRP. Quando o SRP54 foi reduzido, a maioria dessas proteínas secretadas, particularmente aquelas que carregam uma clássica etiqueta de sinal “endereço”, caiu acentuadamente. Muitas proteínas de membrana dentro da célula também diminuíram, revelando-as como clientes da SRP. Um conjunto menor de proteínas com etiquetas de endereço semelhantes foi amplamente não afetado, marcando-as como independentes da SRP; essas provavelmente usam rotas alternativas para alcançar o retículo endoplasmático. Os pesquisadores também descobriram que características específicas da etiqueta de endereço — como uma região carregada positivamente em seu início — eram mais comuns entre proteínas dependentes da SRP, sugerindo regras sutis que ajudam a SRP a escolher sua carga. Ao mesmo tempo, algumas proteínas envolvidas em marcar proteínas danificadas para destruição e na função mitocondrial aumentaram, sugerindo que as células ativam sistemas de backup e a produção de energia quando seu guia principal de embarque é comprometido.
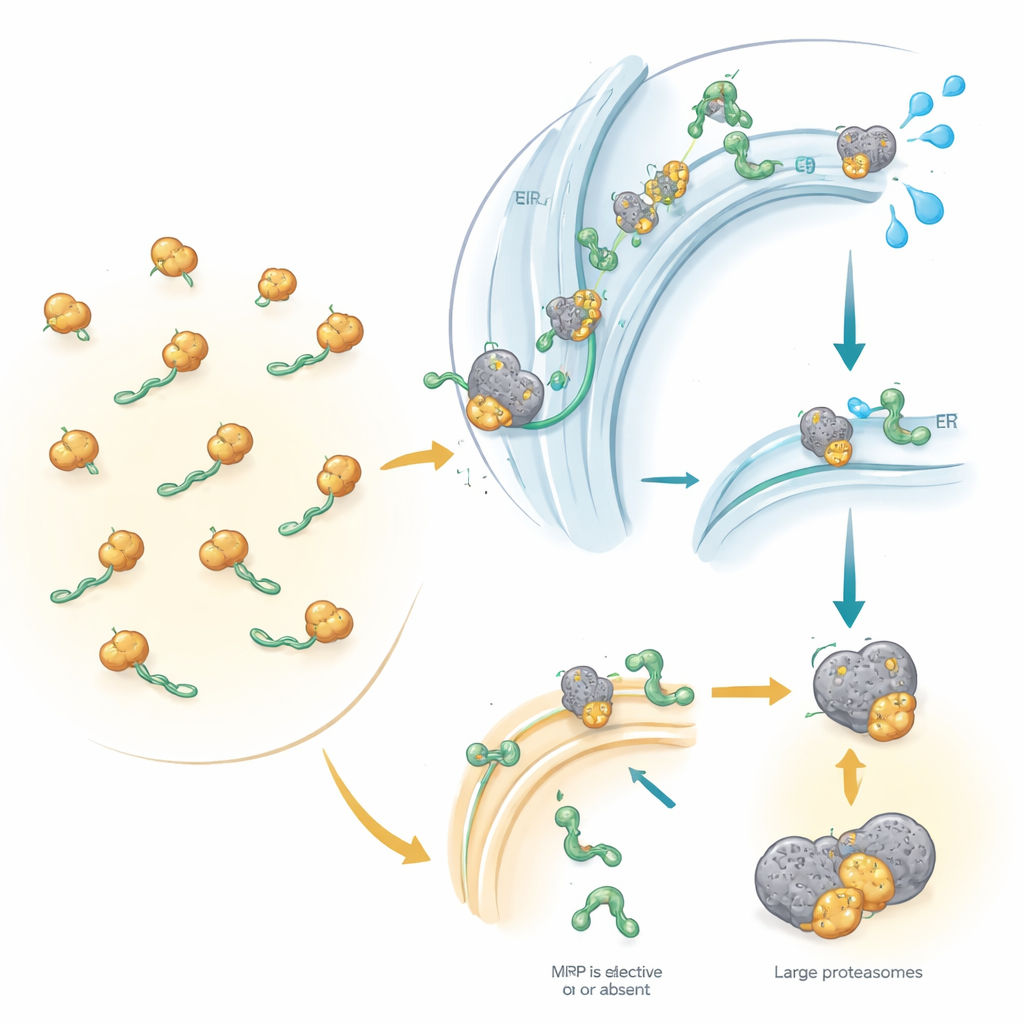
Controle de Qualidade Quando o Alvo Dá Errado
O estudo foi além da contagem de proteínas: comparou essas mudanças com variações no RNA mensageiro, as plantas usadas para fabricar proteínas. Muitas proteínas dependentes da SRP perderam não apenas a proteína, mas também seus moldes de RNA, implicando uma via de controle de qualidade conhecida como RAPP. Quando a SRP não consegue engajar adequadamente uma proteína secretora ou de membrana em formação, essa via parece desencadear a degradação do RNA correspondente, impedindo a produção continuada de uma proteína mal direcionada. Ao mesmo tempo, proteínas incompletas que não alcançam o retículo endoplasmático provavelmente são marcadas com pequenas bandeiras moleculares e enviadas aos “trituradores” celulares chamados proteassomos. Curiosamente, vias clássicas de estresse no retículo endoplasmático não foram fortemente ativadas, sugerindo que a deficiência de SRP provoca um tipo distinto de resposta ao estresse celular.
O Que Isso Significa para a Saúde e a Doença
Ao mapear, pela primeira vez em células humanas, quais proteínas secretadas e de membrana são dependentes ou independentes da SRP, este trabalho fornece um mapa de referência das regras de embarque da célula. Os achados mostram que a maioria das proteínas exportadas realmente depende da SRP e que, quando a SRP falha, as células respondem degradando tanto as proteínas quanto seus moldes enquanto acionam mecanismos alternativos de enfrentamento. Como muitas mutações causadoras de doenças afetam as etiquetas de sinal nas proteínas secretadas, entender exatamente como a SRP reconhece seus clientes e como a RAPP remove as versões defeituosas pode ajudar a explicar por que certas mutações levam a deficiências hormonais, problemas imunológicos ou neurodegeneração — e pode, eventualmente, apontar para novas formas de ajustar o encaminhamento de proteínas na saúde humana.
Citação: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Palavras-chave: secreção de proteínas, partícula de reconhecimento de sinal, secretoma, controle de qualidade de proteínas, retículo endoplasmático