Clear Sky Science · pt
Inibição sequencial de platina e PARP aumenta a eficácia da imunoterapia anti‑PD1 em câncer pancreático murino com mutação em Brca2
Por que esta pesquisa importa para os pacientes
O câncer de pâncreas é um dos mais letais e, mesmo quando os médicos identificam uma vulnerabilidade útil no tumor — como uma mutação no gene BRCA2 — os tratamentos atuais raramente mantêm a doença sob controle por muito tempo. Este estudo usa um modelo de camundongo realista para fazer uma pergunta prática que muitos pacientes e oncologistas enfrentam hoje: após uma quimioterapia intensa seguida de um inibidor de PARP, adicionar imunoterapia moderna pode ampliar de forma significativa a sobrevida, e por que os tumores reaparecem com tanta frequência?
Um câncer resistente com um ponto fraco genético
O adenocarcinoma ductal pancreático é notoriamente difícil de tratar, com sobrevivência em cinco anos ainda na casa dos dígitos únicos. Uma pequena fração de pacientes apresenta defeitos herdados ou específicos do tumor em BRCA2, um gene necessário para reparar DNA quebrado. Esses tumores são incomumente sensíveis a drogas que danificam o DNA, como quimioterapia à base de platina, e a inibidores de PARP, que prejudicam ainda mais a capacidade das células cancerosas de reparar DNA. O cuidado padrão atual para câncer pancreático avançado com mutação em BRCA é meses de quimioterapia à base de platina seguidos por tratamento de manutenção com um inibidor de PARP. Ainda assim, no principal ensaio clínico POLO, essa estratégia não prolongou a sobrevida global, destacando a necessidade de entender a resistência e desenvolver melhores abordagens de manutenção.
Construindo um modelo de camundongo mais realista
Muitos modelos laboratoriais existentes removem os componentes imunes e estromais que rodeiam tumores reais em pacientes. Para superar isso, os autores desenvolveram camundongos que desenvolvem tumores pancreáticos deficientes em BRCA2 em um contexto de sistema imune totalmente funcional. A partir desses tumores espontâneos, derivaram linhas celulares clonais que puderam ser implantadas em camundongos geneticamente compatíveis. Esses tumores mutantes de Brca2 se assemelhavam e se comportavam muito como cânceres pancreáticos humanos: eram densamente fibróticos, excluíam em grande parte células T e apresentavam altos níveis de dano de DNA espontâneo. Crucialmente, os tumores foram altamente sensíveis a uma combinação comum com platina (gemcitabina mais cisplatina), enquanto o tratamento com inibidor de PARP isolado teve efeitos modestos e de curta duração nos animais, apesar da forte atividade contra as mesmas células em cultura. 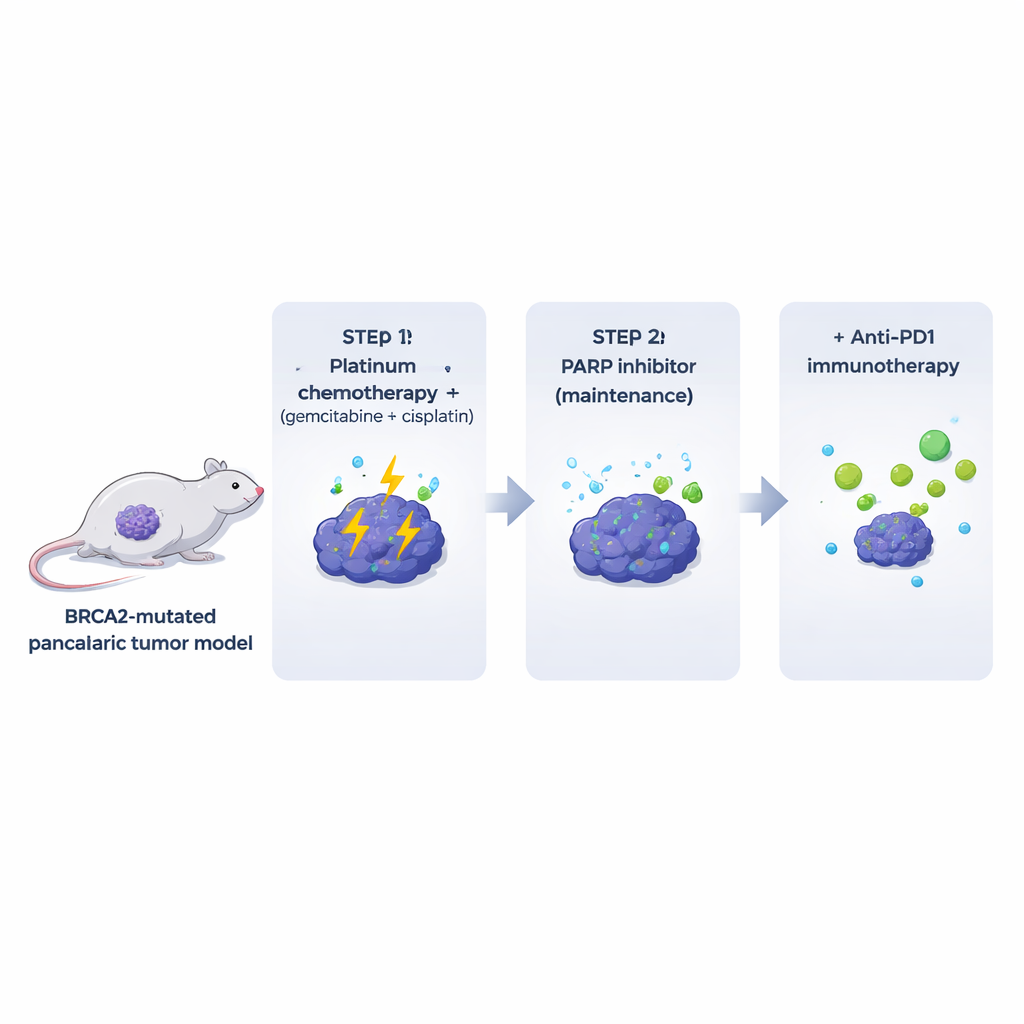
A quimioterapia remodela a vizinhança do tumor
A equipe então investigou o que ocorre dentro do tumor após a quimioterapia com platina. Dez dias após o tratamento, os tumores haviam encolhido, mas não foram erradicados. Análises de expressão gênica revelaram uma mudança marcante em direção a atividades relacionadas ao sistema imune: vias associadas à ativação de células T e à imunidade adaptativa foram ativadas. Mais células T foram encontradas dentro dos tumores tratados, e muitas dessas células T exibiam marcadores de exaustão — sinais de que foram ativadas, mas estavam se tornando ineficazes. Padrões semelhantes de aumento da presença de células T foram observados em cânceres pancreáticos humanos com mutações em BRCA ou no gene relacionado PALB2 após pacientes receberem quimioterapia à base de platina antes da cirurgia. Ao mesmo tempo, as células tumorais aumentaram os níveis de PD‑L1, uma proteína de superfície que pode desligar as células T ao engajar o receptor PD‑1, sugerindo que os tumores estavam se defendendo dessa nova pressão imune.
Por que PARP sozinho não é suficiente — e onde surge a resistência
Espelhando o cuidado clínico, os pesquisadores administraram aos camundongos um ciclo inicial de gemcitabina e cisplatina, seguido de manutenção com o inibidor de PARP olaparibe. Essa sequência melhorou o controle tumoral e a sobrevida em comparação com a quimioterapia isolada, confirmando que a quimioterapia prévia pode tornar os tumores mais suscetíveis à inibição de PARP. No entanto, nenhum camundongo foi curado: os tumores eventualmente cresceram novamente sob manutenção com PARP. Tumores resistentes exibiram aparência mais diferenciada e níveis fortemente aumentados do regulador de desenvolvimento CDX2. Isso sugere que, ao menos neste modelo, a resistência não surge simplesmente por consertar o defeito original na reparação do DNA, mas pode envolver uma alteração na identidade celular do tumor. CDX2 poderia potencialmente servir como biomarcador de resistência emergente em pacientes.
Desbloqueando a imunoterapia com a sequência correta
Drogas que bloqueiam pontos de controle imune, como anticorpos anti‑PD1, transformaram o tratamento de vários cânceres, mas o câncer pancreático permaneceu amplamente pouco responsivo. Em consonância com isso, anti‑PD1 (com ou sem outro bloqueador de checkpoint, anti‑CTLA4) não ajudou quando administrado a tumores mutantes de BRCA2 sem tratamento prévio, e também teve pouco efeito quando simplesmente adicionado à terapia com inibidor de PARP. A situação mudou quando a sequência completa foi usada: quimioterapia com platina primeiro, seguida de manutenção com inibidor de PARP mais anti‑PD1. Nesse contexto, os tumores encolheram mais profundamente e os camundongos viveram mais do que com quimioterapia seguida de PARP ou anti‑PD1 isoladamente. A adição de anti‑CTLA4 à manutenção com PARP não produziu benefícios semelhantes, sugerindo que o ambiente tumoral primado pela quimioterapia está especificamente preparado para responder ao bloqueio de PD‑1. 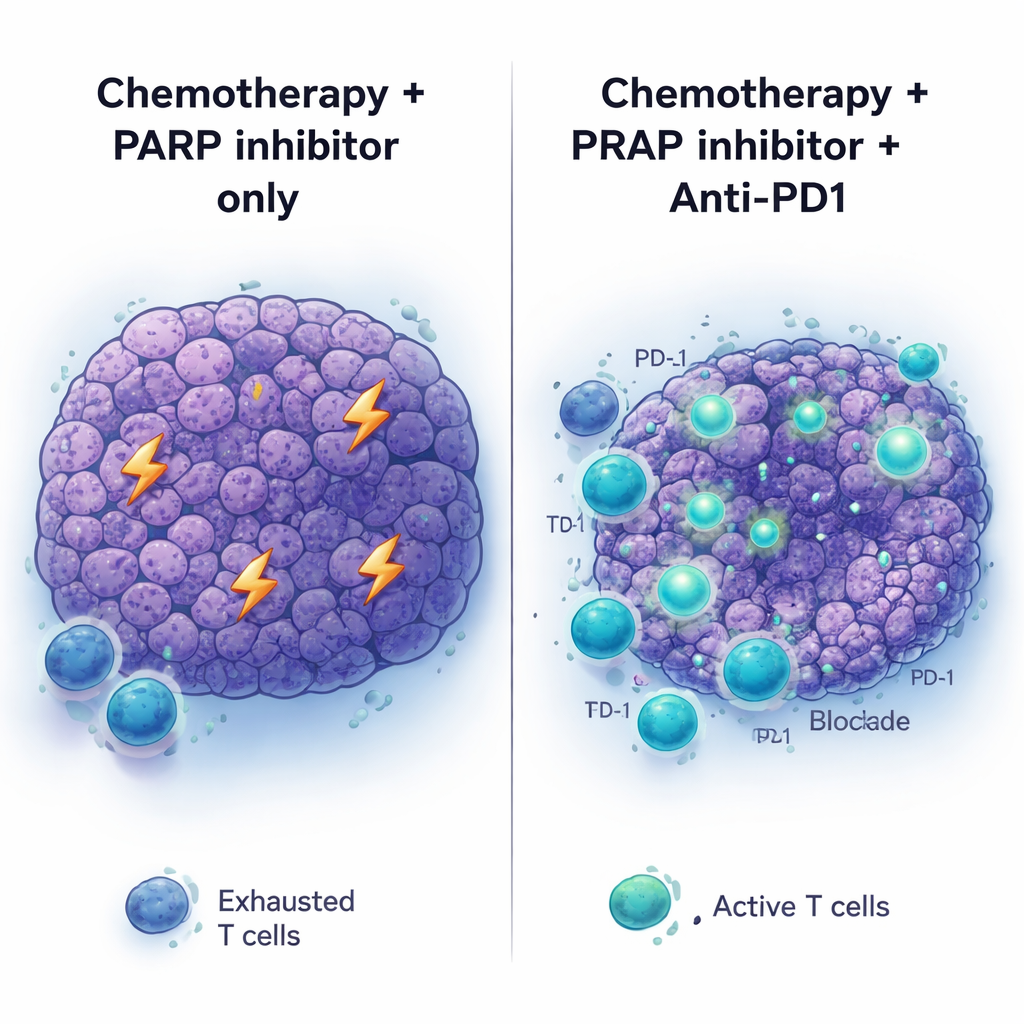
O que isso pode significar para cuidados futuros
Em conjunto, o estudo indica que, para câncer pancreático com mutação em BRCA, a ordem e a combinação das terapias importam muito. A quimioterapia fortemente danificadora do DNA não apenas ataca as células tumorais diretamente, mas também desencadeia uma resposta imune, mesmo que essa resposta seja inicialmente atenuada pela exaustão e pelas defesas via PD‑L1. Inibidores de PARP podem prolongar o benefício, mas é improvável que sejam curativos por si só e podem direcionar os tumores para um estado resistente com altos níveis de CDX2. Ao adicionar imunoterapia anti‑PD1 à manutenção com PARP após quimioterapia com platina, pode ser possível converter esse quadro imune brevemente inflamado e exaurido em um ataque antitumoral mais eficaz e duradouro. Ensaios clínicos em curso que combinam inibidores de PARP com imunoterapia em câncer pancreático relacionado a BRCA serão fundamentais para determinar se essa estratégia cuidadosamente temporizada pode se traduzir em vidas mais longas e com melhor qualidade para os pacientes.
Citação: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Palavras-chave: câncer pancreático, mutação BRCA2, quimioterapia com platina, inibidor de PARP, imunoterapia anti‑PD‑1