Clear Sky Science · pt
Síntese eficiente de amidas sem solvente via reação de Ritter catalisada por um nanocompósito reutilizável Fe3O4/g-C3N4/NTMPA
Por que uma química mais limpa importa
Muitos dos medicamentos que tomamos, os plásticos ao nosso redor e até fibras de alto desempenho são construídos a partir de um tipo simples de ligação química chamada ligação amida. Produzir essas ligações em escala industrial geralmente exige ácidos fortes e corrosivos e grandes volumes de solvente, o que gera resíduos e problemas de segurança. Este artigo descreve um novo catalisador sólido responsivo a campos magnéticos que pode formar amidas em alto rendimento sem uso de solvente, apontando para uma fabricação de drogas e materiais mais segura e sustentável.
Uma ligação essencial em fármacos e materiais
As amidas são as ligações que mantêm proteínas unidas e também aparecem em inúmeros produtos farmacêuticos, agroquímicos e polímeros como o náilon. Os químicos dispõem de várias maneiras de formar ligações amida, mas a maioria dos métodos exige materiais iniciais pré‑ativados ou condições severas. A reação de Ritter se destaca porque une diretamente um álcool (ou alceno) simples a um nitrilo em uma etapa. No entanto, em sua forma clássica, a reação de Ritter depende de ácidos minerais concentrados como ácido sulfúrico ou clorídrico. Esses ácidos líquidos são corrosivos, difíceis de separar dos produtos e complicados de reciclar, tornando‑os pouco adequados à química verde.
Um pequeno ímã que você pode agitar
Os pesquisadores projetaram um catalisador sólido e separável por campo magnético que poderia substituir esses ácidos líquidos. O material combina três componentes: nanopartículas de óxido de ferro (Fe3O4), que conferem propriedades magnéticas; um sólido em camadas rico em carbono e nitrogênio (nitreto de carbono grafítico, g‑C3N4), que atua como suporte protetor; e uma molécula fortemente ácida chamada nitrilotri(metilenfosfonato) (NTMPA), que fornece a acidez necessária para a reação. Essas partes são montadas de modo que o NTMPA fique ancorado na superfície do g‑C3N4, enquanto pequenas partículas de Fe3O4 estão distribuídas ao longo do compósito. Como todo o compósito responde a um ímã, ele pode ser retirado da mistura reacional simplesmente aproximando um ímã do frasco.
Comprovando a estrutura do catalisador
Para confirmar que construíram o que pretendiam, os autores usaram um conjunto de técnicas de ciência dos materiais. Espectroscopia de infravermelho mostrou sinais dos grupos fosfônicos, da estrutura carbono‑nitrogênio e das ligações ferro–oxigênio, todos presentes no compósito final. Difração de raios X indicou que o óxido de ferro magnético manteve sua forma cristalina, enquanto o nitreto de carbono permaneceu como um sólido em camadas, relativamente desordenado. Microscopia eletrônica revelou partículas em formato de folha adornadas com esferas uniformemente dispersas na faixa de 10–20 nanômetros, e mapeamento elemental mostrou ferro, carbono, nitrogênio, oxigênio e fósforo distribuídos de maneira uniforme. Medições de área superficial e tamanho de poros confirmaram uma estrutura mesoporosa — cheia de canais em escala nanométrica que permitem que os reagentes alcancem os sítios ativos — enquanto análise térmica mostrou que o material permanece estável até várias centenas de graus Celsius.
Reações rápidas e sem solvente
Com a estrutura estabelecida, a equipe testou o catalisador na reação de Ritter entre vários álcoois e nitrilos. Eles descobriram que as melhores condições eram surpreendentemente simples: quantidades iguais de álcool e nitrilo, uma pequena quantidade do catalisador sólido, aquecimento a 80 °C e nenhum solvente adicionado. Nessas condições, muitos materiais iniciais diferentes foram convertidos em suas respectivas amidas com rendimentos altos a excelentes, frequentemente acima de 90%. Álcoois terciários e benzílicos (que formam mais facilmente o intermediário reativo necessário para a reação de Ritter) reagiram em apenas 1–4 horas, enquanto substratos mais exigentes precisaram de mais tempo. Tanto nitrilos aromáticos quanto alifáticos funcionaram bem, com substituintes fortemente retiradores de elétrons em nitrilos aromáticos tornando a reação ainda mais eficiente. No geral, o estudo demonstrou que o catalisador sólido pode igualar ou superar muitos ácidos líquidos, evitando meios corrosivos e solventes extras.
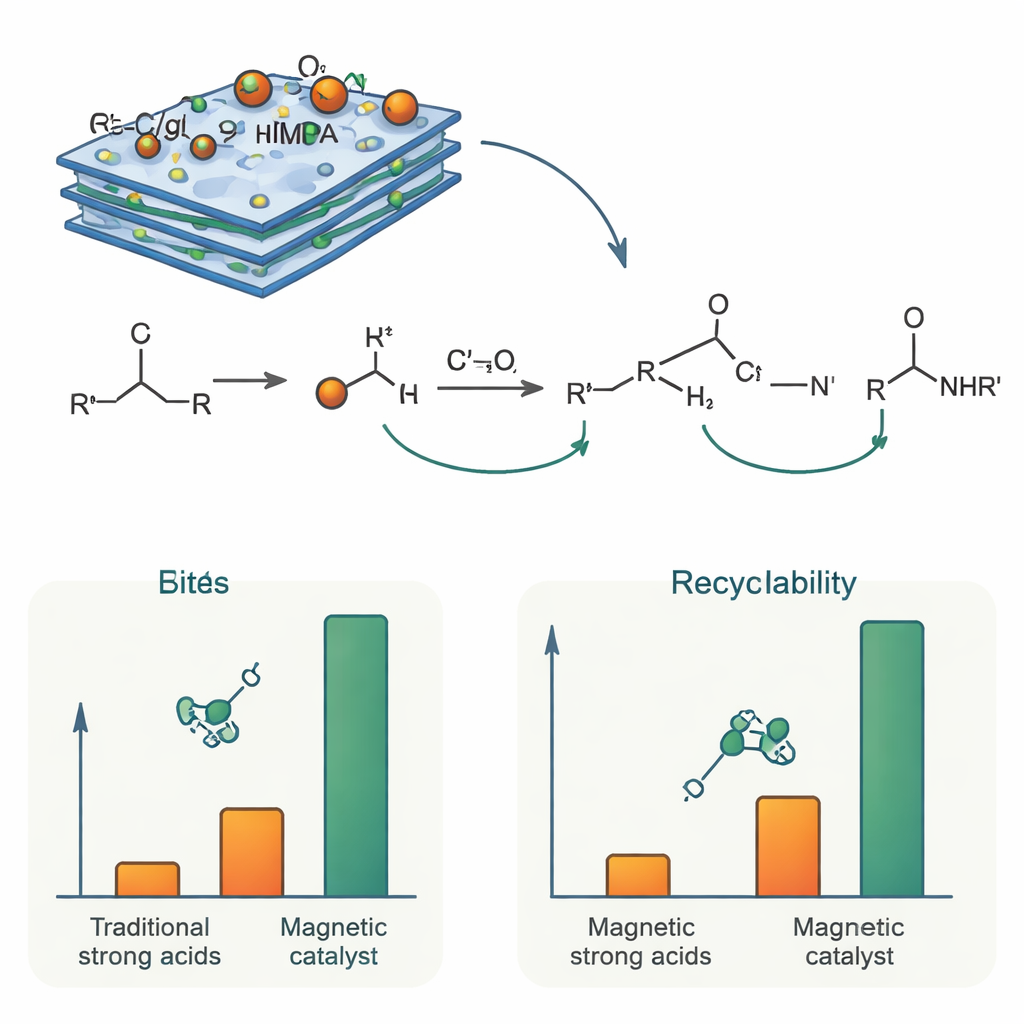
Como funciona e por que perdura
Do ponto de vista químico, o papel do catalisador é protonar temporariamente o álcool e ajudar sua desidratação, gerando uma espécie carregada positivamente de curta duração. Uma molécula de nitrilo então ataca esse intermediário para formar uma nova ligação carbono–nitrogênio, que é finalmente convertida em amida por reação com a água formada no processo. Os grupos fosfônicos no NTMPA fornecem acidez controlada, forte o suficiente para impulsionar essas etapas, mas moderada pelo entorno de nitreto de carbono de modo que reações secundárias indesejadas sejam minimizadas. Como as unidades ativas de NTMPA estão quimicamente vinculadas ao suporte sólido, elas não se lixiviam durante a reação. Medições de magnetização confirmaram que as partículas permanecem fortemente magnéticas, permitindo que o catalisador gasto seja rapidamente removido com um ímã. Em testes de reuso, o mesmo lote de catalisador foi empregado pelo menos seis vezes com apenas uma pequena queda na atividade, e análises estruturais após o uso mostraram que sua composição e morfologia permaneceram amplamente inalteradas.
O que isso significa para uma fabricação mais verde
Para um leitor não especialista, a principal conclusão é que os autores desenvolveram um pó reutilizável e responsivo a ímãs que pode ajudar químicos a montar importantes ligações amida sem depender dos ácidos líquidos agressivos e dos solventes extras normalmente exigidos. Esta abordagem reduz resíduos, simplifica a purificação do produto e facilita a reciclagem do catalisador, tudo isso importante para uma química industrial mais sustentável. Embora o trabalho concentre‑se em um tipo de reação, os mesmos princípios de projeto — ancorar grupos ácidos fortes em um suporte robusto e magnético — podem ser aplicados a muitas outras transformações que sustentam a produção de medicamentos e materiais avançados.
Citação: Karimitabar, H., Sardarian, A.R. Efficient solvent-free amide synthesis via Ritter reaction catalyzed by a reusable Fe3O4/g-C3N4/ NTMPA nanocomposite. Sci Rep 16, 6494 (2026). https://doi.org/10.1038/s41598-026-35371-2
Palavras-chave: síntese de amida, reação de Ritter, <keyword>química sem solvente, catálise verde