Clear Sky Science · pt
Investigação dos resíduos funcionais em pontos quentes de uma enzima por monitoramento em tempo real da reação enzimática usando RMN e abordagens computacionais
Por que isso importa para antivirais futuros
Favipiravir é um comprimido já usado contra a gripe e testado para COVID‑19, mas não combate os vírus na forma como o engolimos. Nossas próprias células precisam primeiro convertê‑lo em uma molécula ativa que bloqueie o vírus. Este estudo dissecou, quase átomo por átomo, como uma enzima humana realiza uma etapa crítica de ativação e quais pequenas partes da enzima atuam como “pontos quentes” que controlam a velocidade e a eficiência com que o fármaco é ativado. Compreender esses detalhes pode orientar o desenho de antivirais de próxima geração que sejam mais potentes e mais previsíveis nos pacientes.
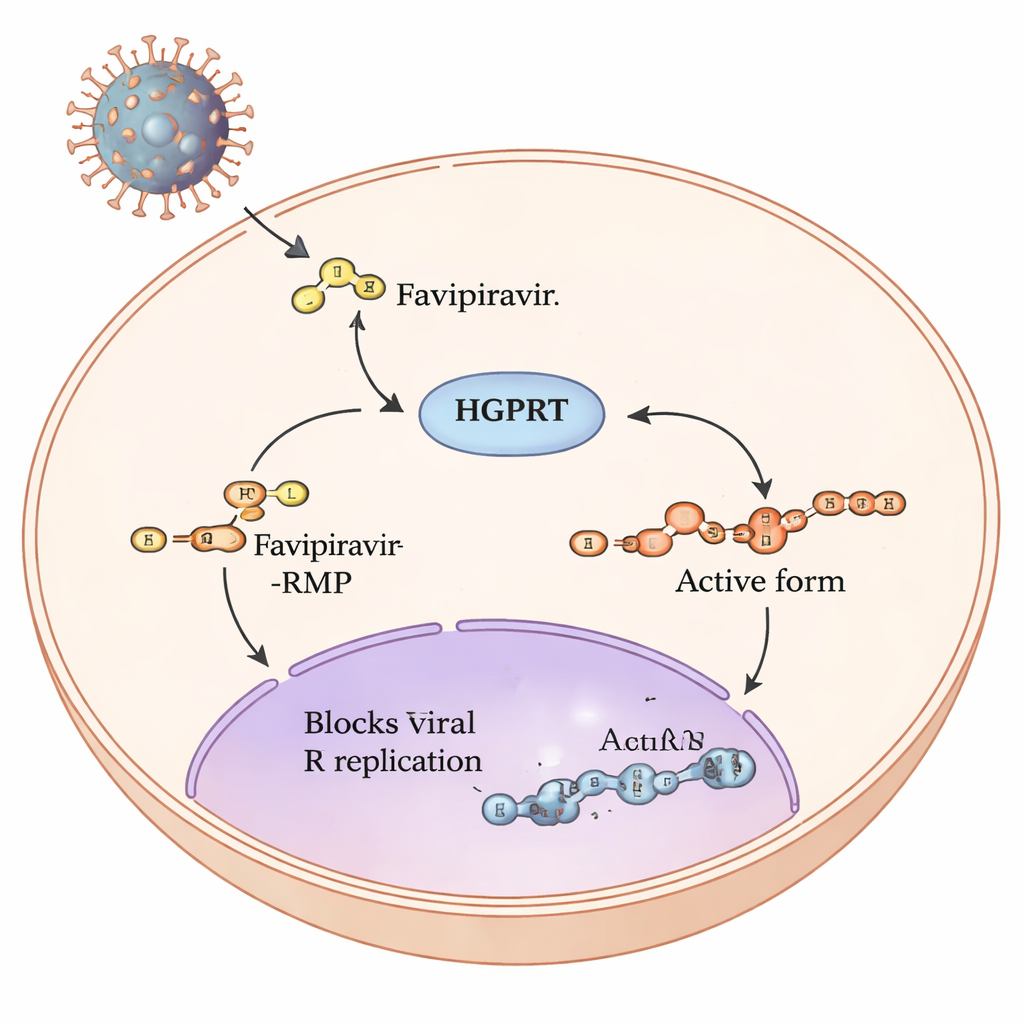
A jornada de um pró‑fármaco dentro de nossas células
Favipiravir é um chamado pró‑fármaco: uma vez que entra nas células humanas, uma série de etapas químicas o remodela em uma forma capaz de travar a maquinaria de cópia de vírus de RNA, como os da gripe e o SARS‑CoV‑2. A primeira e mais lenta etapa dessa via é realizada por uma enzima humana chamada hipoxantina‑guanina fosforribosiltransferase, ou HGPRT. A HGPRT adiciona um pequeno grupo açúcar‑fosfato ao favipiravir, produzindo favipiravir‑RMP. Só depois dessa etapa outras enzimas podem construir a forma trifosfato totalmente ativa que interfere diretamente com a RNA polimerase viral. Como essa primeira etapa catalisada pela HGPRT atua como um gargalo na quantidade de fármaco ativo produzido, os autores buscaram identificar quais partes da HGPRT são mais importantes para processar o favipiravir.
Observando a química em tempo real com RMN
De forma única, o favipiravir contém um átomo de flúor que se comporta como um minúsculo transmissor de rádio em um campo magnético. A equipe aproveitou isso usando espectroscopia por ressonância magnética nuclear do isótopo flúor‑19 para observar, em tempo real, quanto de favipiravir e quanto de favipiravir‑RMP estavam presentes em um tubo de ensaio à medida que a reação progredia. Como apenas o fármaco carrega flúor, os sinais de RMN são limpos e fáceis de acompanhar. Registrando espectros repetidamente ao longo de 12 horas, os pesquisadores puderam seguir o desaparecimento do fármaco inicial e o surgimento do produto modificado, e então extrair medidas cinéticas padrão, como a velocidade da reação e o aparente afinamento com que a enzima liga o fármaco.
Ajustando posições-chave na enzima
Imagens de raios X anteriores da HGPRT ligada ao favipiravir‑RMP haviam sugerido um punhado de aminoácidos que acomodam o fármaco em um bolso. O novo trabalho testa três dessas posições fazendo mudanças precisas de uma única letra no proteína e comparando cada enzima mutante com a natural. Uma modificação, chamada T138A, tornou a enzima surpreendentemente cerca de quatro a seis vezes mais rápida na conversão do favipiravir, mesmo tendo removido um grupo químico que se supunha ajudar a segurar o fármaco. Uma segunda mudança, K140M, desacelerou moderadamente a reação e enfraqueceu um pouco a ligação aparente. Uma terceira mudança, D193N, aboliu completamente a capacidade da enzima de produzir favipiravir‑RMP, embora a proteína alterada ainda pudesse ser produzida e ligar o produto. Juntos, esses resultados mostram que nem todos os pontos de contato são equivalentes: alguns atuam como reguladores sutis de velocidade, enquanto outros são interruptores essenciais.
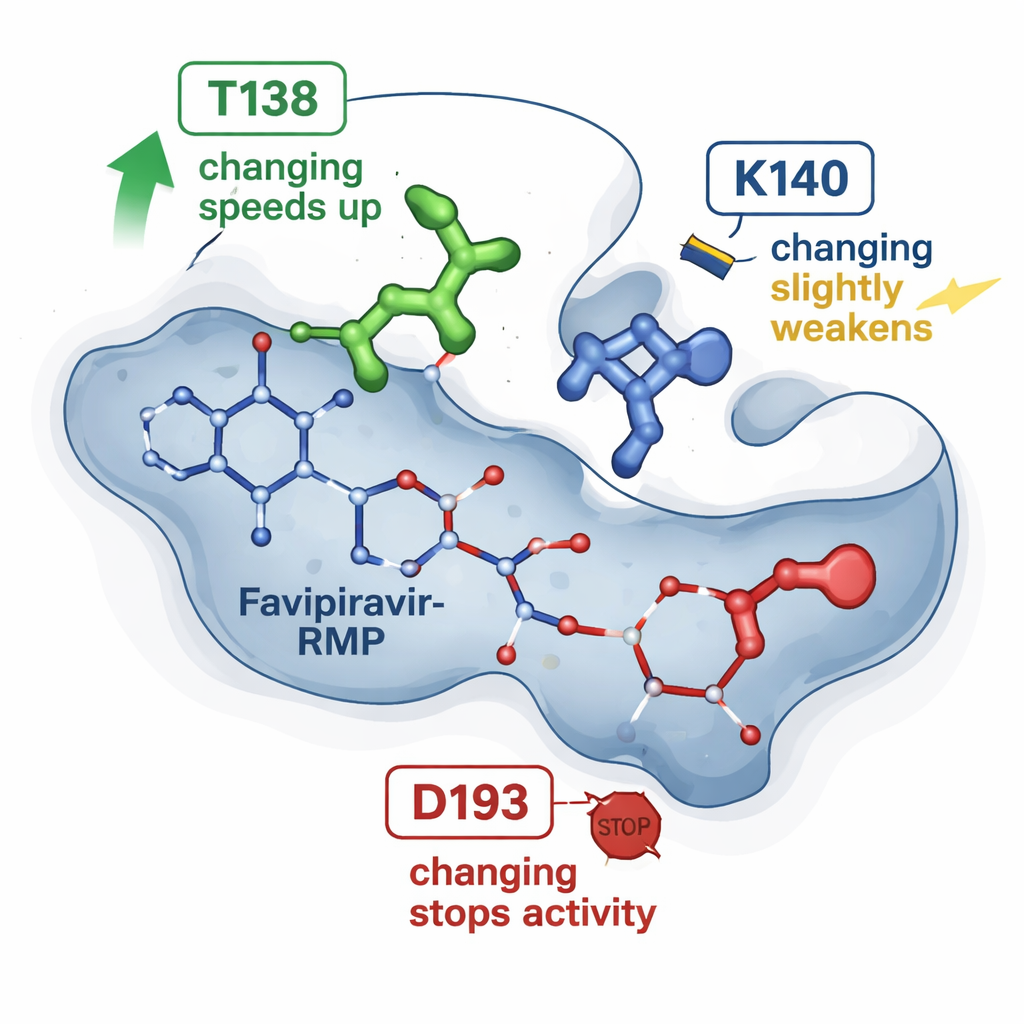
Simulando as peças em movimento no computador
Para ver além das estruturas estáticas, os pesquisadores recorreram a simulações moleculares. Partindo da estrutura tridimensional conhecida da HGPRT com favipiravir‑RMP, usaram ferramentas computacionais estabelecidas para estimar quão fortemente o fármaco se liga em cada mutante e para rodar muitas simulações de dinâmica molecular curtas. Essas simulações acompanham como os átomos se movem e interagem ao longo de dezenas de nanossegundos. Os cálculos concordaram com as tendências derivadas da RMN: a variante T138A tendia a manter o favipiravir‑RMP de forma mais favorável, mas também apresentou episódios em que o fármaco se deslocava em direção a uma via de “escape”, guiado por outro resíduo (K140) que ancora brevemente o grupo fosfato antes da liberação. Em contraste, a variante D193N ainda segurava o produto, mas provavelmente falhou em uma etapa catalítica anterior que requer um íon magnésio, explicando por que perdeu atividade apesar da ligação estável.
Um roteiro para um design antiviral mais inteligente
Ao combinar medições em tempo real por RMN com modelos computacionais detalhados, este estudo mapeia os pontos quentes funcionais na HGPRT que governam quão eficientemente o favipiravir é ativado. Para não especialistas, a conclusão é que nossas próprias enzimas podem influenciar fortemente quanto fármaco antiviral ativo se acumula dentro das células, e que ajustar a forma do fármaco ou o bolso da enzima pode mudar drasticamente esse resultado. A estratégia híbrida dos autores oferece um roteiro geral para investigar como outros medicamentos interagem com suas proteínas‑alvo, potencialmente acelerando o desenvolvimento de novos compostos antivirais mais bem adaptados à maquinaria de ativação do corpo.
Citação: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Palavras-chave: favipiravir, ativação antiviral, enzima HGPRT, espectroscopia de RMN, desenvolvimento de fármacos