Clear Sky Science · pt
Um sistema de etiqueta REC sem lisina para aplicações de biotinilação por proximidade
Por que pequenas etiquetas em proteínas importam
Dentro de cada célula, proteínas raramente atuam sozinhas — elas formam parcerias dinâmicas que impulsionam a saúde e a doença. Para estudar essas parcerias, os cientistas frequentemente prendem pequenas “etiquetas de identificação” às proteínas para que possam ser rastreadas, isoladas de uma mistura ou visualizadas ao microscópio. Um método popular chamado biotinilação por proximidade permite mapear quem está perto de quem dentro da célula, mas traz um problema oculto: muitas dessas etiquetas são quimicamente modificadas e efetivamente desaparecem justamente quando mais são necessárias. Este estudo apresenta um novo tipo de etiqueta, chamada etiqueta REC, projetada para permanecer visível sob essas condições exigentes.
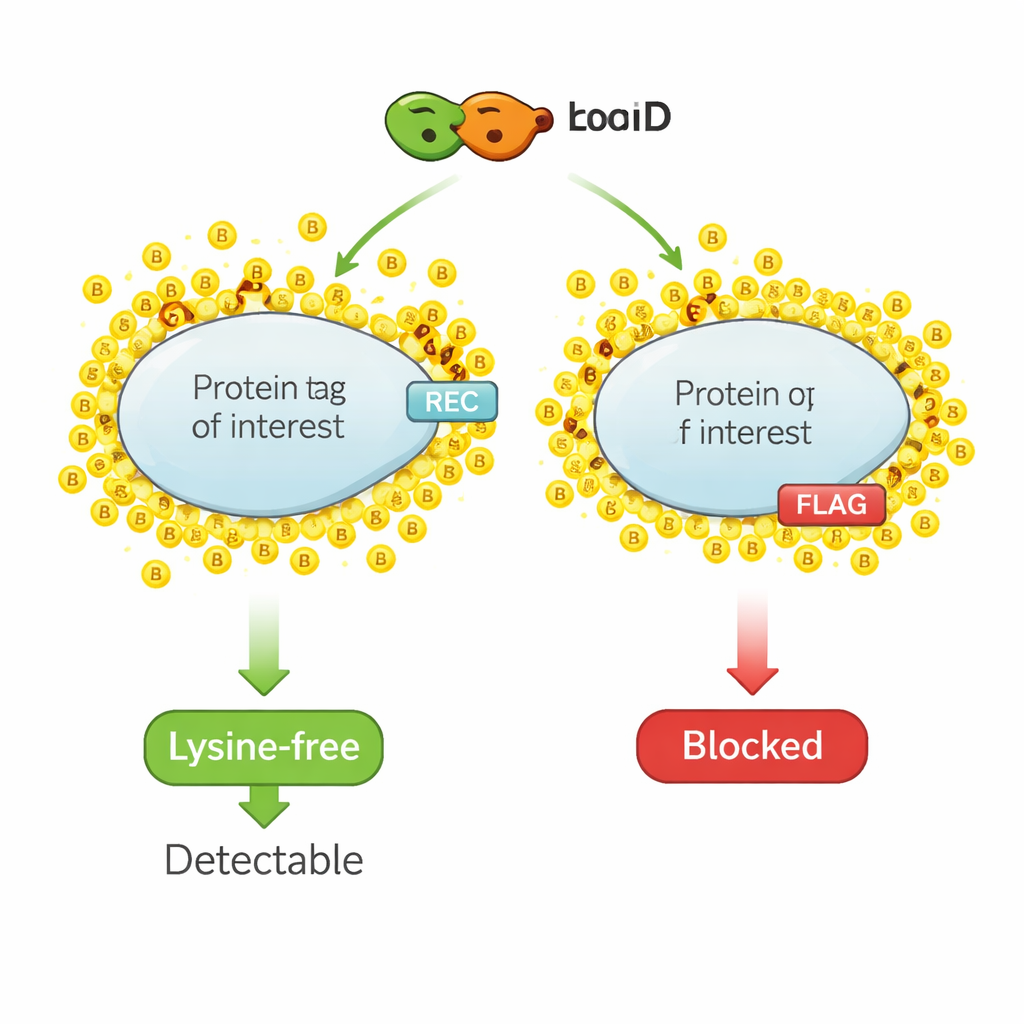
Um marcador químico para vizinhos proteicos
A biotinilação por proximidade funciona como uma caneta marca-texto molecular. Uma enzima modificada, como a TurboID, é fundida a uma proteína de interesse. Quando biotina — uma pequena vitamina — é adicionada, a TurboID rapidamente anexa moléculas de biotina às proteínas próximas. Os pesquisadores então pescam todas as proteínas marcadas com biotina e as identificam, obtendo um instantâneo do entorno proteico. Contudo, a mesma química que marca proteínas vizinhas também atinge as pequenas etiquetas epítopo comumente usadas para detecção, porque essas etiquetas costumam conter lisina, um aminoácido que é o principal sítio de ligação da biotina. Quando as lisinas na etiqueta são cobertas por biotina, os anticorpos não conseguem mais reconhecer a etiqueta, e o sinal nos métodos padrão de detecção cai ou desaparece.
Projetando uma etiqueta que recusa modificação
Para resolver isso, os autores propuseram criar uma nova etiqueta completamente livre de lisina. Eles partiram de um fragmento de uma proteína do parasita da malária chamada PfRipr5, que tem pouca semelhança com proteínas humanas, reduzindo o risco de reações cruzadas indesejadas. Usando um método de triagem em microchip em coelhos, geraram 22 anticorpos monoclonais contra PfRipr5 e identificaram um, apelidado de clone n.º 6, com ligação especialmente forte e específica. Ao podar e mutar sistematicamente o fragmento PfRipr5, reduziram o alvo do anticorpo a um trecho de 11 aminoácidos. Essa sequência mínima continha apenas uma lisina, que eles substituíram por um aminoácido similar, a arginina. Notavelmente, o anticorpo manteve a mesma afinidade. Essa sequência otimizada e sem lisina foi chamada de etiqueta REC, e o anticorpo correspondente, anticorpo REC.
Testando rigorosamente a etiqueta REC
Em seguida, a equipe testou se a etiqueta REC poderia substituir etiquetas amplamente usadas, como FLAG, em técnicas laboratoriais comuns. Quando fundida a proteínas fluorescentes ou de sinalização e produzida em sistemas sem células e em células de mamíferos, as proteínas marcadas com REC foram prontamente detectadas por imunoblotting, por um ensaio de alta sensibilidade baseado em luminescência chamado AlphaScreen e por imunomarcação em células. A força de detecção foi semelhante à da etiqueta FLAG e a outro sistema sem lisina (AGIA), e o anticorpo REC mostrou muito pouco ruído de fundo em várias linhas celulares humanas e de macacos. Importante, a etiqueta funcionou tanto quando posicionada no início quanto no final da proteína, e em proteínas localizadas em diversas regiões celulares, incluindo núcleo, mitocôndria, retículo endoplasmático e membrana plasmática.
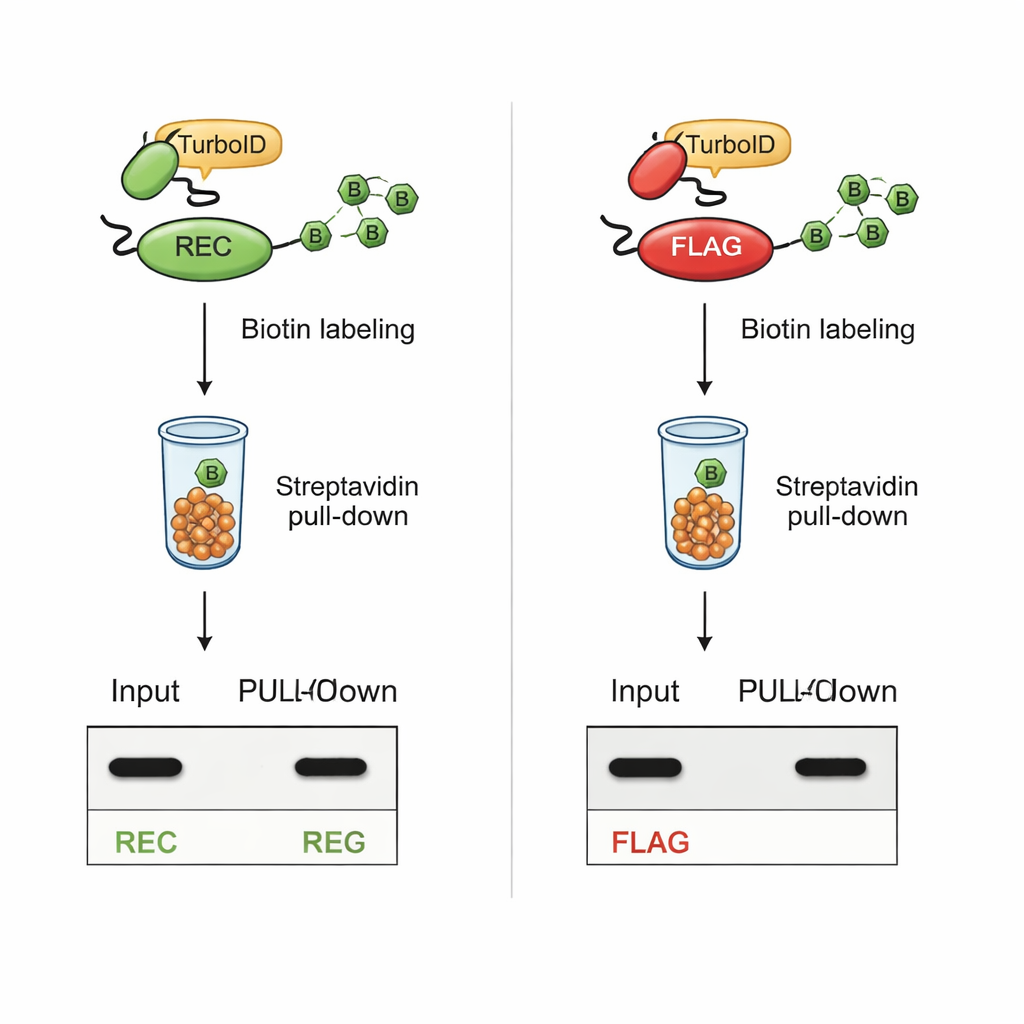
Permanecendo visível durante marcação intensa
O teste crítico foi verificar se o REC permaneceria detectável após a biotinilação mediada por TurboID. Em células onde a TurboID estava fundida a parceiros de interação conhecidos, proteínas carregando a etiqueta REC permaneceram claramente visíveis tanto em extratos totais de células quanto na fração purificada rotulada com biotina. Em contraste, proteínas com a etiqueta clássica FLAG perderam seu sinal FLAG uma vez que a TurboID estava ativa, embora as proteínas em si ainda estivessem presentes. Experimentos adicionais com peptídeos sintéticos mostraram que a TurboID biotinila diretamente as lisinas na sequência FLAG, bloqueando fisicamente o acesso do anticorpo. A etiqueta REC, desprovida de lisina, permaneceu intacta diante da TurboID e continuou fácil de detectar.
O que isso significa para experimentos futuros
Para pesquisadores que exploram redes proteicas em células vivas, a etiqueta REC oferece uma nova ferramenta prática: ela se comporta como etiquetas familiares em ensaios cotidianos, mas continua a funcionar mesmo quando enzimas potentes de marcação por proximidade estão ativas. Isso significa que os cientistas podem confirmar com mais confiança que suas proteínas marcadas estão presentes e foram corretamente capturadas, além de estudar outras modificações baseadas em lisina — como ubiquitinação e acetilação — sem que a própria etiqueta interfira. Em resumo, o REC é uma pequena mudança de projeto com grande impacto, ajudando a tornar experimentos complexos de mapeamento proteico mais claros e confiáveis.
Citação: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Palavras-chave: marcação de proteínas, biotinilação por proximidade, TurboID, interações proteicas, etiquetas epítopo