Clear Sky Science · pt
Interação entre metilação do DNA de ELMO1 e Med31 promove EMT e metaplasia intestinal induzidas por H. pylori no câncer gástrico via polarização M2
Por que as bactérias do estômago importam para o risco de câncer
A maioria de nós carrega bilhões de bactérias no trato digestivo, e uma delas — Helicobacter pylori — pode viver silenciosamente no estômago por décadas. Para algumas pessoas essa infecção é inócua, mas para outras torna‑se o primeiro passo rumo ao câncer gástrico, um dos tipos de câncer mais letais do mundo. Este estudo explora como uma pequena alteração química no DNA das células do estômago ajuda a transformar uma infecção persistente em dano precanceroso e, eventualmente, em um ambiente que favorece o crescimento tumoral.
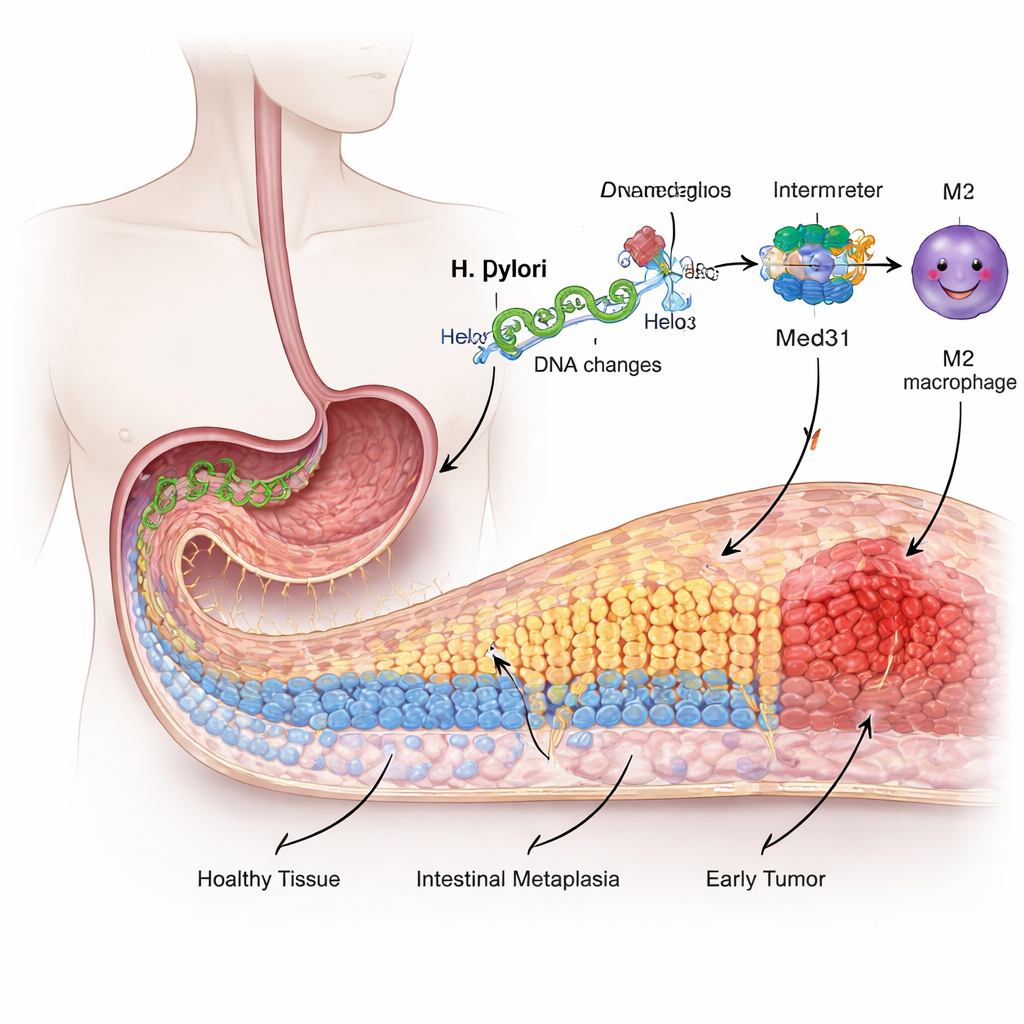
Do revestimento amigável a uma transformação de risco
A superfície interna do estômago é revestida por células especializadas, adaptadas para lidar com ácido forte, não para a digestão de alimentos como o intestino. Ao longo de anos de irritação e inflamação causada por H. pylori, algumas dessas células gástricas começam a “redecorar”‑se, assumindo características de células intestinais em um processo chamado metaplasia intestinal. Essa alteração é considerada um estágio precanceroso. Os pesquisadores usaram uma linhagem celular gástrica humana para mimetizar a infecção e descobriram que a exposição a H. pylori fez essas células crescerem mais rápido, moverem‑se com mais facilidade e ativarem marcadores do tipo intestinal — todos sinais de que o revestimento estava se afastando de sua identidade normal.
Pequenas etiquetas químicas com grandes consequências
Nosso DNA pode ser marcado com pequenas etiquetas químicas chamadas grupos metil, que funcionam como interruptores liga‑desliga para genes sem alterar o código genético em si. A equipe concentrou‑se em um gene chamado ELMO1, já conhecido por participar do movimento celular e da disseminação do câncer. Eles mostraram que a infecção por H. pylori aumentou a metilação do gene ELMO1 e, de forma aparentemente contraintuitiva, elevou sua atividade e os níveis de proteína nas células gástricas. Quando usaram um fármaco que remove essas marcas metil, as células perderam muitas das mudanças induzidas pela infecção: dividiram‑se menos, moveram‑se menos e apresentaram menos sinais de metaplasia intestinal. Isso apontou a metilação de ELMO1 como um interruptor crucial acionado pela bactéria.
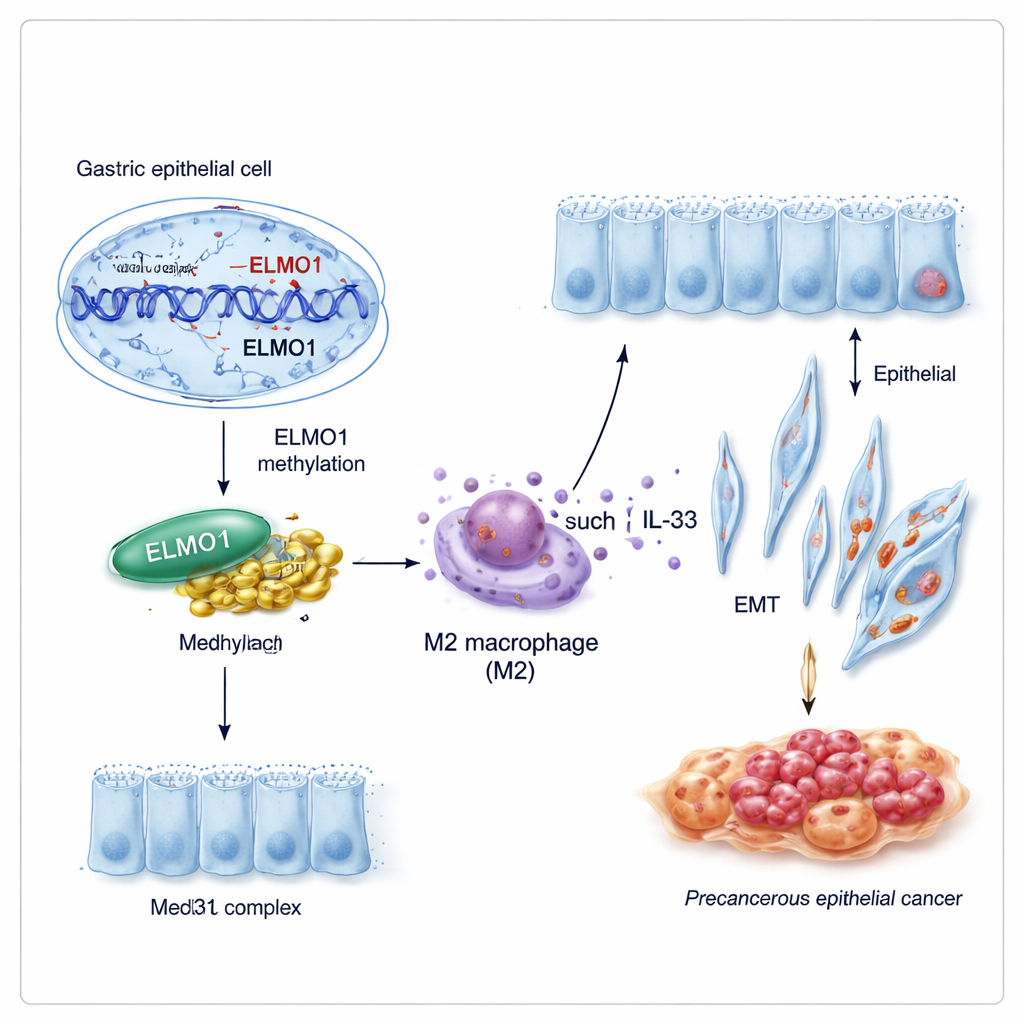
Uma nova parceria que reprograma o comportamento celular
Genes raramente atuam isoladamente. Os pesquisadores descobriram que o ELMO1 metilado favorece uma parceria com outra proteína, Med31, parte de um grande “painel de controle” que ajuda a decidir quais genes uma célula ativa. Em condições que promovem a metilação do DNA, os níveis de ELMO1 aumentaram, Med31 cresceu e as duas proteínas passaram a se ligar fisicamente, enquanto uma parceira conhecida anterior de ELMO1, DOCK10, ficou em segundo plano. Essa nova dupla ELMO1–Med31 parece deslocar o programa de expressão gênica das células gástricas de formas que as encorajam a adotar características intestinais e a comportarem‑se de modo mais agressivo.
Como as células imunes são incentivadas a ajudar o tumor
O câncer não se desenvolve isoladamente; cresce dentro de um bairro complexo de células imunes e de suporte. O estudo mostra que células gástricas infectadas com ELMO1 metilado liberam níveis mais altos de IL‑33, um sinal que impulsiona células imunes vizinhas chamadas macrófagos a um estado “M2” pró‑tumoral. Usando um sistema de cocultura, os autores descobriram que macrófagos expostos a esses sinais se inclinaram fortemente para o tipo M2 e, por sua vez, secretaram fatores que induziram novas células gástricas a tornarem‑se mais móveis, mais invasivas e mais parecidas com células intestinais. Marcadores de transição epitélio‑mesênquima — quando células do revestimento estacionárias se transformam em células migratórias e com capacidade de invasão — aumentaram acentuadamente sob a influência desses macrófagos M2.
O que isso significa para prevenir o câncer de estômago
Em conjunto, o trabalho traça uma cadeia de eventos: a infecção por H. pylori altera a metilação do DNA de ELMO1, esse ELMO1 modificado se associa a Med31, as células infectadas enviam sinais que convertem as células imunes próximas em ajudantes M2, e esses ajudantes então promovem tanto a metaplasia intestinal quanto um estado celular mais invasivo. Para leigos, a ideia central é que uma bactéria comum do estômago pode remodelar tanto o revestimento gástrico quanto a resposta imune local por meio de marcas químicas reversíveis no DNA. Compreender essa via pode abrir caminhos para novos testes sanguíneos que detectem padrões de metilação de risco precocemente, bem como para fármacos que interrompam o eixo ELMO1–Med31–M2 antes que uma infecção crônica progrida para câncer gástrico.
Citação: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Palavras-chave: câncer gástrico, Helicobacter pylori, metilação do DNA, metaplasia intestinal, microambiente tumoral