Clear Sky Science · pt
Avaliação da base bioquímica por trás da resistência contra a amiloidose sistêmica
Quando pequenas mudanças em proteínas bloqueiam um acúmulo letal
Muitas doenças inflamatórias crônicas, da artrite reumatoide à tuberculose, podem desencadear uma complicação rara, mas muitas vezes fatal, chamada amiloidose sistêmica AA. Nessa condição, uma proteína sanguínea normal se acumula como fibras rígidas que obstruem órgãos. Este estudo faz uma pergunta surpreendentemente esperançosa: pequenas mudanças naturais nessa proteína podem tornar alguns animais largamente imunes à doença — e, em caso afirmativo, como?
A ameaça oculta dos acúmulos proteicos
A amiloidose AA começa com um sinal inflamatório no sangue chamado amilóide sérico A (SAA). Durante inflamação severa ou prolongada, os níveis de SAA podem disparar a milhares de vezes acima do normal. Em algumas pessoas e animais, parte dessa proteína se desenrola de maneira anômala e empilha-se em longas fibras, conhecidas como fibrilas amilóides, que se espalham por órgãos como baço e rins. Com o tempo, essas fibras comprometem a função orgânica. No entanto, nem todo indivíduo com níveis altos de SAA desenvolve amiloidose, e certas linhagens de camundongos permanecem surpreendentemente resistentes mesmo quando expostas a condições que induzem a doença em laboratório. Entender por quê pode apontar para novas estratégias de prevenção do acúmulo de amiloide em humanos.
Camundongos resistentes e suas versões especiais da proteína
Em camundongos, a maioria das fibrilas amilóides AA surge de uma versão da SAA chamada SAA1.1, fortemente associada à doença. No entanto, algumas linhagens produzem predominantemente versões ligeiramente alteradas, denominadas SAA1.5 e SAA2.2, e essas linhagens raramente desenvolvem amiloidose sistêmica AA. As proteínas diferem apenas por um punhado de blocos construtores (aminoácidos), mas essas diferenças se agrupam em uma região densamente empacotada que forma o núcleo interno das fibrilas causadoras da doença. Os pesquisadores propuseram que essas pequenas diferenças não impedem por completo a agregação das proteínas, mas em vez disso evitam que elas adotem a forma fibrilar muito específica que é danosa.
Colocando as proteínas à prova no laboratório
Para investigar essa ideia, a equipe produziu as três variantes de SAA de camundongo em bactérias e observou seu comportamento em experimentos de tubo de ensaio. Eles monitoraram a formação de fibrilas usando um corante fluorescente que acende quando a amiloide se forma, e verificaram as estruturas com microscopia eletrônica. A SAA1.1 associada à doença formou prontamente longas fibrilas retilíneas. A SAA2.2 também podia formar fibrilas, mas elas eram mais espessas, mais torcidas e estruturalmente mais variadas, e não desencadearam o mesmo forte sinal do corante. A SAA1.5, em contraste, não formou fibrilas nas condições testadas. Quando os cientistas adicionaram pequenas amostras de fibrilas reais da doença retiradas de baços de camundongos doentes como “sementes”, a SAA1.1 rapidamente cresceu novas fibrilas que copiavam de perto a estrutura do original, como um príon. De forma marcante, SAA1.5 e SAA2.2 não cresceram sobre essas sementes; as fibrilas ex vivo não conseguiram recrutá-las para a conformação patogênica.
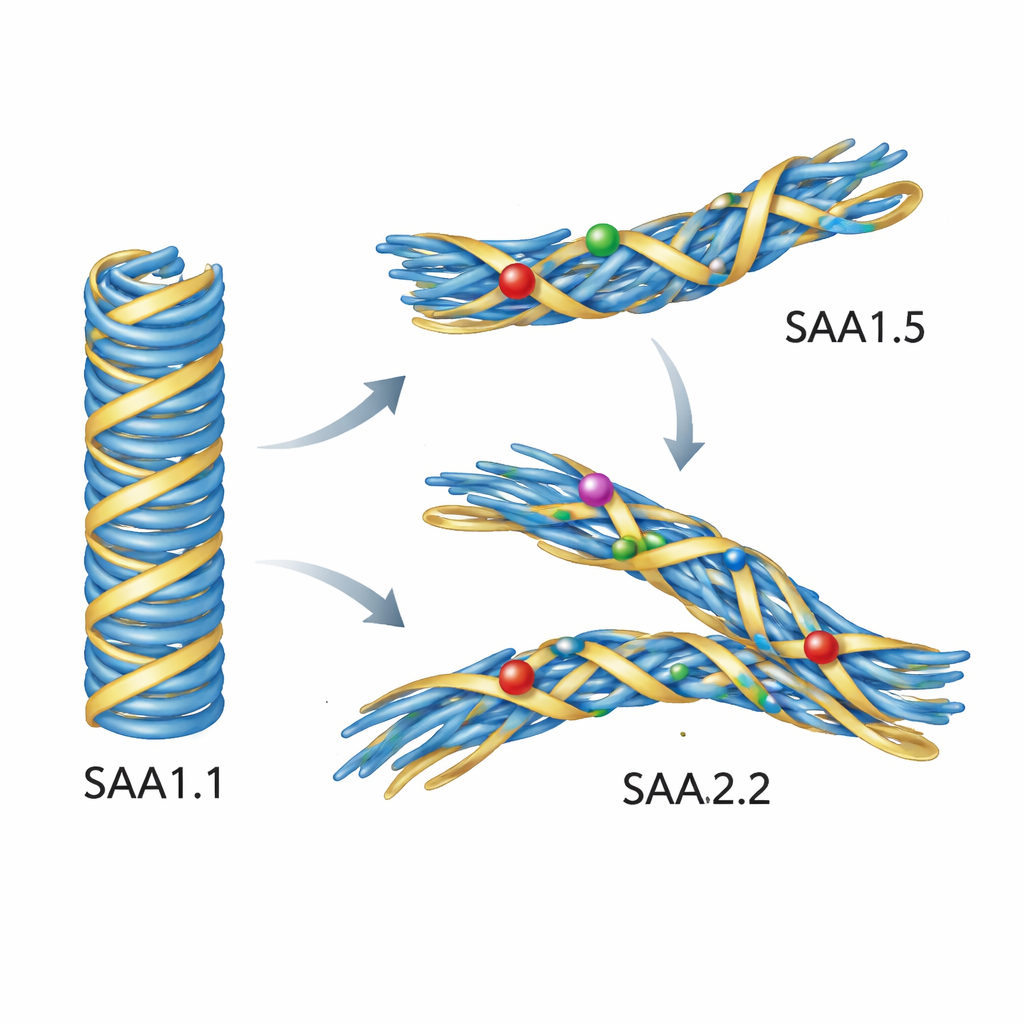
Simulações revelam por que as proteínas mutantes recusam a forma nociva
Experimentos isolados não mostraram exatamente o que falha em nível atômico, então os autores recorreram a simulações computacionais detalhadas. Eles partiram de uma estrutura de alta resolução de uma fibrila AA patogênica de camundongo construída a partir de SAA1.1 e então substituíram computacionalmente pelas sequências SAA1.5 e SAA2.2. Ao simularem essas fibrilas em água à temperatura corporal, o modelo baseado em SAA1.1 permaneceu notavelmente estável. Em contraste, fibrilas construídas com SAA1.5 ou SAA2.2 deslocaram-se e se distorceram. Uma região de laço chave no núcleo moveu-se para fora e afrouxou seu contato com o segmento inicial da proteína, e várias cadeias laterais giraram para novas orientações. Esses rearranjos sutis perturbavam o empacotamento apertado que define a dobra associada à doença. Em outras palavras, as sequências variantes não se opunham a formar fibrilas em geral — mas não conseguiam acomodar confortavelmente o projeto da fibrila AA patogênica.
Como o design da natureza indica possíveis terapias futuras
Em conjunto, o trabalho mostra que linhagens de camundongo “resistentes à amiloide” não estão protegidas porque sua SAA não pode agregar. Em vez disso, suas versões de SAA são estruturalmente incompatíveis com a forma fibrilar específica que causa a amiloidose sistêmica AA. As proteínas ainda podem se aglomerar, mas o fazem em formas alternativas aparentemente benignas. Mutações protetoras semelhantes são conhecidas em outras doenças de desdobramento proteico, incluindo alguns casos de príon e Alzheimer. Isso sugere um princípio mais amplo: ajustar uma proteína propensa à doença para que não possa adotar sua arquitetura tóxica — mantendo ainda sua função normal — pode ser suficiente para prevenir a enfermidade. A longo prazo, terapias inspiradas por essas variantes naturais “resistentes”, ou por pequenos fragmentos derivados delas, poderiam ajudar a direcionar proteínas para longe de dobras nocivas e rumo a dobras inofensivas.
Citação: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Palavras-chave: amiloidose AA, amilóide sérico A, desenovelamento de proteínas, resistência à amiloide, modelos murinos