Clear Sky Science · pt
Modelagem e verificação experimental da precipitação de nanopartículas de policaprolactona
Por que pequenas esferas plásticas importam para a medicina
Imagine embutir um fármaco potente dentro de um ponto tão pequeno que ele pode atravessar vasos sanguíneos e liberar sua carga exatamente onde é necessário. Esses pontos, chamados nanopartículas poliméricas, estão no cerne de muitos tratamentos e ferramentas de imagem emergentes. Mas fabricá‑los com o tamanho certo e de forma reprodutível é surpreendentemente difícil. Este estudo mostra como um modelo computacional simples baseado em física pode prever e ajustar o tamanho de uma nanopartícula biodegradável amplamente usada, potencialmente poupando anos de tentativa e erro no desenvolvimento de novas nanomedicinas.
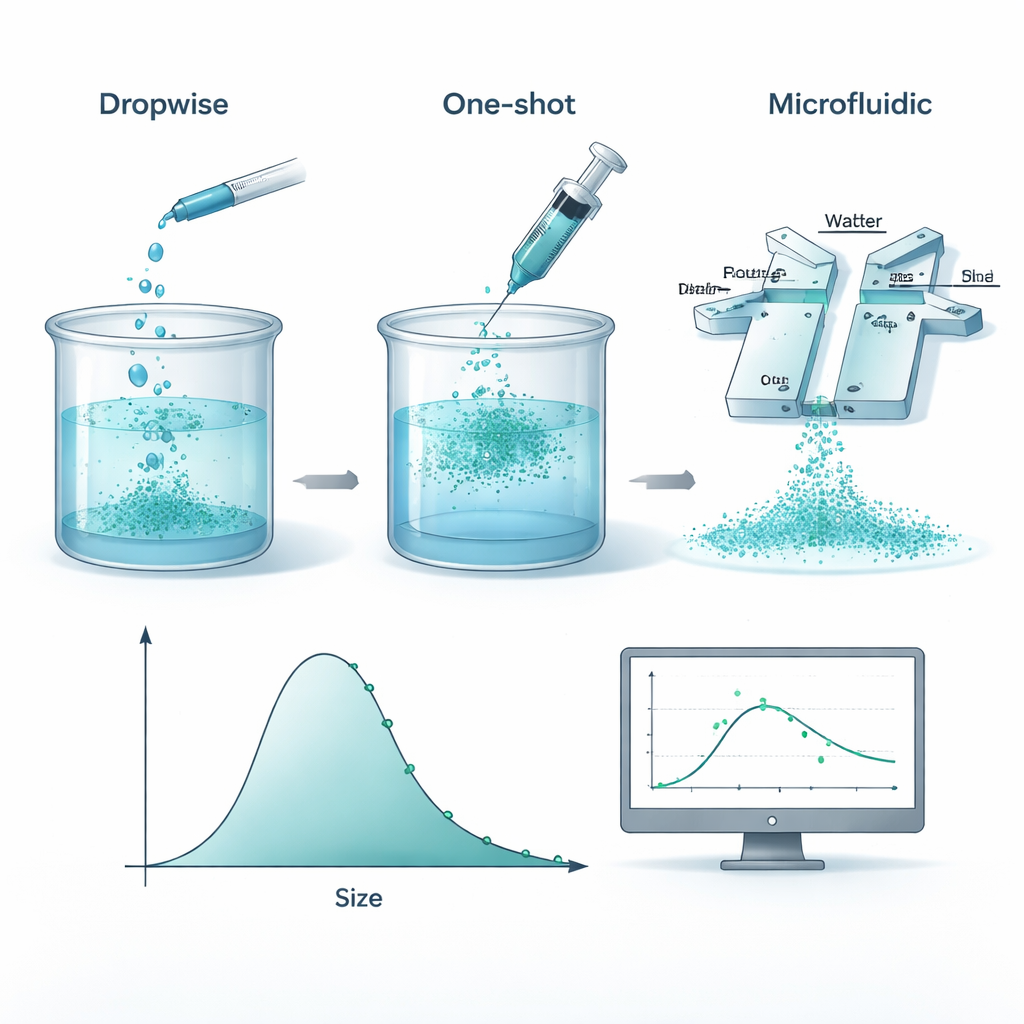
Do mexer de cozinha à precisão de laboratório
Para criar essas nanopartículas, os pesquisadores dissolvem um plástico biodegradável chamado policaprolactona (PCL) em um solvente orgânico e depois o misturam com água para que o polímero “saia” da solução e forme pequenas esferas. A equipe comparou três formas práticas de fazer isso: adicionar lentamente a solução polimérica gota a gota, despejá‑la de uma vez e injetar ambos os líquidos através de um pequeno chip microfluídico onde eles se encontram em canais estreitos. Sob condições cuidadosamente controladas, as três abordagens produziram partículas com tamanhos médios e dispersões de tamanho muito semelhantes. Isso significa que, ao menos nas faixas estudadas, o que importa mais do que o aparato exato de mistura é o que você coloca — quantidades de polímero e estabilizante — em vez de como se agita.
Como a viscosidade e as moléculas auxiliares moldam as partículas
Os pesquisadores então exploraram como os ingredientes da receita controlam o tamanho final das partículas. Aumentar a quantidade de PCL na fase orgânica torna esse líquido mais espesso, ou mais viscoso. Pense em tentar misturar xarope em água em vez de suco: um xarope mais grosso se quebra em gotas maiores. Aqui, soluções poliméricas mais viscosas levaram a nanopartículas maiores e a distribuições de tamanho ligeiramente mais amplas. Adicionar um segundo solvente, etanol, ajudou a manter o processo estável mesmo em níveis muito altos de polímero, mas ao custo de produzir partículas maiores na faixa de concentração mais elevada. Um segundo ingrediente, um surfactante chamado Pluronic F‑127, atua como um agente molecular antiaglomerante. Em níveis baixos de surfactante, as partículas tendem a colidir e aderir, crescendo e tornando‑se menos uniformes. À medida que a concentração de surfactante aumenta, ele reveste as superfícies das partículas, impede a fusão e gera nanopartículas menores e mais estáveis — até certo ponto, além do qual ganhos adicionais são modestos e a distribuição de tamanhos pode ficar mais heterogênea.
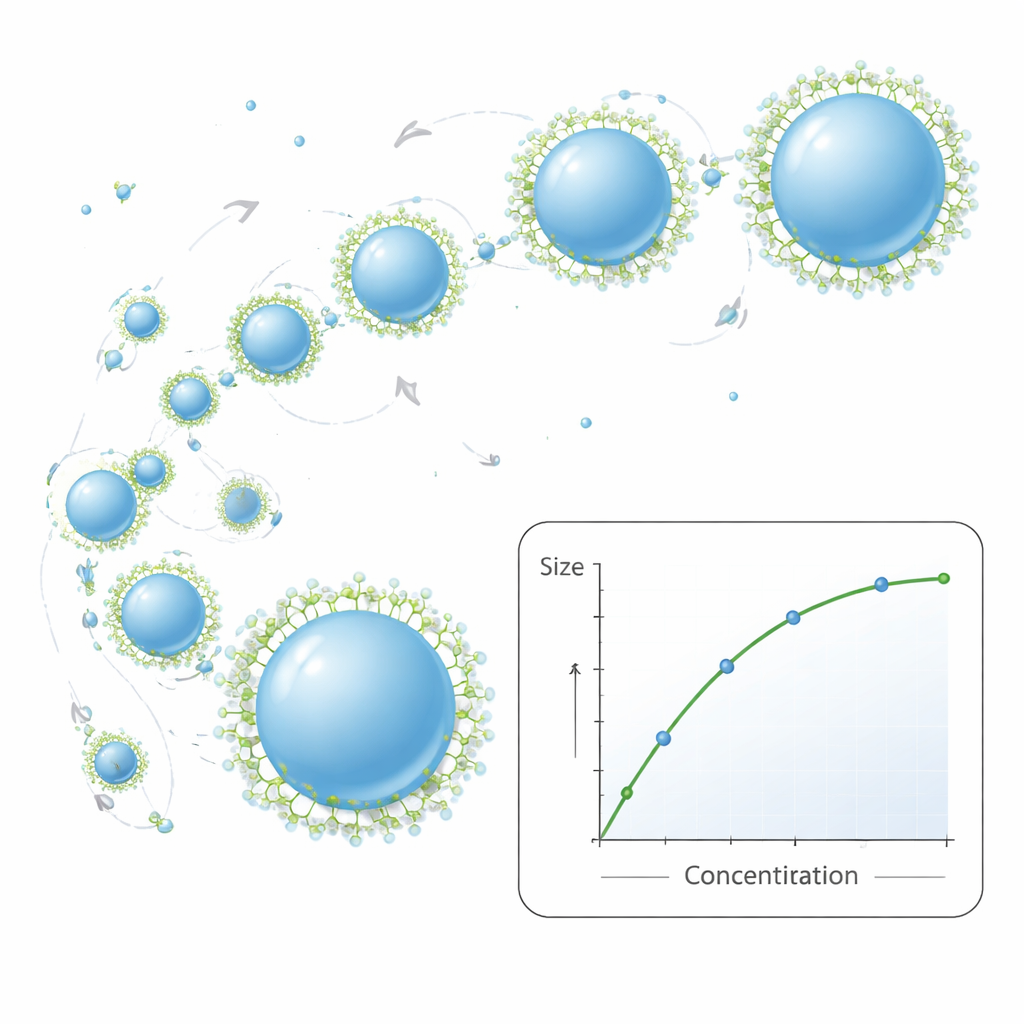
Uma regra simples de crescimento que corresponde à realidade
No cerne do trabalho está um modelo matemático compacto que descreve como as nanopartículas crescem depois que aparecem pela primeira vez. Ele trata seu movimento como um tremor aleatório no líquido, em que colisões às vezes levam dois fragmentos a se fundirem em um maior. Modelos anteriores assumiam que sempre que as partículas se encontravam, elas se mesclavam instantaneamente e viravam esferas perfeitas. O novo modelo acrescenta duas nuances realistas: primeiro, permite um tempo finito para que duas partículas em contato relaxem de uma forma alongada para uma única esfera; segundo, deixa que moléculas de surfactante gradualmente “bloqueiem” a superfície, desacelerando ou impedindo fusões adicionais. Com apenas alguns parâmetros mensuráveis — como temperatura, viscosidade do líquido e concentração inicial de polímero — o modelo prevê como o tamanho médio das partículas deve mudar com as condições da receita. Em muitos experimentos, os tamanhos previstos corresponderam de perto aos medidos por espalhamento de luz, ao mesmo tempo em que capturaram tendências gerais sobre o alargamento da distribuição de tamanhos.
Usando o modelo como ferramenta de projeto
Para testar se essa abordagem é realmente útil, a equipe inverteu o problema: em vez de pedir ao modelo que explicasse dados passados, eles o usaram para sugerir formulações que deveriam produzir três tamanhos específicos de nanopartículas e graus de uniformidade. Em seguida, prepararam essas formulações “projetadas” no laboratório. Os diâmetros medidos das partículas diferiram dos alvos por apenas 1–7 por cento — bem dentro da variação experimental típica — mostrando que o modelo pode orientar de forma confiável as escolhas de formulação. As previsões sobre quão estreita ou ampla seria a distribuição de tamanhos foram menos exatas, mas ainda suficientes para distinguir populações relativamente homogêneas de outras mais dispersas. Em comparação com métodos de simulação intensivos que acompanham cada molécula ou cada redemoinho do fluxo, este modelo enxuto roda rapidamente em computadores modestos e é fácil de adaptar a outros polímeros e configurações de processamento.
O que isso significa para a futura nanomedicina
Para não especialistas, a mensagem principal é que fabricar nanopartículas úteis não precisa mais depender exclusivamente de trabalhosos experimentos por tentativa e erro no laboratório. Ao capturar a física essencial de como pequenas gotas plásticas se movem, colidem e são protegidas por surfactantes, este trabalho entrega um “mapa” prático que relaciona escolhas de formulação — quanto polímero, qual mistura de solventes, quanto estabilizante — ao tamanho final das partículas. Como a PCL é um material biodegradável comum usado em liberação de fármacos, implantes e agentes de imagem, esse modelo pode ajudar pesquisadores a projetar nanomedicinas mais seguras e efetivas de forma mais rápida e com menos desperdício de material. Os mesmos princípios podem ser estendidos a outros polímeros, trazendo mais previsibilidade e eficiência ao mundo das terapias em escala nanométrica.
Citação: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Palavras-chave: nanopartículas poliméricas, nanoprecipitação, liberação de fármacos, modelagem numérica, policaprolactona