Clear Sky Science · pt
Nicorandil melhora a dor neuropática e inflamatória via sinalização TNF-α, IL6/MAPKERK1/2 e NO/cGMP
Por que aliviar a dor nervosa importa
Milhões de pessoas convivem com dor queimaçante, lancinante ou formigante que persiste muito depois da cicatrização de uma lesão. Essa dor “neuropática” pode ser notoriamente resistente a analgésicos comuns e frequentemente vem acompanhada de efeitos colaterais pelo uso prolongado de medicamentos. O estudo resumido aqui investiga se o nicorandil — um medicamento cardíaco já administrado a pacientes com dor no peito — também pode acalmar vias de dor hiperativas no sistema nervoso e como isso ocorre em nível celular.
Um remédio do coração entra na pesquisa sobre dor
O nicorandil é rotineiramente prescrito para tratar angina porque relaxa os vasos sanguíneos. Faz isso por duas ações principais: doa pequenas quantidades de óxido nítrico, uma molécula de sinalização, e abre determinados canais de potássio nas células. Trabalhos anteriores em animais sugeriram que o nicorandil também pode reduzir a dor agindo em receptores nervosos envolvidos em sensações de calor e pimenta e ativando o próprio sistema opióide do corpo. No presente estudo, os pesquisadores propuseram mapear o que acontece a jusante desses efeitos iniciais, concentrando-se na inflamação, no estresse oxidativo (uma espécie de “ferrugem” química) e em vias específicas de sinalização dentro das células nervosas.
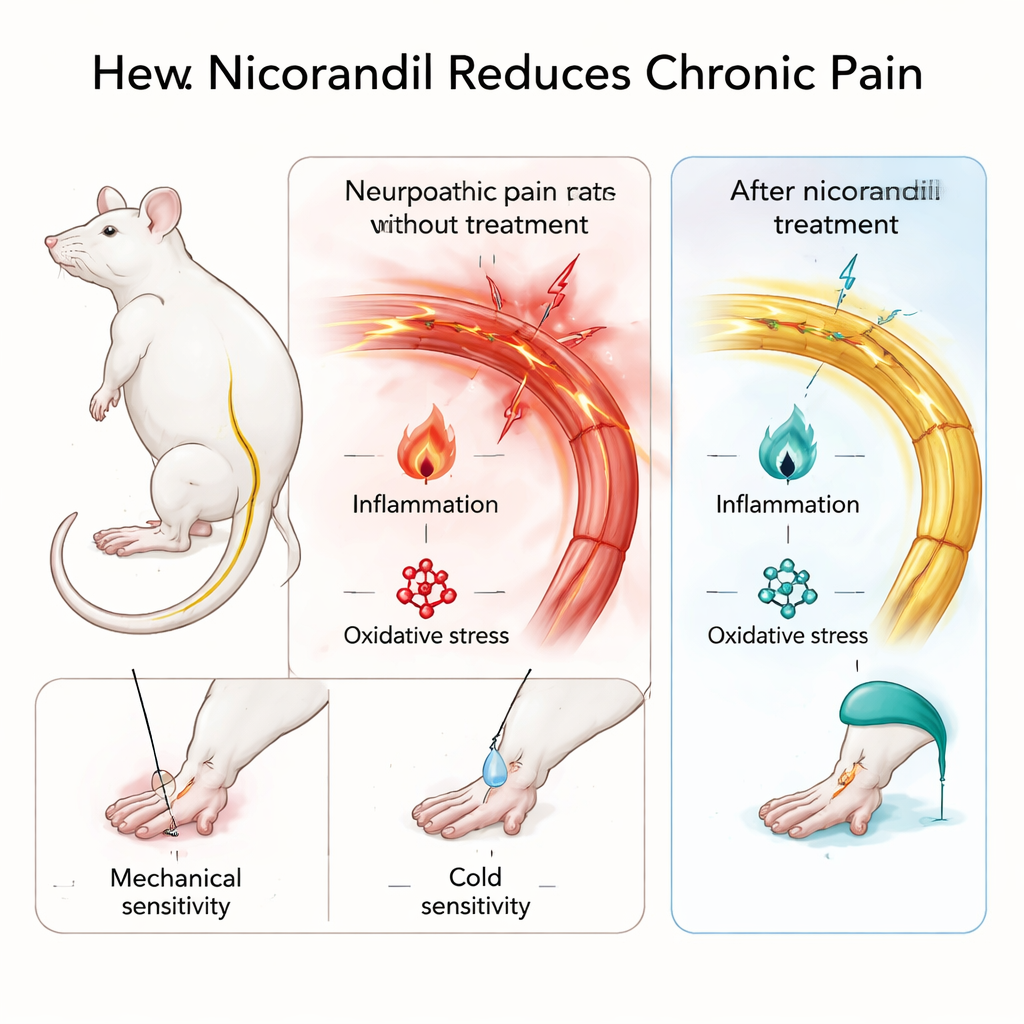
Testando o nicorandil em modelos de dor persistente
Para simular dor nervosa de longa duração, a equipe frouxamente laçou o nervo ciático em ratos, um procedimento clássico que produz sensibilidade ao toque e ao frio semelhante à dor neuropática humana. Eles também usaram o teste da formalina, no qual um irritante químico suave é injetado na pata para criar uma dor inflamatória bem definida e duradoura. Os ratos receberam nicorandil por via oral em duas doses, e os cientistas mediramm quão fortemente reagiam ao toque leve e ao frio na pata lesionada, assim como o quanto lambiam ou faziam movimentos de sobressalto após a formalina. Importante: o nicorandil não deixou os animais sonolentos ou instáveis em um teste de campo aberto, sugerindo que qualquer redução no comportamento de dor não se devia simplesmente a sedação.
Reduzindo sinais químicos de alarme
O nicorandil reduziu de forma clara tanto a dor induzida por lesão nervosa quanto a dor evocada pela formalina. Ratos tratados toleraram melhor o toque e o frio e apresentaram menos sobressaltos e tempos de lambedura mais curtos. Exames de sangue mostraram que o nicorandil diminuiu os níveis de mensageiros inflamatórios poderosos — fator de necrose tumoral alfa (TNF-α) e interleucina-6 (IL‑6) — além da ciclooxigenase‑2, uma enzima que contribui para a produção de prostaglandinas relacionadas à dor. Também reduziu o malondialdeído, um marcador de estresse oxidativo, indicando menor dano químico às membranas celulares. Ao microscópio, nervos de animais tratados com nicorandil pareciam mais saudáveis: houve menos dano estrutural e inchaço no nervo ciático e no conjunto de corpos celulares sensoriais conhecido como gânglio da raiz dorsal.
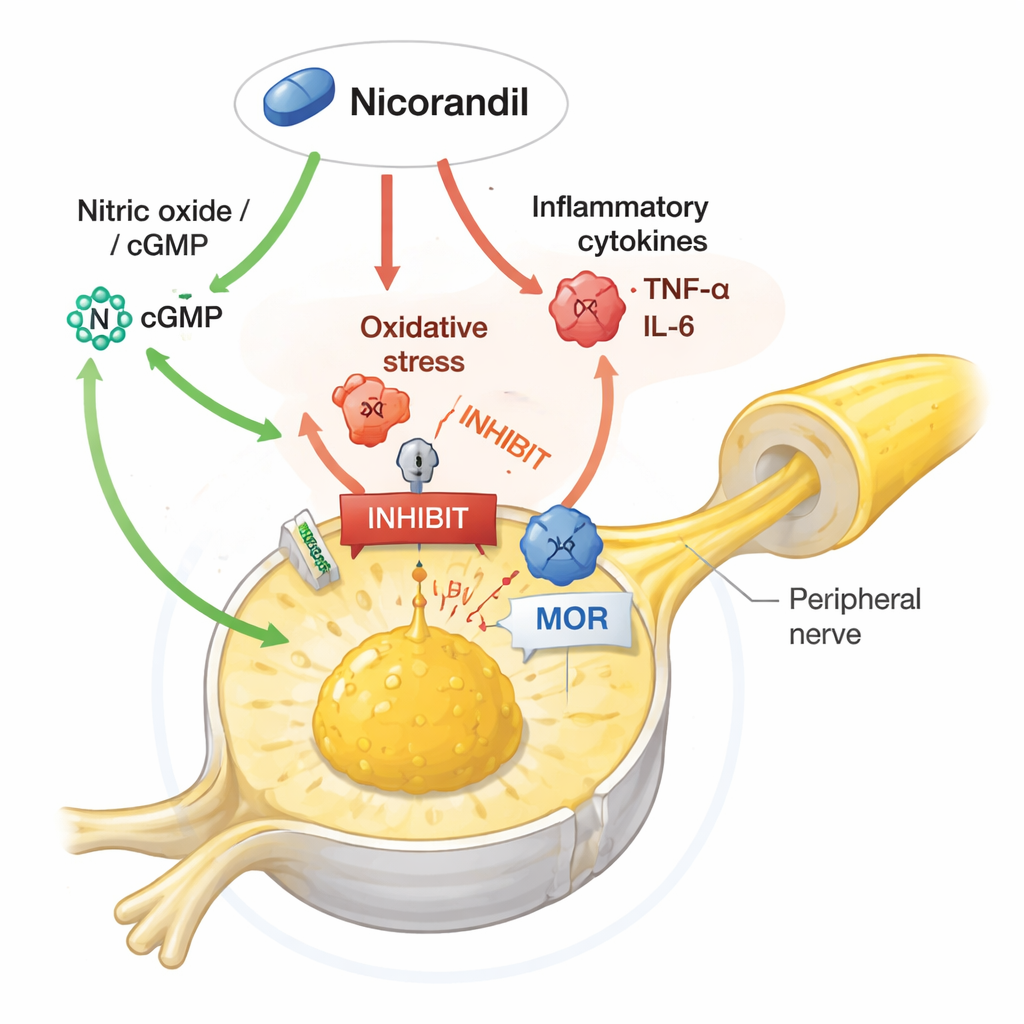
Desvendando a rede de sinalização dentro dos nervos da dor
O estudo avançou ao investigar quais vias moleculares eram necessárias para os benefícios do nicorandil. Quando os pesquisadores deram drogas que aumentavam o óxido nítrico ou elevavam o GMP cíclico (um mensageiro ligado ao óxido nítrico), eles parcialmente atenuaram a capacidade do nicorandil de reduzir a dor e de normalizar proteínas-chave. O nicorandil evitou o aumento habitual de ERK1/2, membro da família MAP quinase que amplifica sinais de dor, e conteve os níveis de TRPV1, um canal que torna os nervos mais sensíveis ao calor e a irritantes químicos. A intensificação da sinalização do óxido nítrico ou do GMP cíclico reverteu essas mudanças protetoras, enquanto bloquear enzimas que produzem óxido nítrico às vezes reforçou o alívio da dor pelo nicorandil. Surpreendentemente, bloquear os canais de potássio que o nicorandil costuma abrir não aboliu seus efeitos antinociceptivos, sugerindo que, nesse contexto, seu poder analgésico depende mais de modular o óxido nítrico, o estresse oxidativo, a inflamação e a sinalização relacionada a opióides do que de sua ação vascular clássica.
O que isso pode significar para pessoas com dor
No conjunto, os achados pintam o nicorandil como um modulador de dor de múltiplos alvos: ele acalma vias nervosas hiperativas ao reduzir o dano oxidativo e mensageiros inflamatórios, silenciar ERK1/2 e TRPV1 dentro de neurônios sensoriais e interagir com o óxido nítrico e o sistema opióide do próprio corpo. Embora esses resultados venham de modelos em ratos e de administração em curto prazo, sugerem que um medicamento já em uso clínico para doenças cardíacas pode um dia ser reposicionado ou adaptado para ajudar no tratamento de dores neuropáticas e inflamatórias difíceis. Estudos futuros em humanos serão necessários para determinar doses seguras, efeitos a longo prazo e se os mesmos mecanismos protetores operam nos nervos humanos.
Citação: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Palavras-chave: dor neuropática, nicorandil, inflamação, estresse oxidativo, sinalização do óxido nítrico