Clear Sky Science · pt
Interrupção da homeostase do zinco reduz níveis de acetilação de histonas em células normais e tumorais
Quando um metal útil se torna prejudicial
O zinco é mais conhecido como o nutriente presente em multivitamínicos que ajuda nosso sistema imunológico e a cicatrização. Mas dentro das células, o zinco precisa ser mantido em uma faixa muito estreita de “no ponto”. Este estudo mostra que, quando os níveis de zinco nas células ficam muito altos, eles podem silenciar silenciosamente genes importantes ao apertar a forma como o DNA é empacotado e até empurrar as células para um processo de autolimpeza chamado autofagia. Como suplementos de zinco, ingredientes anti‑caspa e drogas experimentais contra câncer podem alterar os níveis de zinco, entender esse sistema de controle oculto importa para a saúde diária e para terapias futuras.
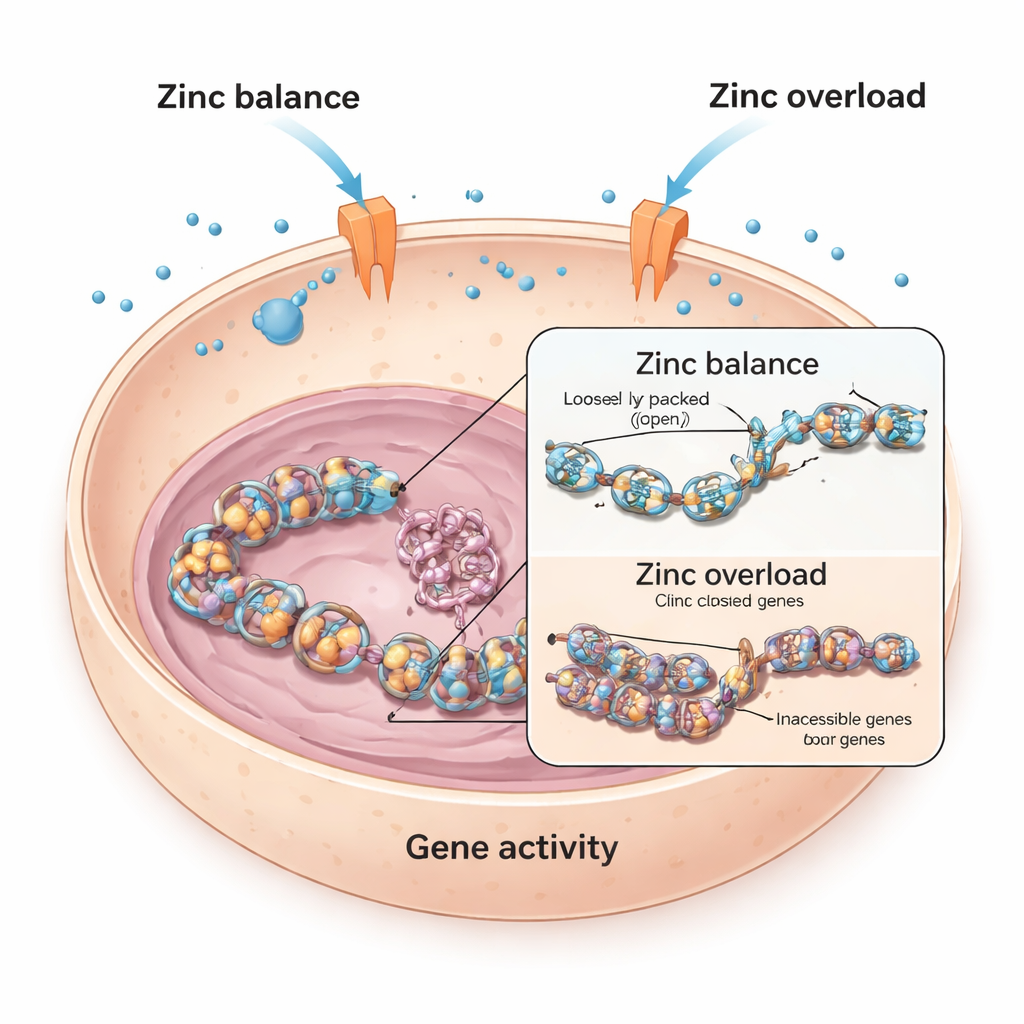
Equilibrando o zinco dentro de células vivas
Cada célula depende do zinco, que ajuda milhares de proteínas a desempenharem suas funções. Para evitar tanto a escassez quanto a sobrecarga, as células usam “portões” especiais em suas membranas, chamados transportadores de zinco, para mover o metal para dentro e para fora. Os pesquisadores começaram com células do músculo cardíaco de camundongos e humanos, perguntando o que acontece quando essas células são expostas a zinco extra. Eles descobriram que, nas células cardíacas de camundongo, níveis altos de zinco reduziram fortemente a atividade de um gene cardíaco chave chamado Bmp4, que ajuda a orientar o desenvolvimento e a função do coração. Em contraste, células cardíacas humanas foram muito menos afetadas, sugerindo que diferentes células se defendem contra a sobrecarga de zinco de maneiras distintas.
Como o zinco aperta o empacotamento do DNA
Para descobrir como o zinco silencia genes como Bmp4, a equipe examinou as histonas, as proteínas em forma de carretel em torno das quais o DNA é enrolado. Quando pequenas marcas químicas chamadas grupos acetil são adicionadas às histonas, o DNA fica mais solto e mais fácil de ser lido; quando essas marcas são removidas, o DNA se compacta mais e os genes ficam mais difíceis de serem ativados. O estudo mostrou que o excesso de zinco nas células cardíacas de camundongo levou a uma queda na acetilação de histonas em um sítio específico (conhecido como H3K9), acompanhando de perto a queda na atividade de Bmp4. Drogas que bloqueiam enzimas desacetilases de histonas puderam reverter o efeito do zinco e restaurar Bmp4, sugerindo que o zinco estava inclinando o equilíbrio desse sistema de marcação química.
Demais zinco por dentro, não apenas por fora
O passo crucial revelou‑se ser o zinco dentro do citoplasma aquoso da célula, não apenas no fluido ao redor. Usando uma sonda fluorescente que se acende na presença de zinco livre, os pesquisadores observaram um surto de zinco dentro das células cardíacas de camundongo após o tratamento. Quando usaram uma molécula carreadora de zinco para forçar o metal diretamente para dentro das células, observaram a mesma queda na acetilação de histonas e na atividade gênica, mesmo com muito menos zinco no meio externo. Nas células cardíacas humanas, em contraste, os transportadores na membrana celular ajustaram‑se rapidamente: alguns importadores de zinco foram desligados e exportadores aumentaram a atividade, prevenindo uma grande elevação do zinco interno e protegendo a acetilação das histonas. Células cardíacas de camundongo mostraram uma resposta de transportadores mais “mal configurada”, permitindo que mais zinco entrasse e perturbasse o controle gênico.
Do controle gênico à autolimpeza em células normais e tumorais
Os investigadores então perguntaram se esse aperto do empacotamento do DNA dirigido pelo zinco é único das células cardíacas. Eles testaram vários tipos de células humanas normais e linhas celulares tumorais do estômago, útero e ovário. Quando o zinco foi permitido se acumular no interior com a ajuda de um carreador, quase todas essas células apresentaram uma queda clara na acetilação de histonas. Em algumas células tumorais, como células de câncer gástrico, isso aconteceu em doses de zinco especialmente baixas, sugerindo que certos cânceres são incomumente sensíveis ao desequilíbrio do zinco. A equipe também relacionou a redução da acetilação à autofagia, um processo pelo qual as células reciclam componentes desgastados. Aumentos moderados de zinco interno estimularam a autofagia, mas zinco muito alto acabou por enfraquecê‑la, sugerindo uma janela estreita na qual o zinco poderia ser usado para ajustar esse caminho de autolimpeza.
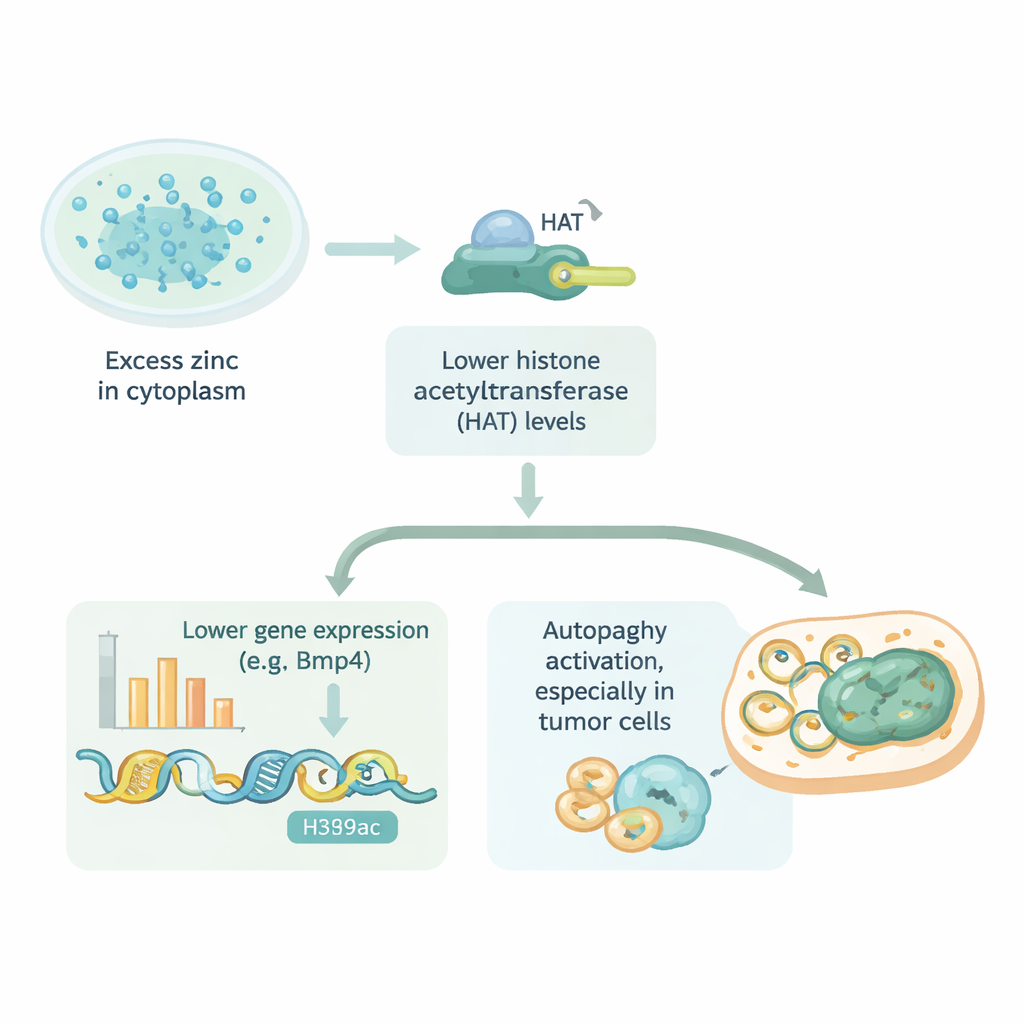
O que isso significa para saúde e tratamento
Em termos práticos, este trabalho revela que zinco em excesso dentro das células pode reduzir a atividade gênica tornando o DNA mais difícil de acessar, e que essa mesma via pode influenciar o quão ativamente as células se autoclean. O efeito não se limita às células cardíacas; aparece em diferentes células normais e tumorais, embora algumas sejam melhores em se defender contra a sobrecarga de zinco do que outras. Essas percepções sugerem que os pequenos “portões” transportadores de zinco nas membranas celulares podem ser alvos promissores para drogas — seja para proteger tecidos saudáveis de danos relacionados ao zinco ou para empurrar células tumorais vulneráveis rumo à morte. Embora os achados venham de experimentos em cultura celular, eles oferecem uma nova lente sobre como um nutriente cotidiano pode moldar a atividade gênica e a doença quando seu delicado equilíbrio é perturbado.
Citação: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Palavras-chave: homeostase do zinco, regulação gênica, acetilação de histonas, autofagia, células cancerígenas