Clear Sky Science · pt
Reprogramação metabólica aumenta a resistência ao estresse oxidativo em cardiomiócitos em diferenciação
Por que a luta das células cardíacas contra o oxigênio importa
Cada batida do seu coração depende de células musculares especializadas chamadas cardiomiócitos. À medida que crescemos, essas células enfrentam uma mudança de vida dramática: passam de um ambiente intrauterino com baixo oxigênio e metabolismo baseado em açúcar para um mundo rico em oxigênio após o nascimento. O oxigênio é vital, mas também gera subprodutos nocivos que podem danificar o DNA e matar células. Este estudo investiga como as células cardíacas em maturação reprogramam seu metabolismo para lidar com mais oxigênio, gerar mais energia e ainda assim se proteger do dano oxidativo — percepções que podem orientar tratamentos futuros para doenças do coração e estratégias de regeneração.
De construtores simples a atletas de alta performance
As células cardíacas imaturas, conhecidas como cardiomioblastos, são células pequenas e em divisão que dependem principalmente da degradação da glicose para obter energia. Ao se diferenciarem em cardiomiócitos maduros, elas deixam de proliferar e aumentam de tamanho, muitas vezes se fundindo em células polinucleadas e alongadas mais adequadas para contrações potentes. Usando microscopia de alta resolução, os pesquisadores observaram essa transformação ao longo de dez dias em um modelo celular de laboratório. Marcadores de proliferação celular caíram, enquanto as células se alongaram e se reorganizaram em estruturas fibrosas semelhantes ao tecido cardíaco, confirmando que haviam entrado em um estado mais adulto e contrátil. 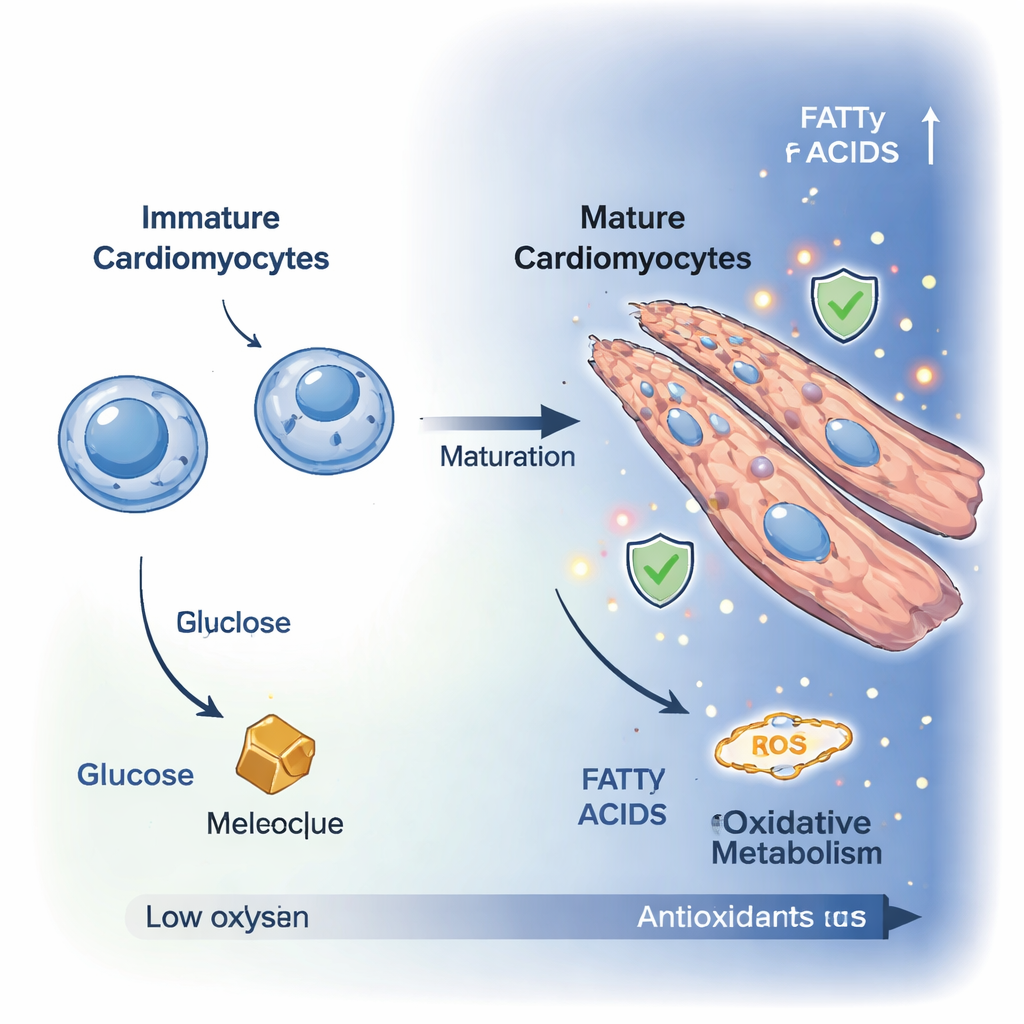
Trocando fontes de combustível e conectando novas rotas energéticas
Para entender o que acontece por dentro, a equipe mediu centenas de pequenas moléculas dentro das células e usou imagens avançadas da fluorescência natural celular para acompanhar o uso de energia em tempo real. Em conjunto, essas técnicas mostraram uma mudança clara de um estado glicolítico, em que as células queimam principalmente glicose, para um estado oxidativo dominado pela respiração mitocondrial. Níveis de glicose e frutose caíram, enquanto intermediários do ciclo do ácido tricarboxílico (TCA) — como ácido cítrico, malato e oxoglutarato — aumentaram. A análise de vias revelou maior atividade em rotas que alimentam combustível para as mitocôndrias, incluindo o shuttle malato–aspártato e a degradação de aminoácidos, indicando que os cardiomiócitos maduros ampliam suas opções de combustível e canalizam a energia de forma mais eficiente para suas “usinas”.
Vivendo com mais oxigênio — e mais estresse
Queimar combustível de forma mais eficiente nas mitocôndrias tem um custo: maior produção de espécies reativas de oxigênio (ROS), moléculas quimicamente agressivas que podem danificar lipídios, proteínas e DNA. Os pesquisadores observaram que, à medida que os cardiomiócitos amadureciam, suas mitocôndrias se tornavam maiores e mais alongadas, e marcadores de estresse oxidativo aumentaram. A imagem por fluorescência revelou mais grânulos semelhantes a lipofuscina, uma marca de lipídios oxidados, e uma sonda nuclear mostrou níveis mais altos de ROS nas células diferenciadas. A metabolômica indicou alterações no metabolismo do glutationa, um sistema antioxidante central que usa a molécula glutationa — sintetizada a partir de aminoácidos como glutamato e glicina — para neutralizar ROS. Esses achados sugerem que, à medida que as células cardíacas aumentam o metabolismo oxidativo, elas também ajustam suas vias antioxidantes para manter o dano sob controle. 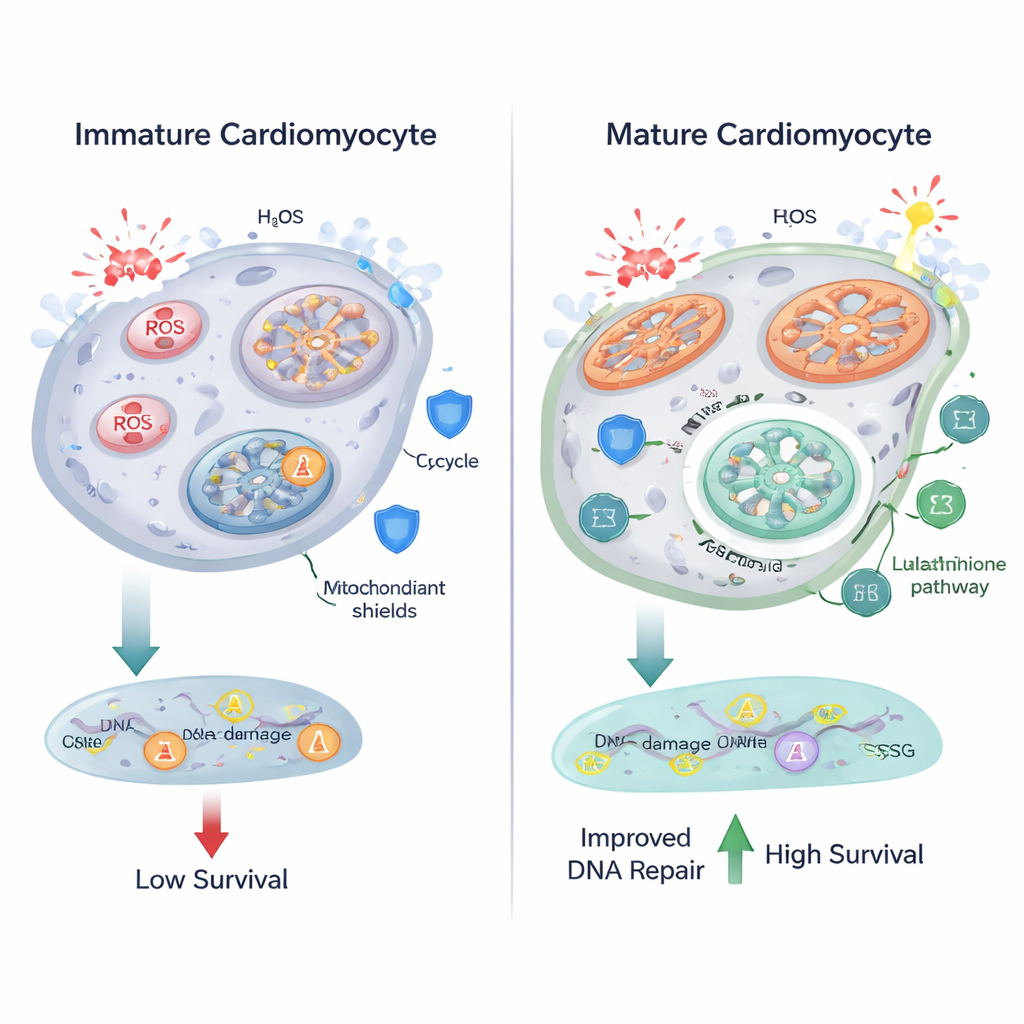
Dano contido, defesas reforçadas
Surpreendentemente, apesar do aumento de ROS, os cardiomiócitos diferenciados não apresentaram mais quebras de DNA do que seus equivalentes imaturos quando medidas por focos de γ-H2AX, um marcador sensível de dano ao DNA. Quando a equipe desafiou as células com peróxido de hidrogênio, um forte agente oxidante, tanto as células imaturas quanto as maduras acumularam ROS e quebras de DNA — mas as células maduras se saíram melhor. Elas exibiram proporcionalmente menos lesões de DNA em relação aos seus níveis mais altos de ROS, foram menos propensas a ativar sinais ligados à morte celular, como PUMA, e mostraram taxas de sobrevivência marcadamente maiores. Esses resultados indicam que os cardiomiócitos em maturação não apenas ajustam seu metabolismo, mas também aprimoram seus mecanismos de reparo de DNA e de sobrevivência, permitindo-lhes resistir a condições oxidativas mais severas.
O que isso significa para proteger o coração
Em termos simples, este estudo mostra que, ao amadurecer, as células cardíacas aprendem a funcionar com mais intensidade sem se autodestruir. Elas mudam de um estilo de vida rico em açúcar e com baixo oxigênio para um modo intensivo em oxigênio e movido por mitocôndrias, e ao mesmo tempo constroem melhores escudos e equipes de reparo para lidar com o estresse oxidativo. Compreender esse equilíbrio finamente ajustado entre produção de energia e autoproteção pode ajudar cientistas a projetar estratégias para tornar o tecido cardíaco adulto danificado mais resiliente, ou para guiar células-tronco rumo a cardiomiócitos mais seguros e duráveis para terapias regenerativas.
Citação: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Palavras-chave: diferenciação de cardiomiócitos, estresse oxidativo, mitocôndrias, metabolismo celular, doença cardíaca