Clear Sky Science · pt
Previsão da doença de Alzheimer usando aprendizado profundo e seleção de características interpretável baseada em XAI a partir de dados de expressão gênica sanguínea
Por que esta pesquisa é importante
A doença de Alzheimer rouba lentamente a memória e a independência das pessoas; ainda assim, os testes mais precisos de hoje frequentemente exigem exames cerebrais ou punções lombares que são caros, invasivos e de difícil repetição. Este estudo explora uma alternativa menos penosa: usar uma simples coleta de sangue e análise computacional avançada para identificar padrões na atividade gênica que sinalizam Alzheimer, potencialmente abrindo caminho para um diagnóstico mais precoce e acessível.
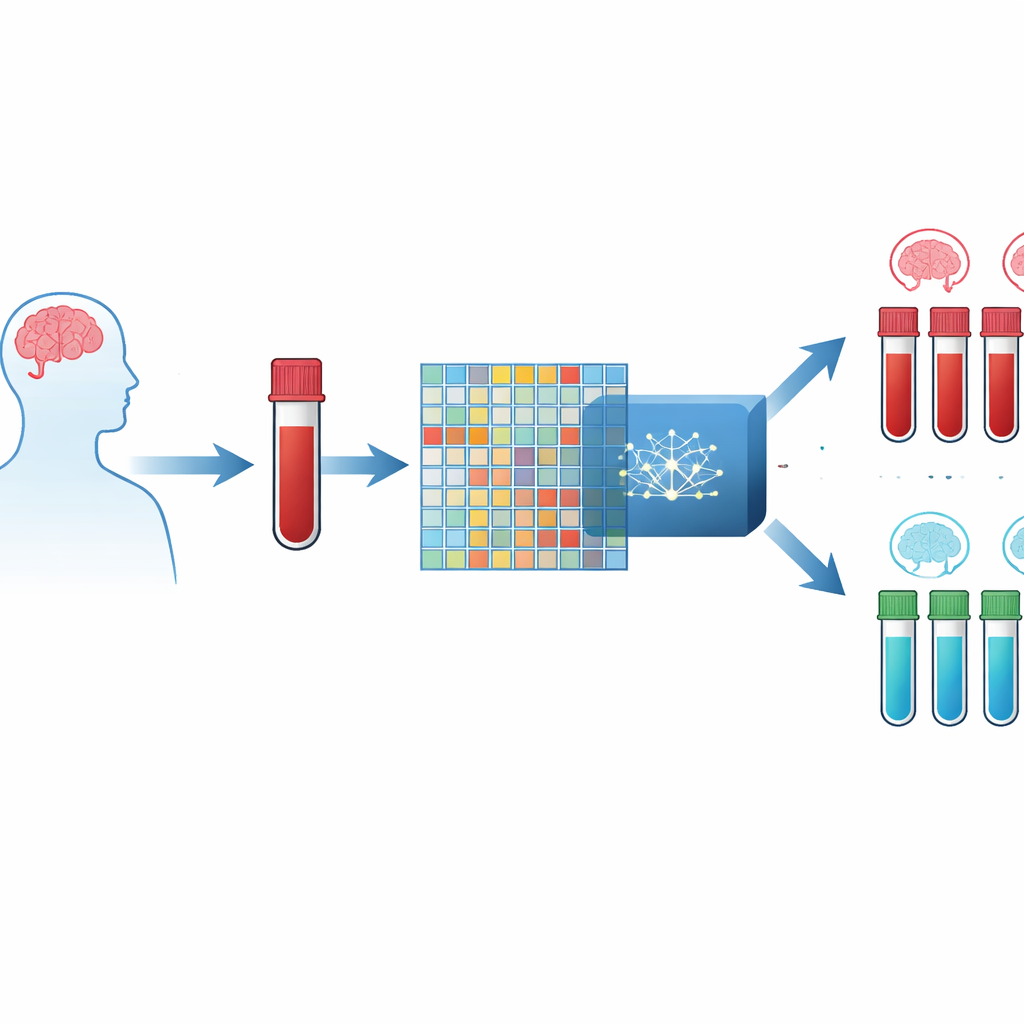
Um exame de sangue em vez de uma varredura cerebral
Os autores se concentram em pequenas alterações em como os genes são ativados ou desativados nas células sanguíneas. Chips laboratoriais modernos podem medir a atividade de milhares de genes de uma só vez, produzindo uma enorme tabela de números para cada pessoa. O desafio é que há muito mais medidas gênicas do que pacientes, o que pode facilmente induzir modelos computacionais em erro. Para contornar isso, os pesquisadores combinaram três grandes conjuntos de dados públicos de amostras de sangue de pessoas com Alzheimer e de voluntários saudáveis, criando um recurso integrado com mais de doze mil genes em comum medidos em centenas de indivíduos.
Ensinando computadores a identificar sinais de alerta chave
Em vez de pedir a um algoritmo que processe todas as doze mil genes, a equipe primeiro o ensinou a selecionar um conjunto muito menor de genes especialmente informativos. Eles compararam várias formas de fazer isso, incluindo testes estatísticos simples, métodos que removem genes menos úteis passo a passo e abordagens que incorporam a seleção diretamente no modelo. Essas ferramentas de “seleção de características” reduzirem a lista para centenas ou pouco mais de mil genes que melhor distinguiam pacientes de controles saudáveis. Os conjuntos gênicos reduzidos ajudaram a evitar que os modelos memorizassem ruído e melhoraram seu desempenho em dados não vistos.
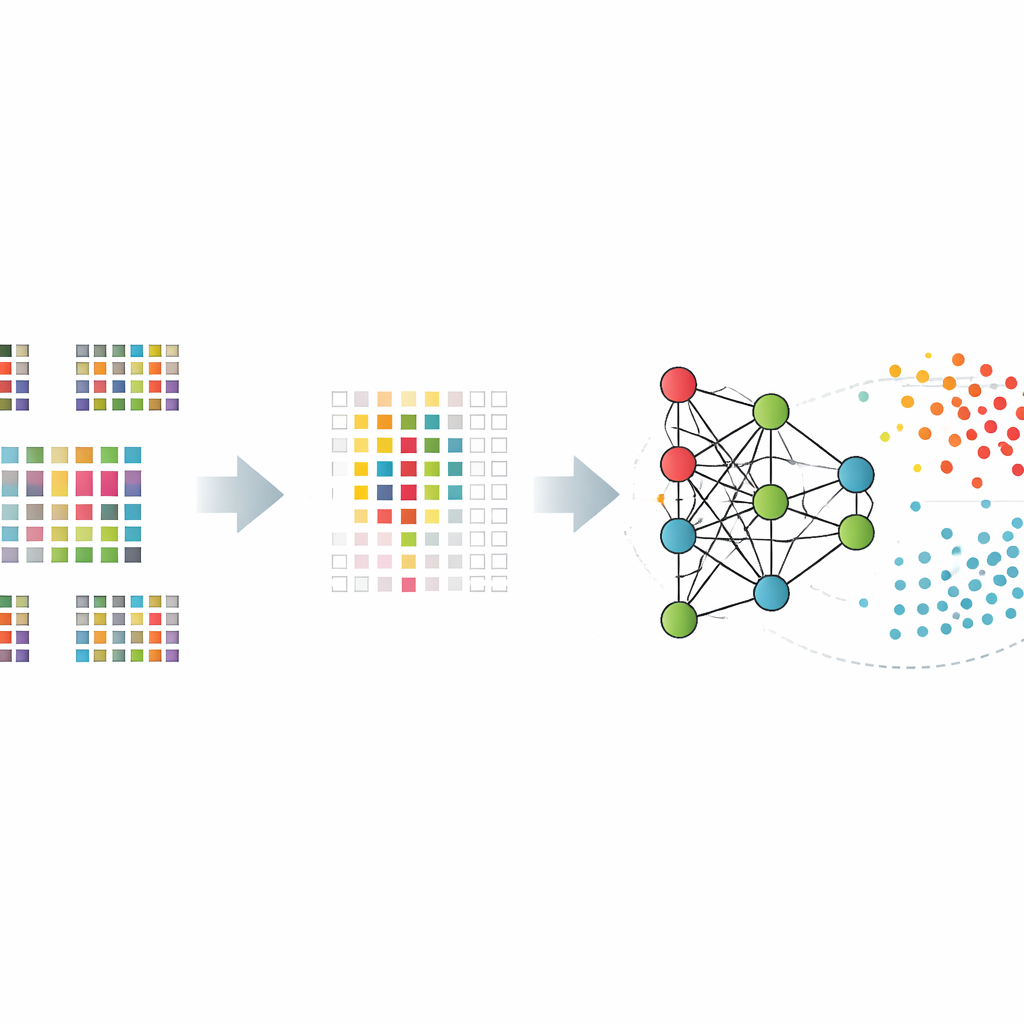
Dando sentido a uma caixa-preta
Para evitar confiança cega numa predição de caixa-preta, os pesquisadores usaram técnicas de inteligência artificial explicável para entender quais genes eram mais importantes e como eles influenciavam cada decisão. Um método chamado SHAP, emprestado da teoria dos jogos, pontua a contribuição de cada gene para o resultado final de cada pessoa. Ao aplicá-lo aos seus modelos de melhor desempenho, os autores destacaram um grupo central de genes cujos padrões de atividade consistentemente inclinavam a balança para uma classificação de Alzheimer ou saudável. Muitos desses genes já haviam sido ligados à saúde cerebral ou à função imune, conferindo credibilidade biológica ao funcionamento interno do modelo.
Potencializando com pacientes sintéticos
Mesmo após a fusão dos conjuntos de dados, o número de amostras sanguíneas reais permaneceu modesto. Para fortalecer seus modelos, os autores treinaram um tipo especializado de rede neural, conhecida como rede geradora adversarial, para criar perfis gênicos sintéticos realistas que se assemelham aos de pacientes reais. Essas amostras artificiais foram adicionadas apenas aos dados de treinamento, nunca aos dados de teste, de modo que as verificações de desempenho permanecessem honestas. Com esse conjunto de treinamento aumentado e genes escolhidos com cuidado, uma rede neural profunda foi capaz de identificar casos de Alzheimer com cerca de 91% de acurácia geral e 95% de precisão, o que significa que pouquíssimas pessoas saudáveis foram incorretamente sinalizadas como portadoras da doença.
O que os achados significam para os pacientes
Este trabalho sugere que um futuro teste sanguíneo para Alzheimer, impulsionado por algoritmos inteligentes que tanto selecionam quanto explicam sinais gênicos-chave, poderia complementar ou até reduzir a dependência de exames caros e procedimentos invasivos. Embora sejam necessárias mais validações em grupos independentes de pacientes, e as diferenças entre métodos laboratoriais precisem ser melhor controladas, o estudo mostra que combinar múltiplos conjuntos de dados, eliminar informações pouco úteis e abrir a “caixa-preta” da IA pode nos aproximar de um teste sanguíneo prático e interpretável para detecção mais precoce e confortável do Alzheimer.
Citação: Hariharan, J., Jothi, R. Alzheimer’s disease prediction using deep learning and XAI based interpretable feature selection from blood gene expression data. Sci Rep 16, 8022 (2026). https://doi.org/10.1038/s41598-026-35260-8
Palavras-chave: diagnóstico da doença de Alzheimer, biomarcadores sanguíneos, expressão gênica, aprendizado profundo, IA explicável