Clear Sky Science · pt
A desglucosilação induz uma nova conformação distal no receptor de manose CD206
Por que as coberturas açucaradas em sensores imunes são importantes
Nossas células imunes dependem de “antenas” moleculares para detectar ameaças, como micróbios e células cancerosas. Uma dessas antenas, chamada receptor de manose CD206, ajuda as células imunes a capturar moléculas decoradas com açúcares e até a localizar tumores. Como muitas proteínas, o CD206 é ele próprio coberto por pequenas cadeias de açúcar. Este estudo faz uma pergunta aparentemente simples, com grandes implicações: o que acontece com a forma e a função do CD206 quando esses açúcares são removidos?
Um braço flexível que lê sinais açucarados
O CD206 fica na superfície de certas células imunes, especialmente macrófagos que patrulham tecidos e tumores. Possui uma estrutura longa e articulada que se projeta a partir da membrana celular, terminando em vários segmentos “lectina” que reconhecem açúcares em moléculas em trânsito. O CD206 também pode ser liberado na corrente sanguínea, cujos níveis se correlacionam com doenças inflamatórias e fibróticas, tornando-o um possível marcador de enfermidade. A proteína é fortemente decorada com glicosilação N-ligada, e trabalhos anteriores mostraram que esses açúcares podem influenciar o quanto diferentes segmentos do receptor reconhecem açúcares. Muitos desses sítios de glicosilação estão distantes dos principais bolsões de ligação, sugerindo que podem agir mais como interruptores remotos do que simples bloqueadores.
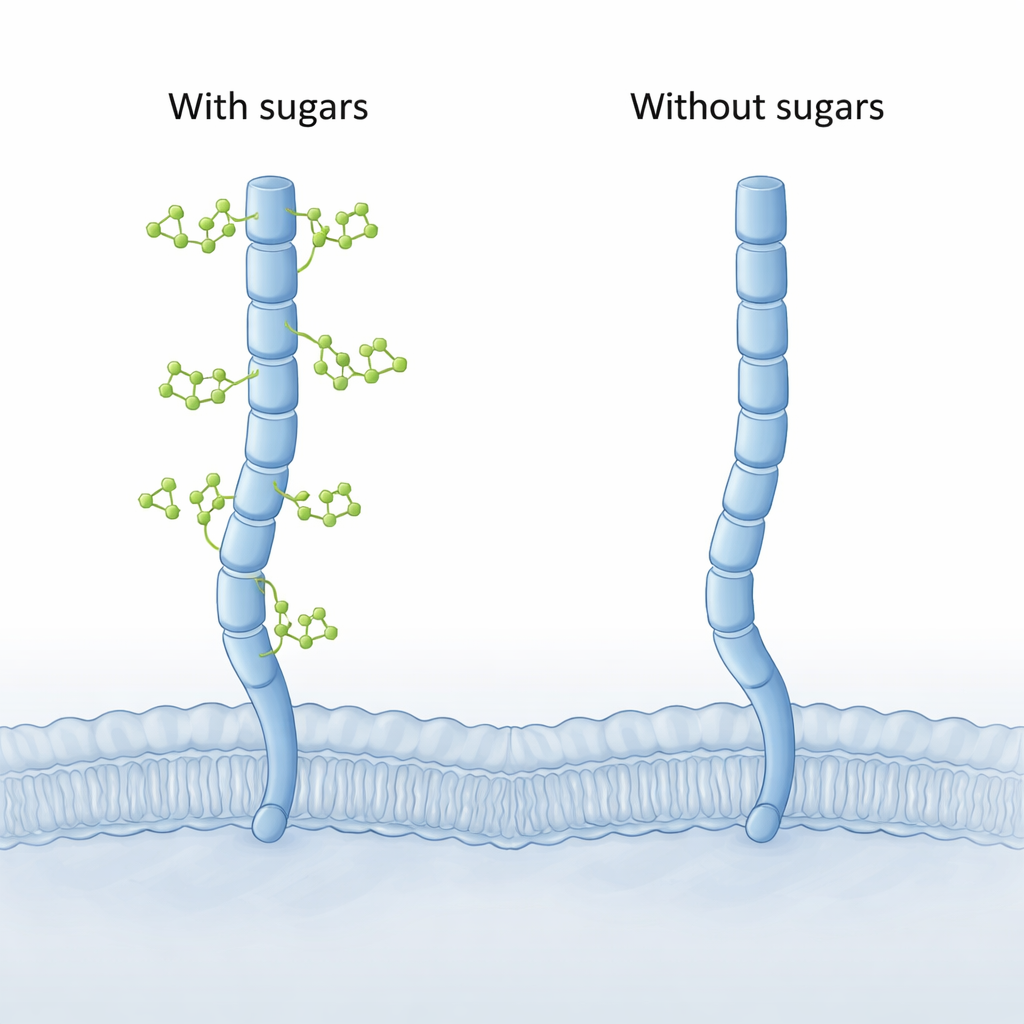
Modelos computacionais revelam uma curvatura oculta
Como a estrutura 3D completa do CD206 ainda não foi capturada experimentalmente, os autores recorreram a ferramentas computacionais modernas. Primeiro usaram o AlphaFold para construir modelos de comprimento total do receptor e, em seguida, realizaram simulações longas e detalhadas de dinâmica molecular do CD206 com e sem seus açúcares anexados. Ambas as versões comportaram-se como um braço molecular estendido, mas a forma “sem açúcar” exibiu um movimento novo e marcante em sua extremidade distal. Os dois últimos segmentos de lectina (chamados CTLD7 e CTLD8) puderam oscilar para dentro, formando uma ponta côncava e encurvada para dentro — uma geometria nunca observada na versão glicosilada, que permaneceu mais curvada para fora, ou convexa.
Como uma pequena mudança redesenha o movimento
Para entender essa diferença, a equipe analisou os movimentos dominantes em suas simulações. Constatou que o principal deslocamento que diferenciava as duas formas era essa flexão da ponta distal, presente apenas quando os açúcares estavam ausentes. A remoção dos açúcares tornou o receptor geralmente mais flexível, especialmente nos segmentos de lectina distais e, em menor grau, próximo à extremidade N-terminal. Mapas de correlação de como diferentes partes da proteína movem-se em conjunto mostraram que, sem açúcares, os dois últimos segmentos de lectina movem-se de forma mais concertada e estão mais fortemente acoplados a outras regiões. Em essência, os açúcares não ficam apenas na superfície; eles ajudam a ajustar como todo o braço se flexiona e se comunica ao longo de seu comprimento.
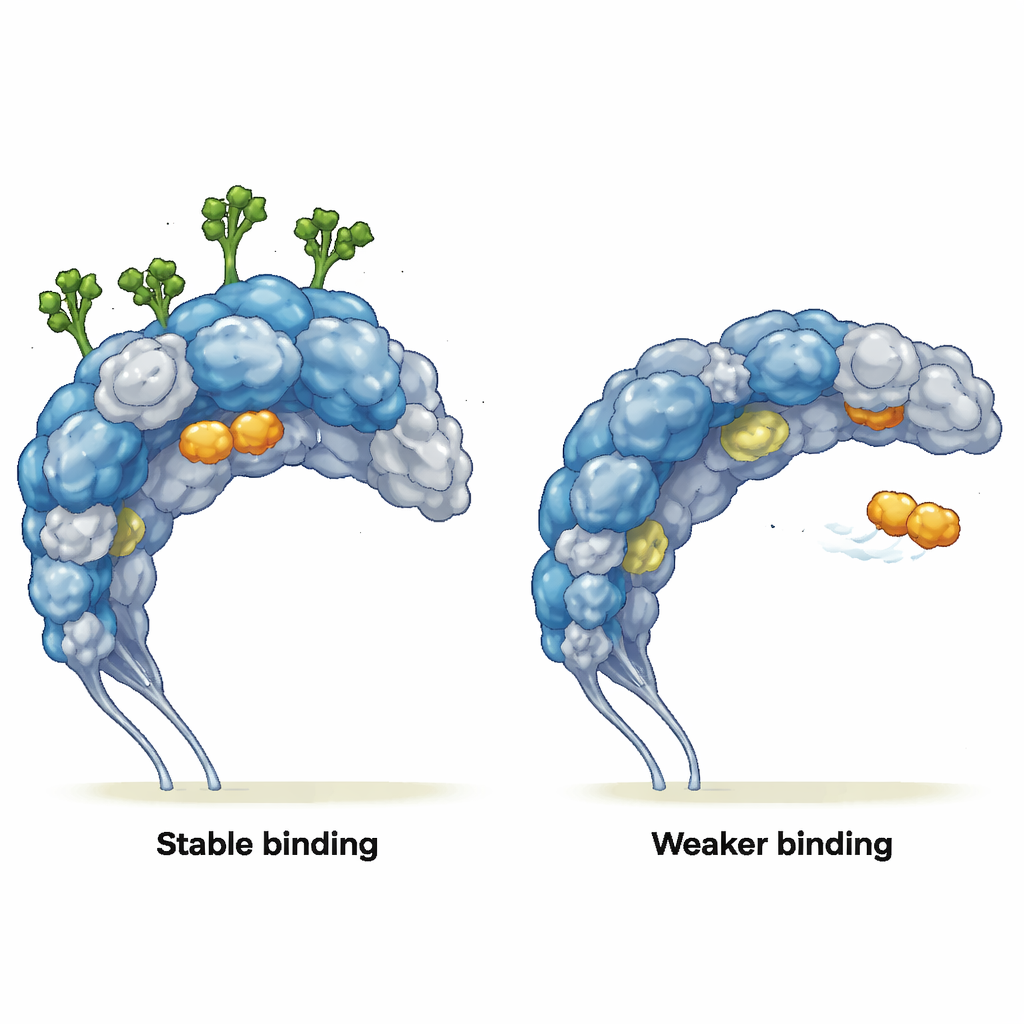
Mudando a forma como parceiros se ligam
Os autores então perguntaram como esse movimento alterado afeta parceiros de ligação reais. Simularam interações com dois ligantes: um açúcar simples semelhante à manose (MMA), que se encaixa em um bolso bem definido, e um peptídeo com afinidade tumoral chamado mUNO, que mira macrófagos associados a tumores positivos para CD206. Quando os açúcares estavam presentes, o MMA permaneceu firmemente em seu bolso de ligação durante toda a simulação, mantendo contatos-chave, embora a estrutura proteica circundante mal se alterasse. Sem os açúcares, o MMA escapou do bolso, deslizando pela superfície da proteína e formando apenas contatos breves e superficiais. Para o mUNO, o receptor glicosilado exibiu várias poses de ligação estáveis com contatos frequentes e duradouros. No receptor deglicosilado, a ligação do mUNO foi mais fraca e mais dispersa, e ele também começou a explorar regiões normalmente bloqueadas pelas cadeias de açúcar, revelando novos sítios de interação anteriormente ocultos.
O que isso significa para doença e terapia
Em conjunto, esses resultados mostram que os açúcares ligados ao CD206 atuam como reguladores remotos de sua forma e adesividade. Ao restringir certas flexões e organizar como seus segmentos se movem em conjunto, a glicosilação ajuda o receptor a reter alguns ligantes com maior firmeza e a direcionar outros para locais de acoplamento preferenciais, além de proteger partes de sua superfície. Em doenças como o câncer, onde os padrões gerais de glicosilação de proteínas frequentemente se alteram, o CD206 pode adotar formas e comportamentos de ligação diferentes, modificando como as células imunes percebem seu entorno. Compreender esse “interruptor conformacional” dependente de açúcares não apenas esclarece o funcionamento do CD206, mas também sugere novas maneiras de projetar fármacos ou agentes de imagem que explorem sua paisagem mutável em tumores e outras condições patológicas.
Citação: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Palavras-chave: receptor de manose, glicosilação de proteínas, reconhecimento imune, macrófagos associados a tumores, dINÂMICA molecular