Clear Sky Science · pt
Perda de Snhg5 perturba a regulação do ciclo celular sem alterar a cistogênese em um modelo murino de doença renal policística
Por que um gene renal com um nome estranho importa
A doença renal policística (DRP) é um distúrbio hereditário comum no qual inúmeros sacos cheios de líquido gradualmente invadem os rins, frequentemente levando à insuficiência renal. Os cientistas sabem que defeitos em dois genes, PKD1 e PKD2, impulsionam a doença, mas muitos outros fatores genéticos podem influenciar a rapidez com que ela progride. Este estudo foca em um tipo incomum de gene chamado RNA longo não codificante, denominado Snhg5, fazendo uma pergunta simples, porém importante: essa molécula molda de forma significativa o desenrolar da DRP, ou é em grande parte uma espectadora?
Um olhar mais atento para um mensageiro genético obscuro
Diferentemente dos genes típicos que fornecem plantas para proteínas, os RNAs longos não codificantes atuam mais como organizadores moleculares ou interruptores dentro das células. Trabalhos anteriores mostraram que Snhg5 está fortemente aumentado em modelos murinos de DRP e foi associado a vários tipos de câncer e lesões renais, sugerindo que poderia impulsionar um crescimento prejudicial. Os pesquisadores primeiro mapearam onde e quando o Snhg5 está ativo em camundongos normais. Eles descobriram que ele é ligado em muitos órgãos, com níveis especialmente altos no intestino, e que sua atividade no rim cai abruptamente após o nascimento, à medida que o órgão passa de crescimento rápido para um estado mais estável e maduro. Nas células renais, quase todas as moléculas de Snhg5 residem no núcleo, o centro de comando que abriga o DNA, sugerindo que Snhg5 ajuda a controlar a atividade gênica em vez de produzir proteínas diretamente.
Padrões em rins doentes não contam toda a história
A equipe então comparou os níveis de Snhg5 em uma variedade de modelos murinos de DRP. Em modelos de progressão rápida, onde os cistos se formam rapidamente, Snhg5 estava aumentado de duas a três vezes nos rins doentes, e imagens ao nível de célula única mostraram sinais nucleares fortes nas células que revestem os cistos e tecidos próximos. Surpreendentemente, quando examinaram um modelo murino mais lento e mais brando que imita melhor o curso longo da DRP humana, Snhg5 não aumentou. Ainda mais marcante, em tecido renal de pessoas com DRP autossômica dominante avançada, o equivalente humano do gene, chamado SNHG5, foi na verdade reduzido em mais de 90 por cento. Em conjunto, esses resultados sugerem que mudanças nesse RNA acompanham a formação de cistos, mas a direção e a temporalidade da alteração diferem entre espécies e estágios da doença, levantando dúvidas de que Snhg5 sozinho seja um motor direto do crescimento cístico.
O que acontece quando o gene é removido
Para ir além da correlação, os pesquisadores usaram edição genética CRISPR para deletar completamente o gene Snhg5 em camundongos, criando uma linhagem “knockout” global. Ao contrário das preocupações de que remover uma molécula tão fortemente alterada pudesse ser prejudicial, os camundongos sem Snhg5 nasceram em proporções normais, viveram vidas normais e tiveram rins que pareciam e funcionavam como os de seus irmãos saudáveis. Exame microscópico revelou estrutura renal normal sem fibrose ou inflamação, e exames sanguíneos não mostraram sinais de filtração renal comprometida. No nível molecular, entretanto, surgiram mudanças mais sutis: tanto rins de camundongo quanto células de túbulos renais cultivadas sem Snhg5 exibiram alterações consistentes na atividade de genes ligados à divisão celular e à replicação do DNA. Em cultura celular, mais células ficaram presas em estágios tardios do ciclo celular e em um estado danificado, sub-G1. Uma proteína em particular, ARPC5, parte de um complexo que ajuda as células a se dividir reorganizando seu arcabouço interno, foi reduzida quando Snhg5 estava ausente, sugerindo uma possível cadeia de causa e efeito.
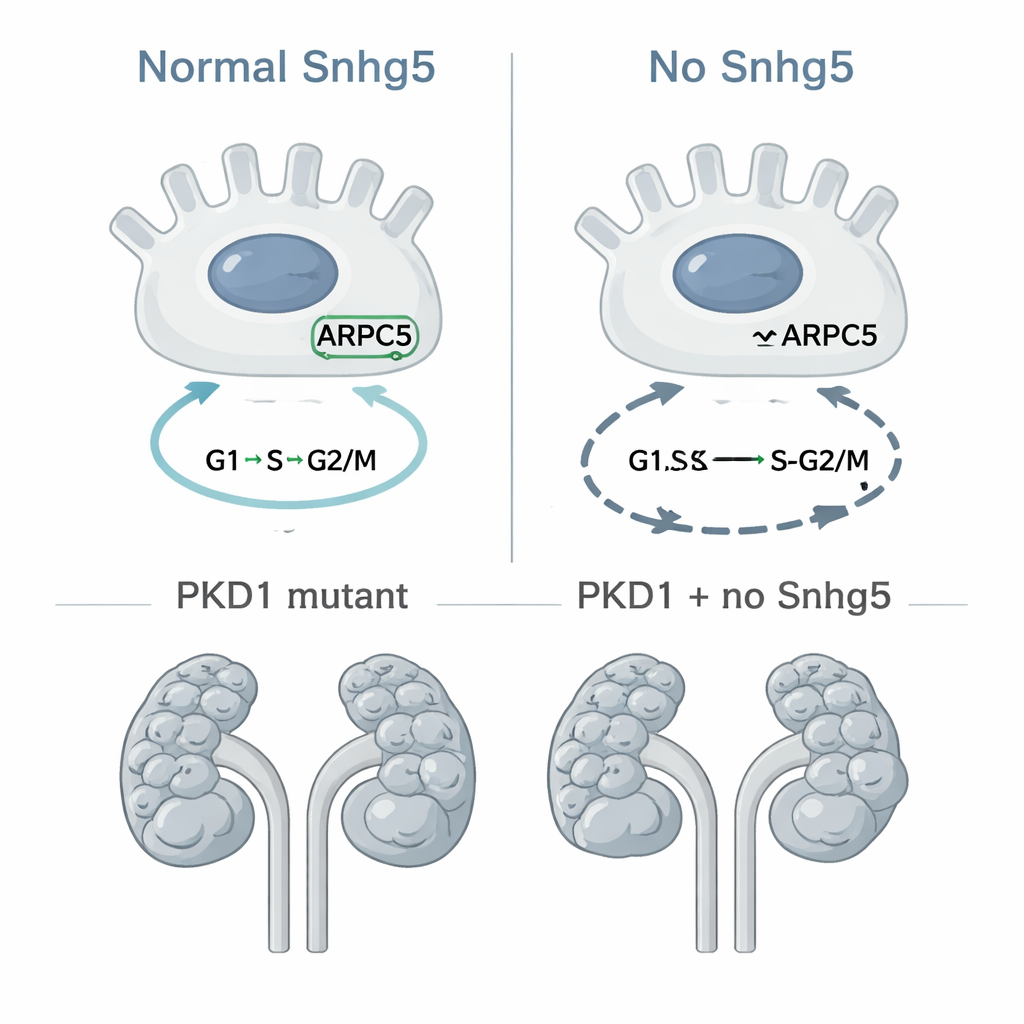
Testando seu papel no crescimento de cistos diretamente
Porque a divisão celular descontrolada é uma característica central da DRP, a equipe então perguntou se remover Snhg5 retardaria a formação de cistos em um modelo murino bem estabelecido no qual o gene PKD1 é desativado especificamente nas células do ducto coletor, fonte de muitos cistos. Eles cruzaram camundongos de modo que alguns tivessem apenas a mutação em PKD1, enquanto outros careciam tanto de PKD1 quanto de Snhg5. Quando examinaram os animais aos 10 dias de idade, ambos os grupos apresentaram rins severamente císticos, e medidas cuidadosas de tamanho renal, área cística e número de cistos não revelaram proteção significativa pela deleção de Snhg5. Se é que houve efeito, os camundongos duplos-mutantes tendiam a ter uma carga cística ligeiramente maior, embora a diferença fosse pequena e não estatisticamente convincente. Em outras palavras, embora Snhg5 influencie genes do ciclo celular em células renais, sua ausência não altera de forma perceptível a rapidez com que cistos aparecem ou crescem neste modelo específico de DRP.
O que isso significa para tratamentos futuros
Para pacientes e desenvolvedores de fármacos, a principal conclusão é que Snhg5, apesar de ser um dos sinais genéticos mais fortemente alterados na DRP murina, não é uma peça-chave da formação de cistos—pelo menos não na fase inicial e de crescimento rápido da doença proveniente do ducto coletor. O gene parece ajustar como as células renais progridem pelo ciclo de divisão, provavelmente por seu impacto em fatores como ARPC5, mas essa influência é sutil o suficiente para que sua perda completa deixe o desenvolvimento renal e a progressão inicial da DRP largamente inalterados. Esses achados destacam uma lição mais ampla: nem toda mudança molecular marcante em tecido doente é um alvo terapêutico promissor. Desvendar causa e consequência exigirá testar RNAs longos não codificantes como Snhg5 em vários modelos da doença e em diferentes pontos no tempo antes que possam ser perseguidos com confiança como candidatos a fármaco.
Citação: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Palavras-chave: doença renal policística, RNA longo não codificante, Snhg5, ciclo celular, cistos renais