Clear Sky Science · pt
Nanocápsulas de quitosana-dextran sulfato para aumentar a eficácia da tigeciclina contra Salmonella enterica não tifoide
Por que isso importa para a segurança alimentar
A maioria das pessoas conhece a Salmonella como uma causa desagradável de intoxicação alimentar, frequentemente associada a aves malcozidas. Menos sabem que algumas cepas tornaram-se tão resistentes a antibióticos que até fármacos poderosos de “último recurso” podem falhar. Este estudo investiga uma abordagem baseada em nanotecnologia para resgatar um desses medicamentos, a tigeciclina, encapsulando‑o em minúsculas cápsulas à base de açúcares que o ajudam a penetrar em células infectadas e a neutralizar mecanismos-chave de resistência na Salmonella.
A ameaça crescente de Salmonella resistente
Os sorovares de Salmonella não tifoide (NTS) são uma causa principal de diarreia e infecções na corrente sanguínea no mundo todo, especialmente em países de baixa e média renda. Os pesquisadores examinaram 12 cepas de Salmonella enterica isoladas de carne de frango e de pato no Egito. Essas cepas eram resistentes a muitos antibióticos comumente usados, incluindo penicilinas, cefalosporinas, tetraciclinas e outros, e exibiam altos índices de resistência múltipla. Mesmo a tigeciclina, um fármaco de amplo espectro reservado para casos difíceis, teve desempenho fraco: as bactérias toleravam concentrações muito altas do medicamento. Uma razão principal foi a superatividade de “bombas de efluxo” — máquinas moleculares na membrana bacteriana que expulsam constantemente os antibióticos para fora da célula.
Construindo uma cápsula de fármaco mais inteligente
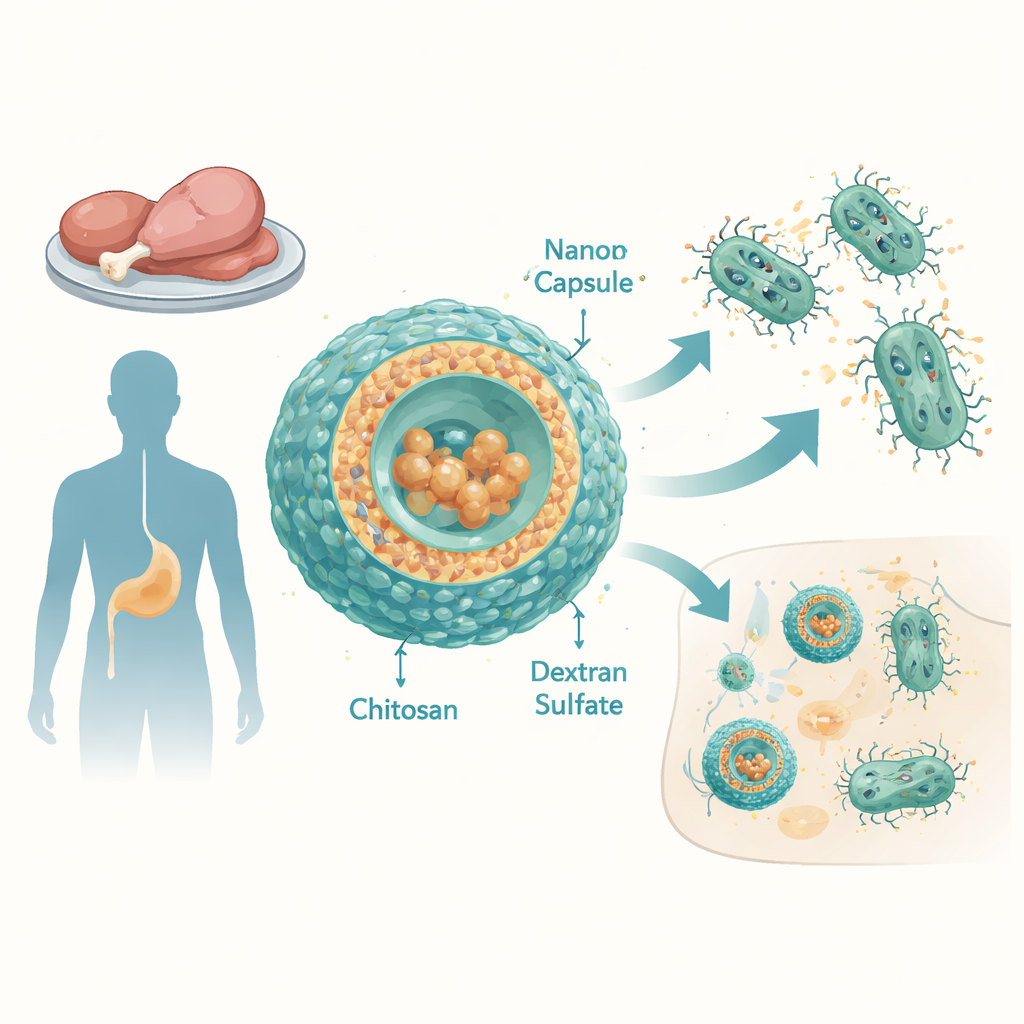
Para superar isso, a equipe projetou cápsulas em escala nanométrica feitas de dois polímeros de origem natural: quitosana, obtida da quitina (material presente em cascas de crustáceos), e dextran sulfato, uma molécula de açúcar ramificada. Ao ajustar cuidadosamente as proporções desses componentes, produziram partículas estáveis com cerca de 100–150 nanômetros de diâmetro, com carga superficial positiva que favorece a interação com membranas bacterianas e das células hospedeiras. A tigeciclina foi carregada nessas partículas com eficiência notavelmente alta — praticamente todo o fármaco ficou dentro das cápsulas. Em testes laboratoriais que mimetizam condições na corrente sanguínea, as cápsulas liberaram a maior parte da tigeciclina em poucas horas, sugerindo que podem fornecer um forte pulso de antibiótico nos locais de infecção.
Reduzindo as defesas bacterianas
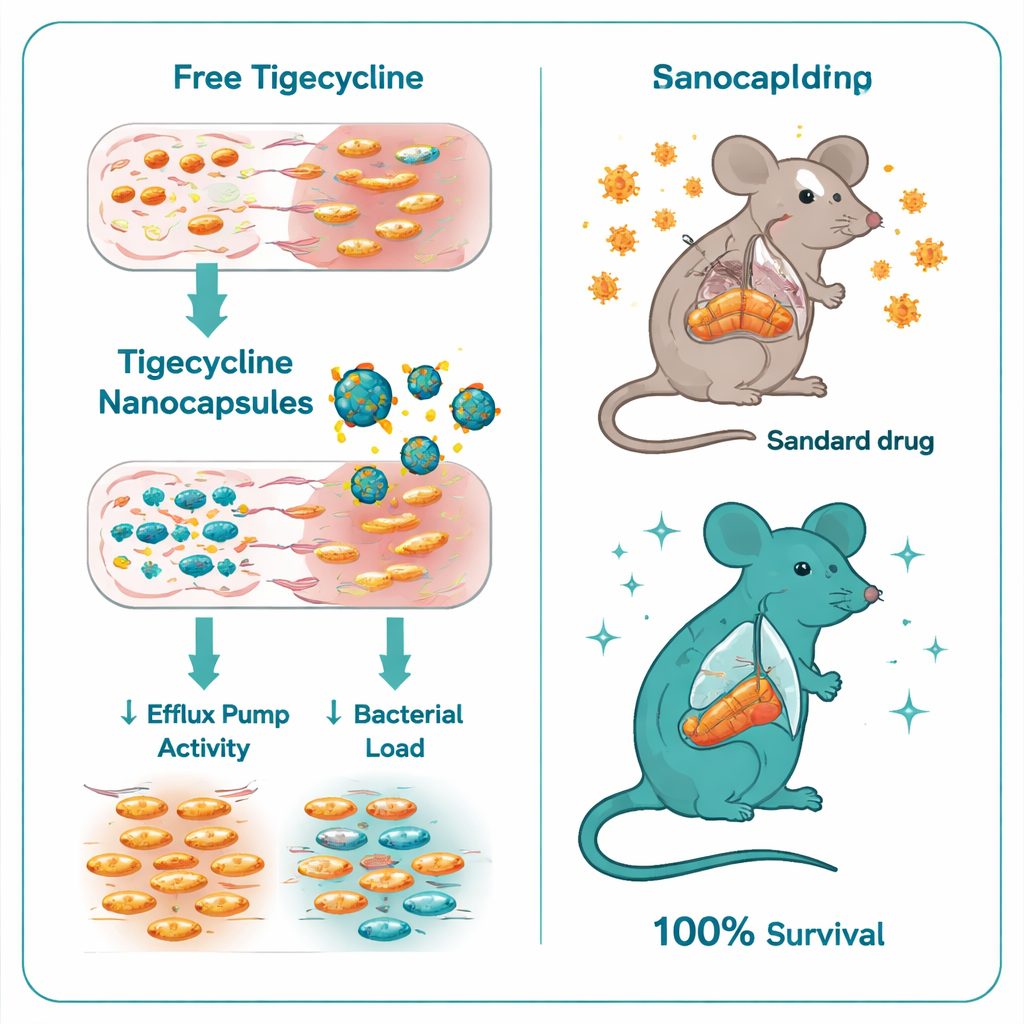
Quando os pesquisadores compararam a tigeciclina simples com a tigeciclina encapsulada nas nanocápsulas de quitosana–dextran sulfato, a diferença foi marcante. A concentração mínima do fármaco necessária para impedir o crescimento bacteriano caiu de 32–128 microgramas por mililitro para a tigeciclina simples para apenas 0,5–1 micrograma por mililitro com as nanocápsulas — uma melhoria de seis a sete vezes. Experimentos de tempo‑morte mostraram que a forma encapsulada matou a Salmonella muito mais rápida e completamente. Em nível genético, as nanocápsulas também reduziram a atividade de reguladores chave da resistência: a expressão dos genes ramA e acrB, que controlam e formam importantes bombas de efluxo, diminuiu várias vezes nas bactérias tratadas. Em outras palavras, as cápsulas não apenas entregaram mais fármaco; ajudaram a desligar uma das principais rotas de escape das bactérias.
Protegendo camundongos infectados de doença letal
A equipe então testou a nova formulação em um modelo de camundongo com infecção severa por Salmonella Typhimurium. Camundongos infectados e não tratados morreram todos em oito dias. Os que receberam tigeciclina padrão tiveram melhor desfecho, mas ainda alta mortalidade, com apenas 40% sobrevivendo. Em nítido contraste, todos os camundongos tratados com as nanocápsulas contendo tigeciclina sobreviveram. Esses animais apresentaram muito menos bactérias no fígado e nos intestinos, exames de sangue mais próximos da função normal do fígado e dos rins e danos teciduais muito mais leves na análise microscópica. Mesmo as cápsulas “vazias” de quitosana–dextran sulfato, sem antibiótico, ofereceram alguma proteção, provavelmente porque a quitosana tem efeitos antimicrobianos e anti‑inflamatórios modestos, mas a combinação com tigeciclina foi claramente superior.
O que isso pode significar para tratamentos futuros
Para não especialistas, a mensagem central é que encapsular um antibiótico existente em uma nanocápsula inteligente e biocompatível pode restaurar sua eficácia contra Salmonella altamente resistente. Ao ajudar o fármaco a alcançar bactérias que se escondem dentro de células e ao reduzir as bombas que normalmente expulsam o medicamento, o sistema quitosana–dextran sulfato transformou um antibiótico de último recurso em declínio em um tratamento altamente eficaz em camundongos, com 100% de sobrevivência. Embora sejam necessários mais estudos antes que essa abordagem possa ser usada em pessoas ou em animais de criação, ela oferece um caminho promissor para estender a vida útil de antibióticos importantes e melhorar a segurança do nosso abastecimento alimentar sem precisar inventar novos medicamentos do zero.
Citação: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Palavras-chave: Salmonella, resistência a antibióticos, nanopartículas, veiculação de fármacos, tigeciclina