Clear Sky Science · pt
Bactérias de alimentos e da microbiota intestinal produzem metilglioxal e esse metabólito leva à formação de alcaloides bioativos 1‑acetil‑β‑carbolina
Por que o laboratório químico do seu intestino importa
Dentro do nosso intestino e em muitos alimentos fermentados, trilhões de bactérias transformam constantemente os açúcares que ingerimos em uma série de subprodutos químicos. Este estudo explora em detalhe uma dessas vias: como algumas bactérias comuns convertem açúcares em um composto altamente reativo chamado metilglioxal, e depois em uma família de moléculas bioativas chamadas 1‑acetil‑β‑carbolinas. Como essas substâncias estão ligadas tanto a processos patológicos quanto a potenciais novos medicamentos, entender quando e como as bactérias as produzem pode remodelar nossa visão sobre alimento, microbioma e saúde.
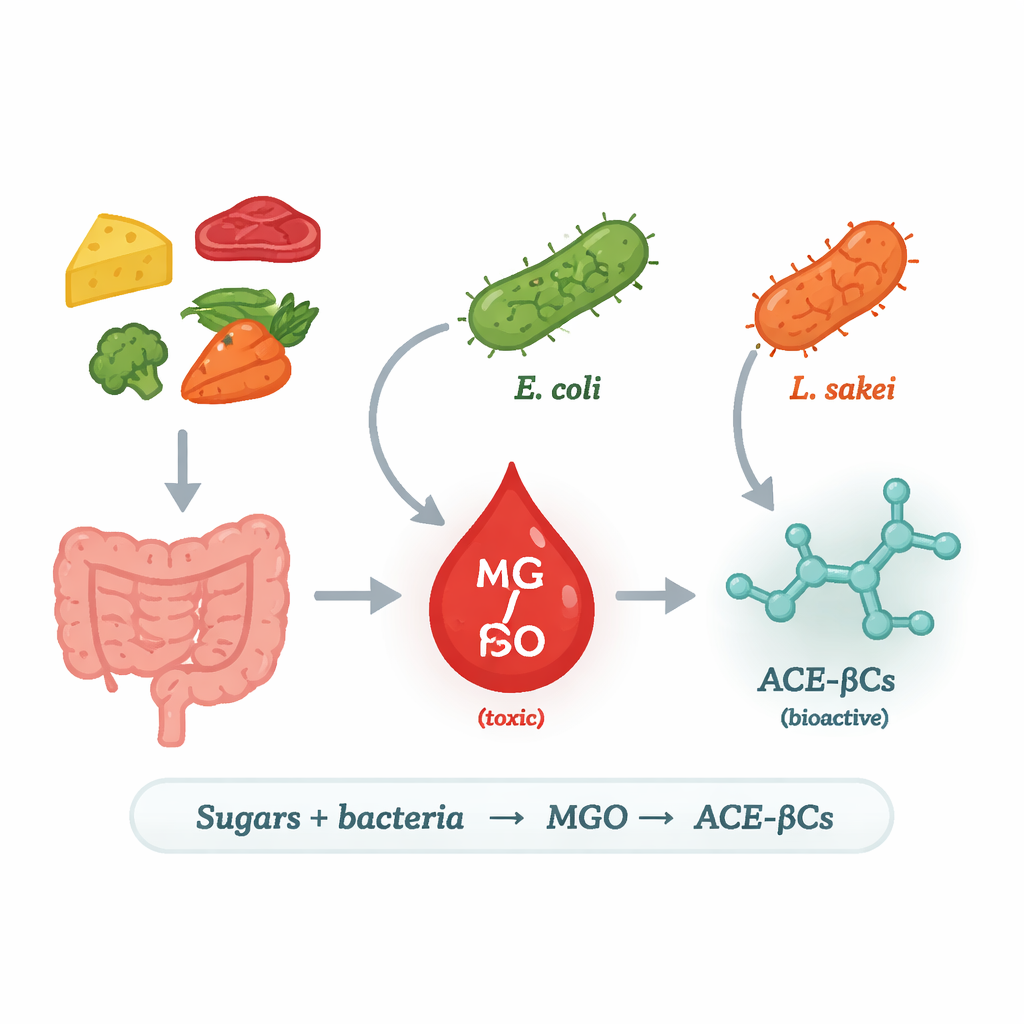
Dos açúcares cotidianos a uma molécula arriscada
Os pesquisadores focaram no metilglioxal (MGO), um subproduto muito reativo e tóxico da degradação de açúcares. Em humanos, excesso de MGO está associado a diabetes, doenças cardiovasculares e neurodegeneração porque pode danificar proteínas e DNA. Nossas células normalmente mantêm o MGO sob controle com sistemas de desintoxicação, mas elas não são a única fonte: bactérias também podem produzir MGO. Em alguns micróbios, uma enzima chamada metilglioxal sintetase (MgsA) converte um intermediário do processamento de açúcar diretamente em MGO, criando um “atalho” no metabolismo energético. A equipe investigou quais bactérias de alimentos e do intestino usam essa rota, em que condições, e o que acontece com o MGO que liberam.
Quem são os produtores bacterianos?
Para responder, os cientistas cultivaram várias linhagens de bactérias do ácido lático frequentemente encontradas em alimentos, junto com uma linhagem laboratorial de Escherichia coli, em um meio controlado contendo glicose ou galactose. Em seguida, acompanharam o MGO e dois alcaloides relacionados no líquido de cultura ao longo do tempo usando cromatografia e espectrometria de massa de alta precisão. Apenas E. coli e a espécie associada a carnes Lactilactobacillus sakei produziram quantidades notáveis de MGO e dos alcaloides; outras bactérias do ácido lático testadas não o fizeram. Uma busca genômica revelou a diferença chave: E. coli e L. sakei carregam o gene para MgsA, enquanto a maioria de suas parentes do ácido lático não. Quando os pesquisadores inseriram o gene mgsA de L. sakei em uma linhagem não produtora, essa bactéria modificada começou a produzir tanto MGO quanto os alcaloides, ligando de forma sólida a MgsA a essa via.
Como o MGO tóxico se torna alcaloides bioativos
A próxima pergunta foi o que acontece com o MGO depois de formado. A equipe concentrou‑se nos alcaloides 1‑acetil‑β‑carbolina (ACE‑βCs), moléculas pequenas com atividades relatadas antimicrobianas, anti‑inflamatórias e anticâncer. Demonstraram que quando bactérias produtoras de MGO foram cultivadas na presença do aminoácido L‑triptófano, os níveis de dois ACE‑βCs — 1‑acetil‑β‑carbolina e sua forma ácido‑3‑carboxílica — aumentaram acentuadamente. Adicionar MGO extra ao meio também elevou sua formação. Isso indica que o MGO vaza das células e reage espontaneamente com L‑triptófano no líquido circundante, sem enzimas adicionais, para gerar esses compostos bioativos. Em outras palavras, a mesma química que torna o MGO perigoso também o converte em moléculas mais complexas que podem ter efeitos úteis.
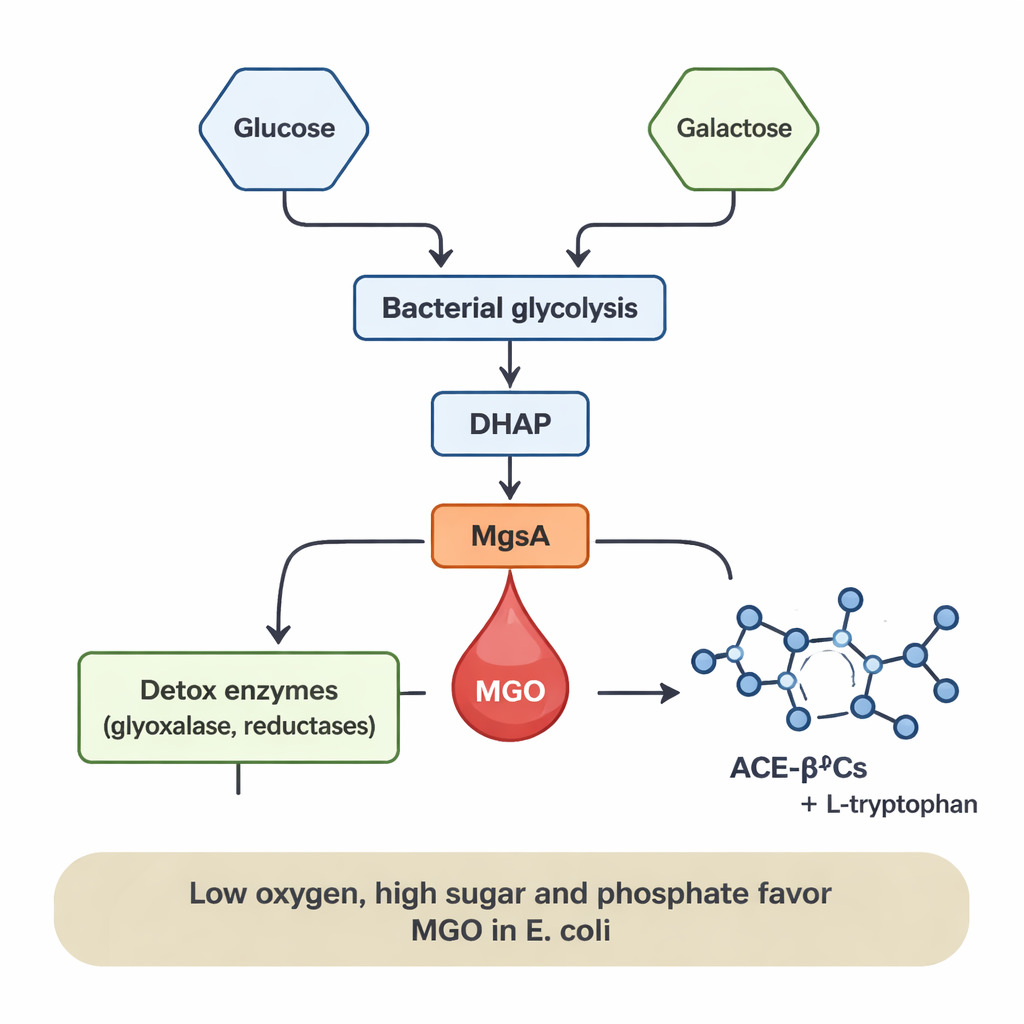
O que ajusta o nível dessa produção
A produção de MGO não era fixa; dependia fortemente da dieta e do ambiente das bactérias. Em E. coli, o MGO apareceu somente quando havia glicose presente, e seus níveis subiram conforme a concentração de glicose aumentava. Adicionar fosfato, um nutriente mineral comum, amplificou ainda mais a formação de MGO por vários vezes, provavelmente porque favorece o acúmulo de intermediários de açúcar fosforilados que alimentam o atalho da MgsA. Condições de baixo oxigênio (anaeróbicas) — semelhantes às do intestino humano — também favoreceram a liberação de MGO, enquanto condições ricas em oxigênio e bem aeradas a reduziram drasticamente, embora as bactérias ainda crescessem bem. Em contraste, L. sakei gerou principalmente MGO quando cultivada em galactose, e a produção aumentou com níveis mais altos de galactose. Esses padrões sugerem que sempre que o fluxo de açúcar pelo metabolismo bacteriano é alto e o oxigênio é limitado, o MGO pode atuar como uma “válvula de alívio”, reduzindo a pressão do acúmulo de intermediários de açúcar.
O que isso pode significar para alimentos e saúde
Os achados sugerem que nem todas as bactérias do intestino ou de alimentos são iguais em sua capacidade de produzir MGO e ACE‑βCs. Espécies que possuem a enzima MgsA, como certas linhagens de L. sakei e E. coli, podem ser contribuidoras significativas, especialmente em ambientes ricos em açúcar e com baixo oxigênio, como o intestino ou algumas fermentações. O MGO que excretam pode aumentar a carga química sobre os tecidos hospedeiros, mas sua conversão em alcaloides ACE‑βC pode também, em parte, “absorver” esse composto reativo ao gerar moléculas com seus próprios efeitos biológicos. Embora este estudo tenha sido realizado em culturas de laboratório, ele destaca uma rota plausível pela qual dieta, composição da microbiota e metabolismo bacteriano em conjunto moldam o equilíbrio entre químicos nocivos e potencialmente benéficos em nossos corpos, e aponta os ACE‑βCs como possíveis marcadores da produção bacteriana de MGO em alimentos e no intestino.
Citação: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Palavras-chave: microbiota intestinal, metilglioxal, metabolismo bacteriano, fermentação de alimentos, alcaloides beta‑carbolina