Clear Sky Science · pt
Modelos compactos de deep learning para histopatologia do cólon com foco em desempenho e desafios de generalização
Por que esta pesquisa importa para pacientes e médicos
O câncer de cólon está entre os tipos mais letais do mundo, e seu diagnóstico ainda depende de especialistas examinando cuidadosamente imagens microscópicas de tecido — uma tarefa lenta e sujeita a discordâncias. Este estudo investiga se modelos de inteligência artificial (IA) muito pequenos e eficientes podem ajudar a identificar tecido canceroso do cólon com precisão suficiente para ser útil em clínicas do dia a dia, inclusive em locais com capacidade computacional limitada. O trabalho também revela uma fraqueza escondida: modelos que parecem quase perfeitos durante o desenvolvimento podem falhar seriamente quando confrontados com dados novos do mundo real.
Ensinando computadores a ler imagens de microscópio
Quando se coleta uma biópsia de cólon, patologistas examinam lâminas finas e coradas ao microscópio. Tecidos cancerosos exibem glândulas distorcidas, formatos celulares irregulares e invasão de estruturas vizinhas, enquanto tecido saudável apresenta padrões ordenados e regulares. Os autores usaram uma coleção pública de 24.000 imagens digitais dessas lâminas, divididas igualmente entre câncer (adenocarcinoma de cólon) e tecido benigno. Todas as imagens foram redimensionadas para um formato pequeno padrão e sofreram ajustes realistas — pequenas rotações, espelhamentos, zooms e alterações suaves de cor — para reproduzir a variação natural na forma como lâminas são cortadas, coradas e digitalizadas. Essa preparação cuidadosa ajuda os modelos de IA a focarem em padrões teciduais relevantes em vez de detalhes superficiais, como orientação exata ou brilho.
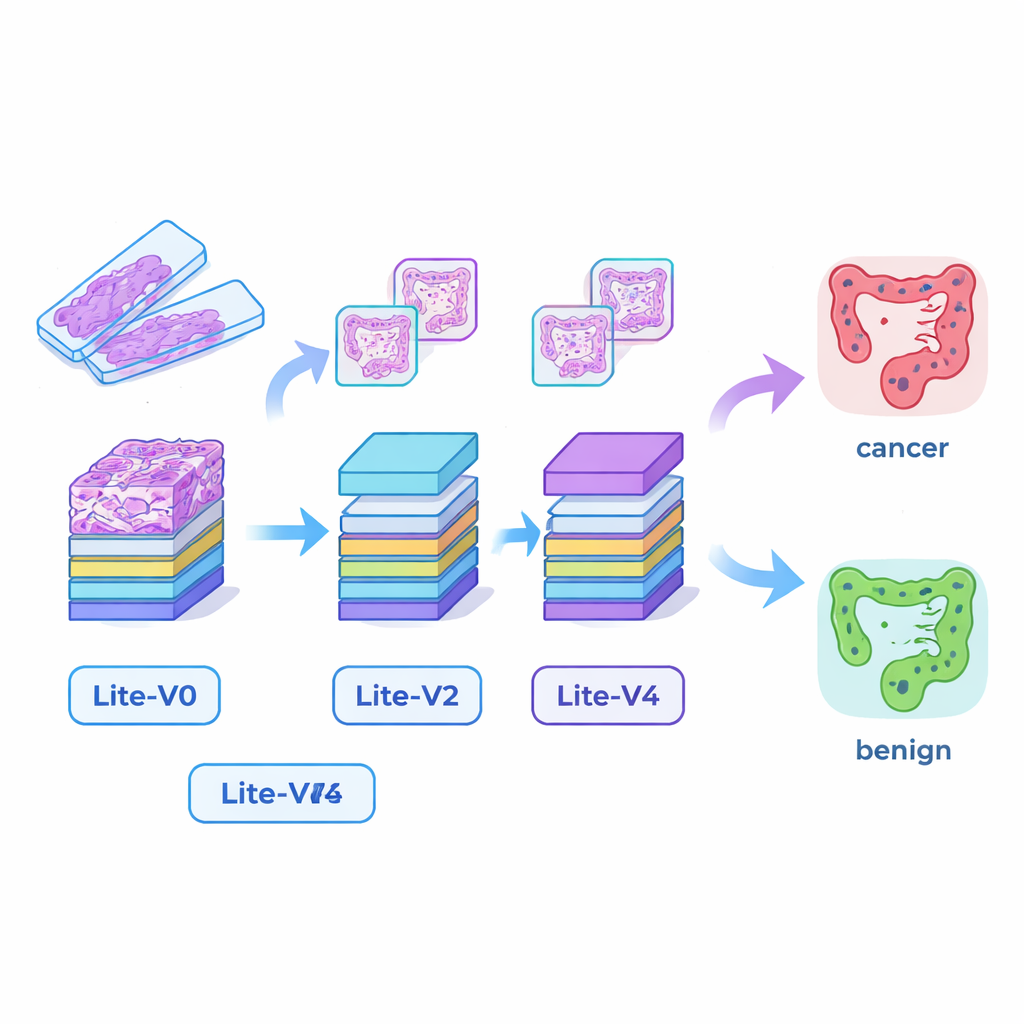
Construindo "olhos" de IA pequenos, mas capazes
Muitos sistemas de IA médica bem‑sucedidos dependem de modelos de deep learning muito grandes que exigem placas gráficas potentes e muita memória, dificultando a implantação em hospitais menores ou à beira do leito. Para reduzir essa barreira, os pesquisadores projetaram quatro redes neurais convolucionais compactas — Lite‑V0, Lite‑V1, Lite‑V2 e Lite‑V4. Cada uma analisa os mesmos fragmentos de imagem, mas diferem no número de camadas e filtros usados para detectar características visuais como bordas, texturas e formas de glândulas. As quatro compartilham um desenho simples e transparente: blocos repetidos de convolução padrão, normalização e pooling, seguidos por uma pequena "cabeça de decisão" que fornece a probabilidade de tecido ser canceroso ou benigno. O objetivo foi avaliar quanta precisão é possível extrair de modelos pequenos o suficiente para rodar confortavelmente em hardware clínico básico.
Resultados impressionantes em ambiente de laboratório
A equipe treinou e comparou os quatro modelos em uma divisão fixa do conjunto de dados, usando medidas amplamente aceitas: acurácia, F1‑score balanceado (macro) que pondera igualmente erros em ambas as classes, matrizes de confusão e gráficos diagnósticos como curvas ROC e precisão‑recall. Um modelo de porte médio, o Lite‑V2, destacou‑se como o melhor desempenho. Apesar de ter apenas cerca de 1,5 megabytes e aproximadamente 128.000 parâmetros treináveis, ele alcançou desempenho quase perfeito no conjunto de validação interno, com F1‑score macro em torno de 0,999 e sensibilidade e especificidade quase perfeitas. Em outras palavras, dentro desse ambiente cuidadosamente preparado, o Lite‑V2 conseguia quase sempre distinguir tecido canceroso de benigno no cólon, mantendo-se rápido e leve o suficiente para uso em computadores modestos.
Quando a variação do mundo real quebra a magia
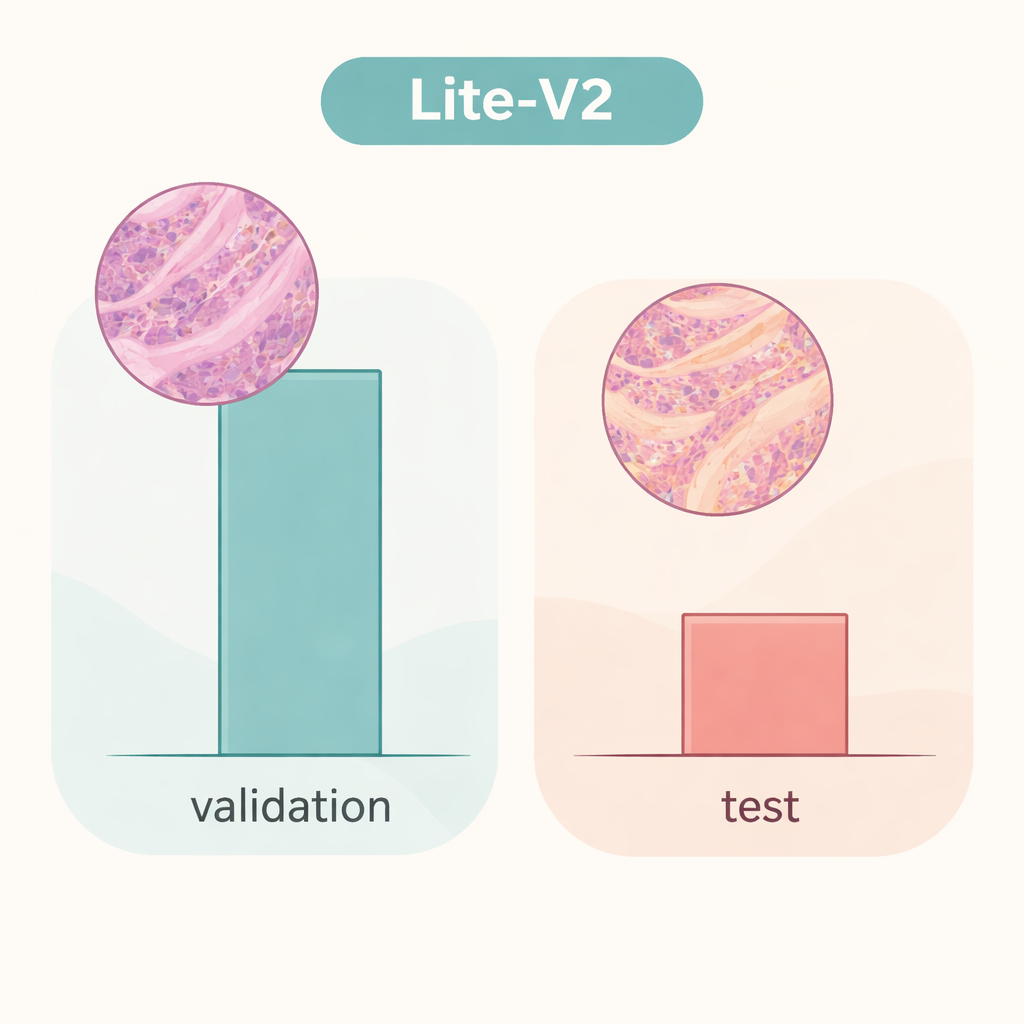
Entretanto, a história muda drasticamente quando o mesmo modelo Lite‑V2 é testado em um conjunto independente de imagens que diferem sutilmente, simulando lâminas de outro laboratório — o que os pesquisadores chamam de "mudança de domínio". Nesse conjunto de teste não visto, a acurácia geral caiu para cerca de 50% e o F1‑score balanceado caiu para aproximadamente 0,33. O modelo continuou a reconhecer muitas amostras cancerosas, mas teve grande dificuldade com tecido benigno, rotulando uma grande fração como maligna. Isso indica que a rede aprendeu detalhes fortemente ligados à fonte original dos dados — como estilo de coloração ou características do scanner — em vez de assinaturas robustas e portáteis da doença. O trabalho destaca que resultados brilhantes na validação interna podem gerar uma falsa sensação de segurança se os modelos não forem testados com dados verdadeiramente diferentes.
O que isso significa para futuras ferramentas de diagnóstico por IA
Para o leitor geral, a lição é dupla. Primeiro, sistemas de IA compactos podem de fato alcançar desempenho ao nível de especialistas em imagens de tecido do cólon, mantendo‑se pequenos e eficientes o suficiente para ampla implantação, o que abre caminho para rastreamento mais rápido e apoio a patologistas sobrecarregados. Segundo, e igualmente importante, um modelo que parece "perfeito" em seu conjunto de origem pode falhar drasticamente ao encontrar imagens de um hospital novo. Os autores argumentam que trabalhos futuros devem focar em tornar esses modelos leves mais robustos a variações de coloração, scanners e populações de pacientes — utilizando estratégias como treinamento robusto à coloração, adaptação de domínio e conjuntos de dados multicêntricos mais amplos. Até lá, a IA deve ser vista como um assistente promissor, e não como um decisor autônomo no diagnóstico do câncer.
Citação: Hanif, F., Raza, A. & Mohammed, H.A. Compact deep learning models for colon histopathology focusing performance and generalization challenges. Sci Rep 16, 5489 (2026). https://doi.org/10.1038/s41598-026-35119-y
Palavras-chave: câncer de cólon, histopatologia, deep learning, CNN leve, mudança de domínio