Clear Sky Science · pt
Fosfatase de dupla especificidade 6 interfere na atividade repressora do forkhead box O1 sobre CYP4A11 que medeia o acúmulo de lipídios no fígado
Por que a gordura no fígado importa
Excesso de gordura no fígado, frequentemente chamado de doença hepática gordurosa, está se tornando cada vez mais comum com dietas modernas ricas em açúcar e gordura. Enquanto muitas pessoas conhecem colesterol ou glicose sanguínea, poucas sabem que pequenos interruptores moleculares dentro das células hepáticas ajudam a decidir se a gordura será queimada ou armazenada. Este estudo examina três desses interruptores — proteínas chamadas DUSP6, FOXO1 e CYP4A11 — e revela como a disputa entre elas pode empurrar as células do fígado para armazenar gordura em excesso. Compreender esse sistema de controle oculto pode indicar caminhos para novos tratamentos para a doença hepática gordurosa e problemas metabólicos relacionados.
Um controlador de tráfego oculto dentro das células do fígado
Os pesquisadores se concentraram em uma proteína chamada DUSP6, conhecida principalmente por desligar uma via de sinalização celular chamada via ERK. Trabalhos anteriores mostraram que camundongos sem DUSP6 eram surpreendentemente resistentes à esteatose induzida por dieta, e seus fígados apresentavam níveis mais baixos de enzimas CYP4A, envolvidas no processamento de lipídios. Aqui, a equipe investigou o que DUSP6 faz em células derivadas do fígado humano e como isso poderia afetar uma versão humana dessas enzimas chamada CYP4A11. Eles utilizaram duas linhas celulares padrão de câncer de fígado, HepG2 e HuH‑7, como substitutas de células hepáticas humanas e as expuseram a uma mistura de ácidos graxos (ácido palmítico e oleico) para mimetizar um ambiente não saudável e rico em gordura. 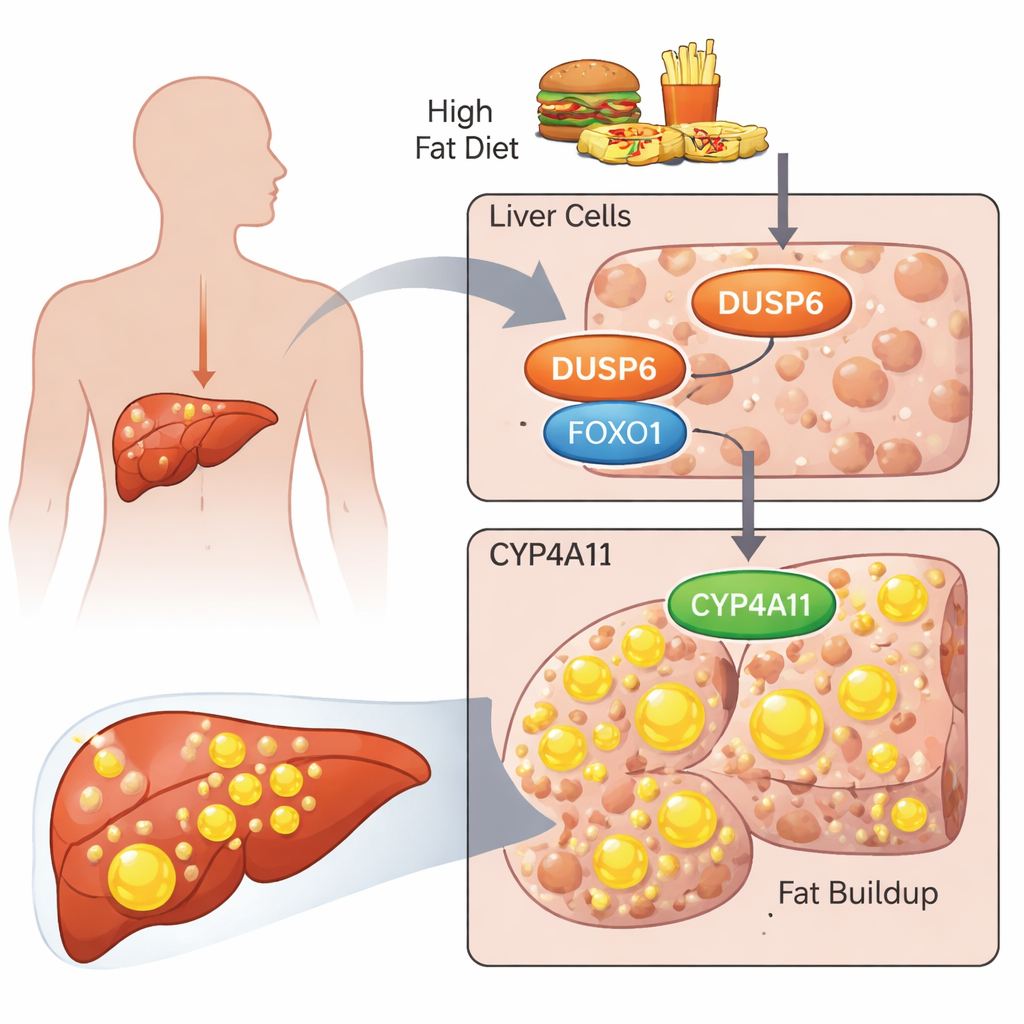
Dos ácidos graxos a uma célula cheia de gordura
Quando as células foram desafiadas com esses ácidos graxos, elas acumularam visivelmente gotículas de gordura, que os cientistas coraram e quantificaram. Ao mesmo tempo, os níveis de DUSP6 e CYP4A11 aumentaram, juntamente com formas ativadas de duas proteínas de sinalização importantes, AKT e FOXO1. A redução de DUSP6 com moléculas de RNA direcionadas reverteu esse padrão: as células armazenaram menos gordura, os níveis de CYP4A11 caíram, mas ERK, AKT e FOXO1 ativados aumentaram. Bloquear somente a via ERK na verdade piorou o acúmulo de gordura, enquanto bloquear apenas AKT o reduziu. Quando ERK e AKT foram inibidos simultaneamente, o acúmulo de gordura diminuiu e os níveis de CYP4A11 caíram. Esses experimentos ligaram estreitamente o CYP4A11 à quantidade de gordura acumulada e sugeriram que a atividade de AKT é especialmente importante para impulsionar o armazenamento de lipídios.
Um freio sobre genes que promovem gordura
Outro ator chave, FOXO1, é um fator de transcrição — uma proteína que pode entrar no núcleo celular e ligar ou desligar genes. Sabe‑se que FOXO1 atua como um freio sobre vários membros da mesma família de enzimas do CYP4A11. A equipe descobriu que reduzir os níveis de FOXO1 fez as células acumular mais gordura e aumentou o CYP4A11, enquanto aumentar diretamente o CYP4A11 deixou as células ainda mais gordurosas. Em contraste, forçar as células a produzir mais FOXO1 reduziu tanto o CYP4A11 quanto o acúmulo de gordura. Um fármaco que bloqueia a atividade do CYP4A11 (HET0016) diminuiu o excesso de gordura causado pela baixa presença de FOXO1, apoiando a ideia de que o CYP4A11 não é apenas um espectador, mas um motor do acúmulo lipídico. Testes químicos mostraram que o HET0016 reduziu 20‑HETE, um produto gerado pelo CYP4A11 associado ao estresse oxidativo e à inflamação, vinculando ainda mais essa via ao dano hepático.
Como DUSP6 desarma o freio
Para entender como FOXO1 controla o CYP4A11, os cientistas examinaram a região do DNA à frente do gene CYP4A11 e encontraram sequências onde FOXO1 pode se ligar. Usando um ensaio de imunoprecipitação de cromatina, mostraram que FOXO1 — especificamente em sua forma não fosforilada — se liga diretamente ao promotor de CYP4A11, consistente com um papel repressivo sobre esse gene. Experimentos de co‑imunoprecipitação revelaram que DUSP6 interage fisicamente com FOXO1, mas não com sua versão fosforilada. Estudos de fracionamento e microscopia mostraram que DUSP6 se localiza no citoplasma celular e, quando presente, mantém mais FOXO1 fora do núcleo. Quando DUSP6 foi reduzido, mais FOXO1 migrou para o núcleo, onde pôde se ligar ao DNA e suprimir o CYP4A11. Em efeito, DUSP6 atua como uma âncora, sequestrando FOXO1 no citoplasma e impedindo‑o de cumprir seu papel de freio sobre o CYP4A11. 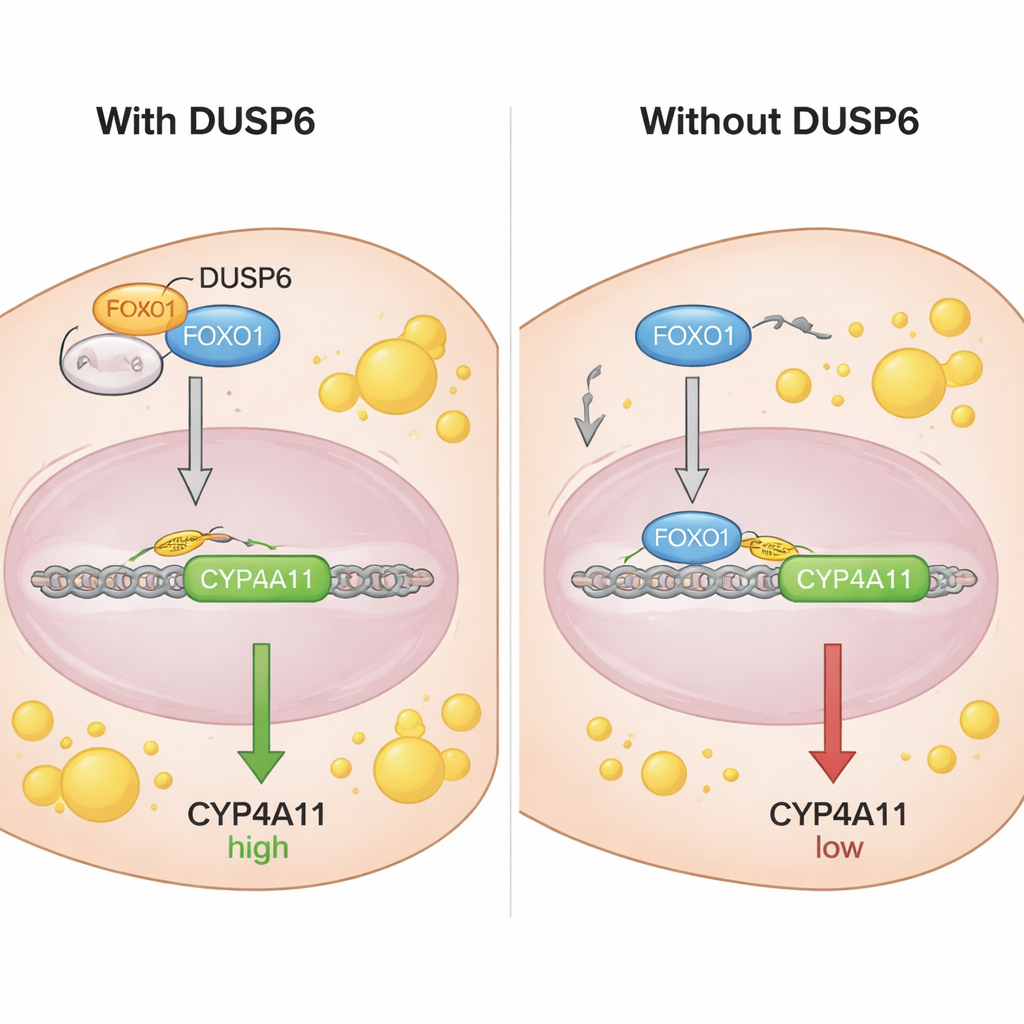
O que isso significa para a esteatose hepática e além
Em termos simples, este trabalho mapeia uma cadeia de eventos dentro das células do fígado: DUSP6 mantém FOXO1 no citoplasma, o que enfraquece a capacidade de FOXO1 de desligar o gene CYP4A11. Com FOXO1 neutralizado, o CYP4A11 torna‑se mais ativo, ajudando a empurrar a célula a armazenar mais gordura e a produzir moléculas como 20‑HETE que podem promover estresse oxidativo e inflamação. Embora essas descobertas provenham de células derivadas do fígado cultivadas em laboratório, e não de tecido hepático saudável humano, elas destacam DUSP6 e CYP4A11 como possíveis novos alvos para tratar a doença hepática esteatósica associada a disfunção metabólica. Terapias que reduzam a atividade de DUSP6 ou atenuem os efeitos do CYP4A11 poderiam, em teoria, restaurar a função de freio do FOXO1 e ajudar a controlar a gordura hepática.
Citação: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Palavras-chave: doença hepática gordurosa, DUSP6, FOXO1, CYP4A11, metabolismo hepático