Clear Sky Science · pt
Mineração do DrugBank com aprendizado de máquina revela novos candidatos à inibição de BCL-2
Por que encontrar medicamentos mais inteligentes contra o câncer importa
Células cancerígenas frequentemente se recusam a morrer quando deveriam. Muitos tumores sobrevivem ao superproduzir uma família de proteínas “guarda-costas” chamada BCL-2, que bloqueia o programa de autodestruição da célula. Já existem fármacos que miram BCL-2, mas eles podem causar efeitos colaterais e não funcionam para todo paciente. Este estudo explora como o aprendizado de máquina moderno pode vasculhar milhares de medicamentos já existentes para encontrar novos candidatos mais seguros que possam desarmar BCL-2 e ajudar as células cancerígenas a se autodestruírem.
Como as células escolhem entre vida e morte
Tecidos saudáveis removem constantemente células danificadas ou desnecessárias por meio de um processo controlado de autodestruição conhecido como apoptose, ou morte celular programada. Um grupo de proteínas chamado família BCL-2 atua como um interruptor central nessa decisão. Alguns membros empurram as células para a sobrevivência, enquanto outros as empurram para a morte. Em muitos cânceres, os membros que promovem a sobrevivência, incluindo BCL-2 e seu par próximo BCL-XL, são produzidos em excesso. Essa proteção adicional permite que células cancerígenas ignorem sinais de morte e resistam à quimioterapia. Por isso, bloquear BCL-2 tornou-se uma estratégia atraente no tratamento do câncer, mas os fármacos atuais frequentemente atingem proteínas relacionadas também, levando a efeitos colaterais como quedas perigosas na contagem de plaquetas.
Ensinando computadores a reconhecer moléculas promissoras
Em vez de procurar novos compostos do zero, os pesquisadores recorreram a bancos de dados de moléculas que já foram estudadas ou usadas como medicamentos. Começaram com um grande recurso público chamado ChEMBL, que contém medições experimentais de quão fortemente diferentes químicos se ligam a BCL-2. Após limpar cuidadosamente essas informações—removendo duplicatas, medições incertas e moléculas excessivamente grandes ou incomuns—eles terminaram com 601 compostos bem caracterizados. Cada molécula foi traduzida em uma espécie de impressão digital digital que captura suas características estruturais. Essas impressões digitais foram usadas para treinar e comparar sete modelos diferentes de aprendizado de máquina na tarefa de decidir se uma nova molécula provavelmente é um bloqueador forte de BCL-2 ou essencialmente inativa. 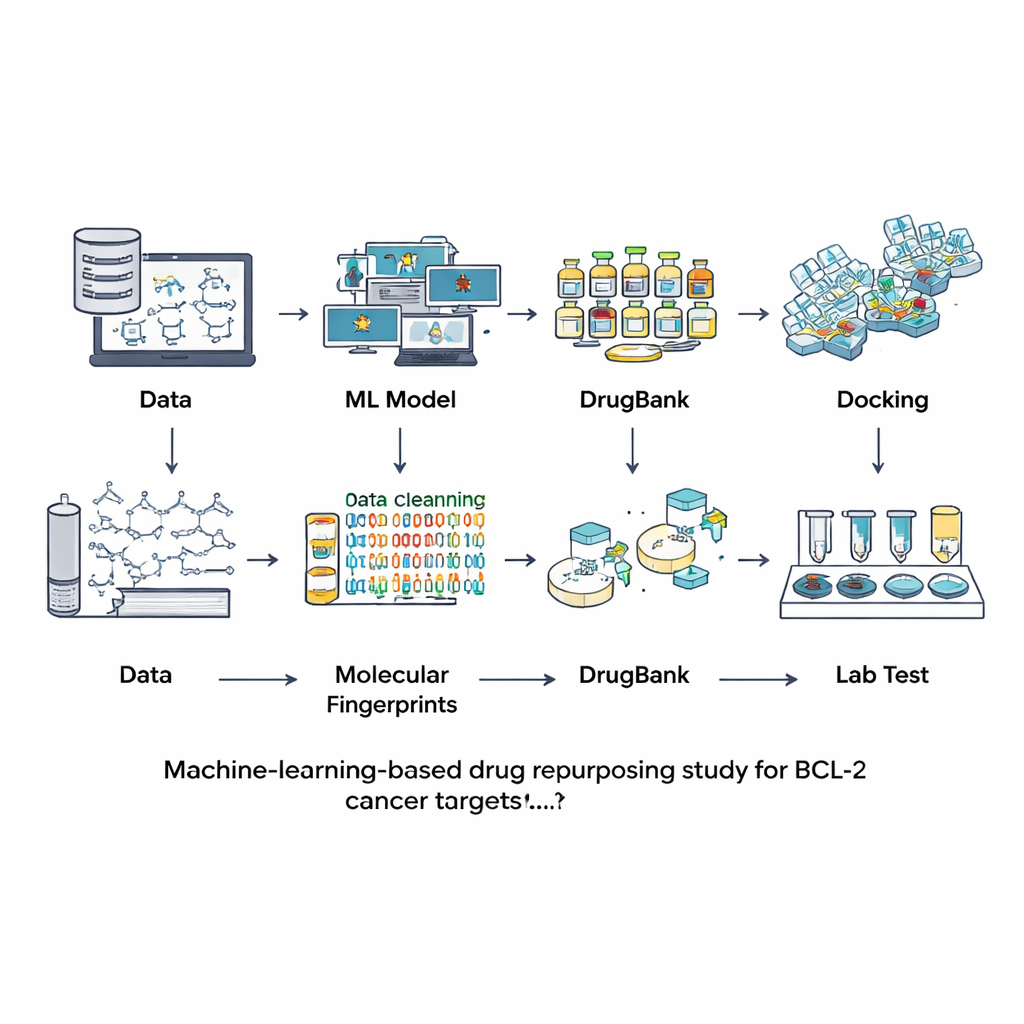
Escolhendo o melhor modelo e vasculhando uma biblioteca de fármacos
A equipe avaliou os modelos usando um conjunto de teste separado que não havia sido visto durante o treinamento, verificando não apenas com que frequência cada modelo estava certo, mas também quão bem distinguia ativos de inativos e quão equilibradas eram suas previsões. Um modelo chamado LightGBM—um método moderno de boosting baseado em árvores—teve o melhor desempenho na maioria das métricas, incluindo acurácia geral e sua habilidade de atribuir probabilidades confiáveis. Com esse modelo ajustado em mãos, os pesquisadores voltaram-se para o DrugBank, uma coleção curada de mais de 12.000 medicamentos aprovados, experimentais e descontinuados. Após calcular o mesmo tipo de impressões digitais, eles perguntaram ao LightGBM quais dessas moléculas pareciam potenciais inibidores de BCL-2. Apenas nove compostos obtiveram pontuações altas, cerca da décima parte de um por cento de toda a biblioteca, mostrando que a triagem virtual foi muito seletiva. Quatro dos nove já eram conhecidos como inibidores de BCL-2, o que tranquilizou a equipe quanto à solidez da abordagem.
Dos acertos computacionais às interações moleculares
Entre as moléculas restantes com pontuação alta, os pesquisadores se concentraram em três que não haviam sido previamente ligadas a BCL-2: Dersalazine, Opelconazole e Zongertinib. Para avaliar se esses candidatos poderiam plausivelmente se encaixar no bolso de ligação de BCL-2, eles usaram docking computacional, uma técnica que prevê como uma pequena molécula pode se acomodar na superfície da proteína. As simulações sugeriram que Opelconazole e Zongertinib, em particular, formam redes de contatos favoráveis com os mesmos aminoácidos-chave que agarram um fármaco de referência bem estudado, o ABT-737. Suas forças de ligação previstas eram próximas às de inibidores estabelecidos, sugerindo que o modelo de aprendizado de máquina de fato descobriu moléculas capazes de desarmar BCL-2. 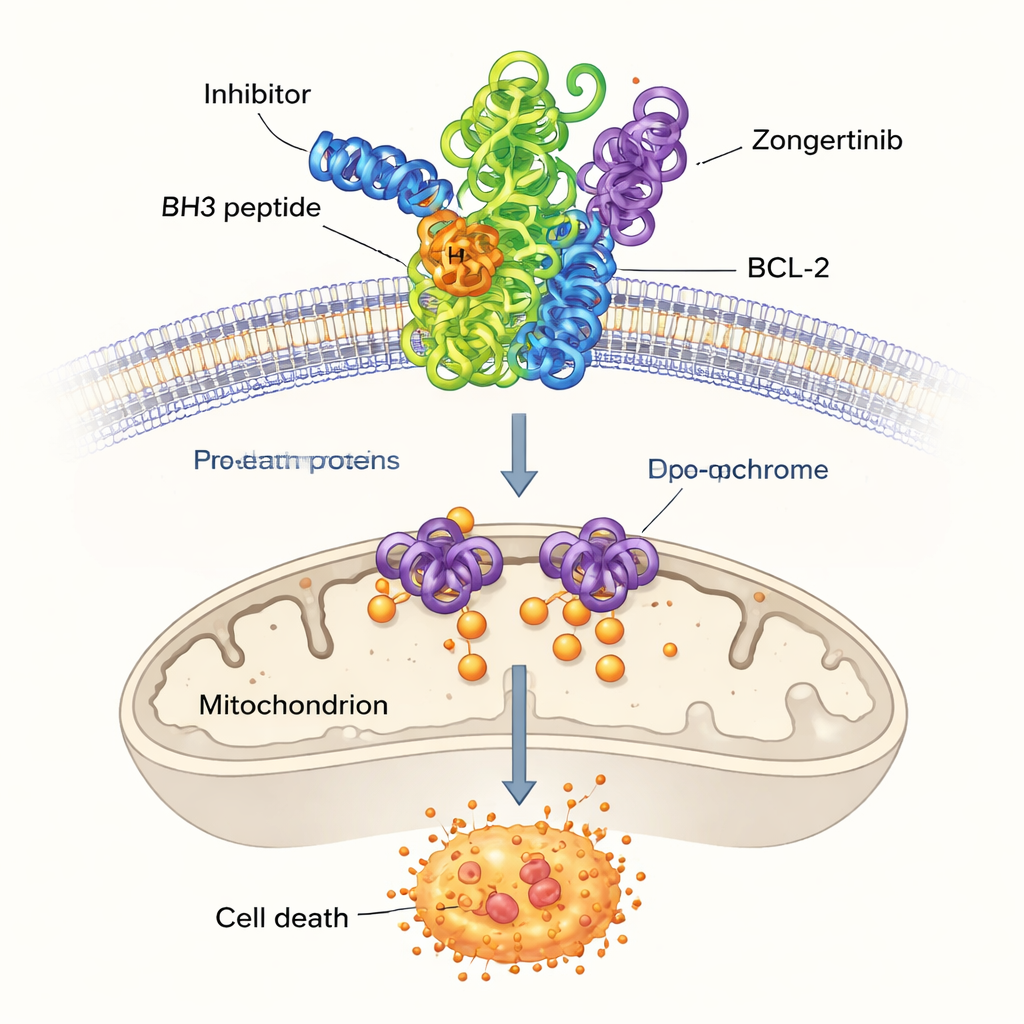
Colocando previsões à prova no laboratório
Dicas computacionais são úteis apenas se se mantiverem em condições do mundo real. A equipe, portanto, testou os três candidatos em um ensaio bioquímico que mede quão bem um composto pode impedir BCL-2 de se ligar a um de seus parceiros naturais. Em uma faixa de concentrações, Dersalazine mostrou pouco efeito. Opelconazole e Zongertinib, no entanto, reduziram a atividade de BCL-2 em doses altas, com Opelconazole quase desligando totalmente o sinal. Embora essas concentrações sejam mais altas do que o ideal para um fármaco pronto para clínica, elas demonstram que os candidatos realmente interagem com BCL-2 e validam todo o fluxo de descoberta.
O que isso significa para futuras terapias contra o câncer
Para um não especialista, a mensagem principal é que os pesquisadores treinaram com sucesso um sistema computacional para reconhecer como é a “cara” de uma molécula que bloqueia BCL-2 e, em seguida, o usaram para minerar uma grande biblioteca de fármacos e compostos semelhantes a fármacos. A abordagem redescobriu medicamentos conhecidos contra BCL-2 e destacou novos candidatos, dois dos quais mostraram atividade inibitória real em testes de laboratório. Embora ainda reste muito trabalho—aumentar a potência, compreender a segurança e testar em células e animais—este estudo demonstra como aprendizado de máquina e curadoria inteligente de dados podem acelerar a busca por melhores medicamentos contra o câncer reaproveitando e reavaliando compostos que já conhecemos.
Citação: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Palavras-chave: inibidores de BCL-2, aprendizado de máquina, repositório de drogas, apoptose, terapia contra o câncer