Clear Sky Science · pt
Estrutura cristalina da cystatin B de Echinococcus multilocularis revela uma característica inédita em stefins clássicos
Por que a arma secreta de um parasita hepático importa
A equinococose alveolar é um nome complicado para uma infecção por um pequeno verme achatado que se comporta de maneira semelhante a um câncer de crescimento lento no fígado. Frequentemente é letal, e os medicamentos atuais têm eficácia limitada e podem causar efeitos colaterais sérios. Este estudo examina uma molécula específica produzida pelo parasita, uma proteína chamada EmCystatin-B, para entender como ela pode ajudar o verme a escapar das nossas defesas — e como, no futuro, poderia ser transformada em alvo para novos tratamentos.
Um verme perigoso que cresce como um tumor
A doença é causada pela fase larval do parasita Echinococcus multilocularis. As pessoas se infectam ao engolir acidentalmente ovos do parasita, por exemplo em alimentos ou água contaminados. Uma vez no corpo, as larvas se instalam principalmente no fígado e crescem formando muitos pequenos sacos cheios de líquido que infiltram o tecido ao redor, espalham-se para órgãos próximos, como o baço, e às vezes alcançam locais distantes como os pulmões ou o cérebro. Sem tratamento eficaz, mais de 9 em cada 10 pacientes morrem em 10 a 15 anos. Atualmente, a melhor opção é cirurgia combinada com medicamentos antiparasitários de longo prazo, mas o diagnóstico precoce é difícil e os fármacos não curam a infecção de forma confiável. Isso torna crucial entender como o parasita interage com o corpo humano em nível molecular.
Uma proteína do parasita que desarma enzimas de corte
Muitos animais, incluindo humanos, produzem uma família de proteínas chamadas cistatinas que atuam como travas de segurança em poderosas enzimas digestivas conhecidas como proteases de cisteína. Essas enzimas podem degradar outras proteínas e são importantes em processos como a eliminação de partes celulares desgastadas e a ativação de respostas imunes. Parasitas aprenderam a produzir proteínas semelhantes a cistatinas para interferir nas enzimas e no sistema imune do hospedeiro. Neste trabalho, os pesquisadores identificaram uma proteína do tipo cistatina em E. multilocularis e a batizaram de EmCystatin-B. Eles descobriram que o gene da EmCystatin-B é muito mais ativo nas cabeças larvais maduras (protoscolex) do parasita do que no tecido do cisto circundante, e que a proteína está presente no citoplasma e no núcleo das células do parasita, especialmente em células germinativas “tipo stem” em divisão. Testes em laboratório mostraram que a EmCystatin-B pode bloquear fortemente a atividade da catepsina B humana, uma importante protease de cisteína envolvida na imunidade e na remodelação tecidual.
Uma forma familiar com uma reviravolta inesperada
Para ver exatamente como a EmCystatin-B é construída, a equipe cristalizou a proteína purificada e utilizou cristalografia de raios X para resolver sua estrutura tridimensional em resolução quase atômica. Como outros membros da família das cistatinas, cada unidade de EmCystatin-B apresenta uma forma característica: um segmento central helicoidal apoiado por várias fitas planas em formato de fita, formando uma cunha que normalmente se ajusta ao sítio ativo de uma protease. Com base em sua sequência e na ausência de um peptídeo sinal óbvio para secreção, a EmCystatin-B pertence ao subgrupo “stefin” das cistatinas, que geralmente são pequenas proteínas intracelulares e sem pontes dissulfeto estabilizadoras. Surpreendentemente, a estrutura revelou que, embora cada unidade de EmCystatin-B apresente o dobramento esperado, a forma como essas unidades se associam entre si é incomum e específica da espécie quando comparada à contraparte humana, a cystatin B.
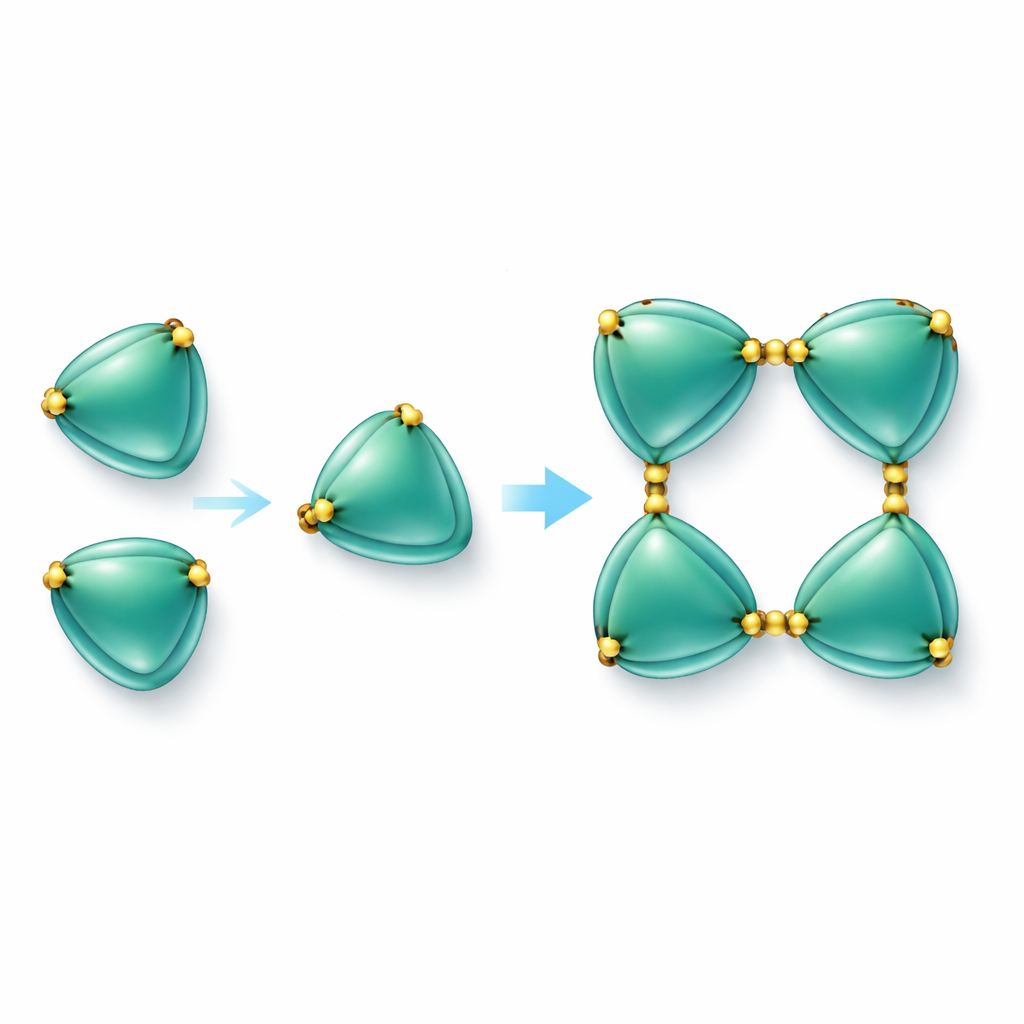
Construindo cadeias proteicas com ligações de enxofre
A descoberta mais marcante foi que as moléculas de EmCystatin-B não ficam simplesmente isoladas como unidades únicas. Em vez disso, elas podem se ligar em etapas para formar dímeros (pares) e depois tetrâmeros (grupos de quatro). Dois mecanismos diferentes ajudam a formar os dímeros iniciais. Em um, uma parte de uma molécula se projeta e completa a estrutura da sua vizinha, um fenômeno conhecido como domain swapping (troca de domínio). No outro, pares de moléculas são amarrados por pontes dissulfeto — ligações químicas fortes entre aminoácidos que contêm enxofre (cisteínas). Na EmCystatin-B, a cisteína na posição 4 de uma molécula liga-se à cisteína na posição 76 de uma molécula parceira. Quatro dessas cruzes então estabilizam o tetrâmero. Esse uso de múltiplas pontes dissulfeto intermoleculares é completamente novo para stefins clássicos, que tipicamente não apresentam tais ligações. Quando os pesquisadores substituíram essas cisteínas-chave por outro aminoácido, a proteína deixou de se montar eficientemente em complexos de ordem superior e sua capacidade de inibir a catepsina B caiu drasticamente.
O que isso significa para combater a infecção
Para quem não é especialista, a mensagem é que o parasita evoluiu uma versão especialmente conectada de uma família proteica comum, usando “rebites” químicos extras para travar várias unidades inibidoras juntas. Essa forma oligomérica parece importante para desligar uma enzima do hospedeiro que, de outra forma, ajudaria a controlar a infecção. Ao revelar a arquitetura precisa da EmCystatin-B e suas assemblies exclusivas ligadas por dissulfetos, o estudo amplia nossa compreensão de como proteínas cistatin podem ser ajustadas entre espécies. A longo prazo, essas descobertas podem orientar o desenho de fármacos que bloqueiem o efeito protetor da EmCystatin-B sobre o parasita ou que imitem suas propriedades de acalmar o sistema imune para tratar doenças inflamatórias.
Citação: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Palavras-chave: equinococose alveolar, Echinococcus multilocularis, cystatin B, estrutura proteica, modulação imune