Clear Sky Science · pt
Interrupção da montagem do inflamassoma NLRP3 via remodelamento induzido por ligante das interfaces do domínio pirina
Por que acalmar a inflamação descontrolada importa
Muitas doenças crônicas — desde artrite e gota até doenças cardíacas e neurodegeneração — são alimentadas por um sistema de alarme imune hiperativo dentro de nossas células. Uma parte-chave desse alarme, chamado inflamassoma NLRP3, nos ajuda a combater infecções, mas também pode promover inflamação nociva quando dispara de forma inadequada. Este estudo descreve uma nova pequena molécula, denominada E9, que mira um passo inicial na ativação do NLRP3, oferecendo um ângulo novo para o desenho de medicamentos que atenuem inflamação prejudicial sem desligar totalmente o sistema imune.
Um alarme celular com um lado sombrio
Quando nossos corpos percebem perigo, células imunes montam o inflamassoma NLRP3, um grande complexo proteico que funciona como um alarme molecular. Uma vez formado, essa estrutura ativa uma enzima chamada caspase‑1, que por sua vez ativa mensageiros inflamatórios potentes, incluindo as citocinas IL‑1β e IL‑18. Esses sinais são vitais para combater infecções e remover tecido danificado. Mas se o inflamassoma permanece ligado por tempo excessivo ou é ativado no momento errado, contribui para condições inflamatórias crônicas que afetam articulações, vasos sanguíneos, cérebro e outros órgãos. Por isso pesquisadores de todo o mundo buscam maneiras precisas de controlar o NLRP3 sem suprimir amplamente a imunidade.
Buscando além dos alvos habituais de fármacos
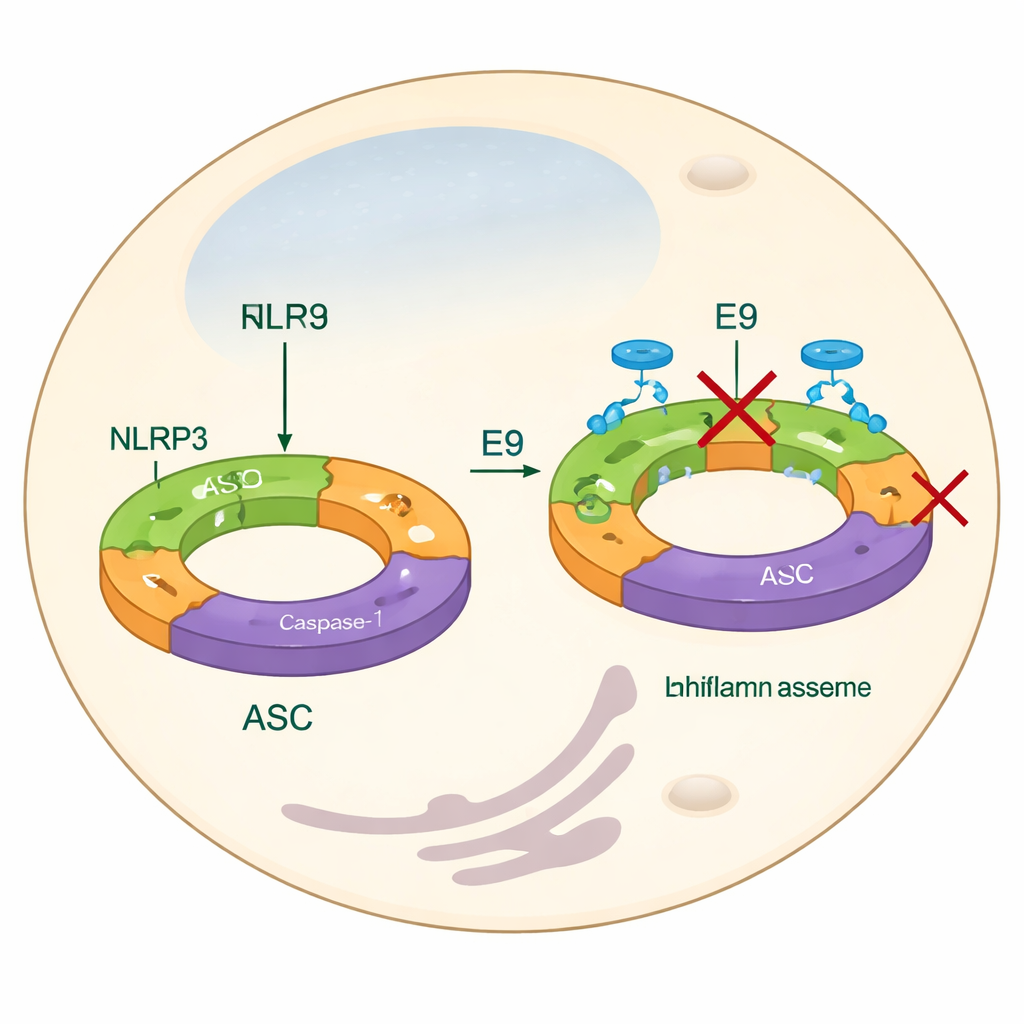
A maioria das estratégias atuais para domar o NLRP3 concentra‑se em bloquear seus produtos finais — como a IL‑1β — ou em interferir com um domínio central tipo motor que usa moléculas de energia como ATP. Embora essas abordagens possam funcionar, elas podem não atingir os passos iniciais de montagem e não explicam completamente como as proteínas NLRP3 se juntam para formar uma máquina funcional. Neste trabalho, os autores focalizam o domínio pirina, uma parte do NLRP3 que ajuda unidades individuais a se acoplarem em filamentos longos. Esses filamentos então recrutam outra proteína adaptadora, ASC, que se agrega em “pontos” brilhantes dentro das células — um marco visual da ativação do inflamassoma. Ao encontrar compostos que impedem que domínios pirina se encaixem corretamente, a equipe pretende evitar a formação do inflamassoma desde o início.
Encontrando uma molécula que quebre a cadeia
Os pesquisadores triaram uma biblioteca de 1.500 pequenas moléculas recém‑sintetizadas usando um ensaio esperto baseado em luz. Eles fundiram pedaços separados de uma enzima luciferase ao domínio pirina do NLRP3; quando dois domínios pirina se aproximavam, os fragmentos enzimáticos se reconstituíam e produziam luz. Compostos que bloqueavam o contato pirina–pirina fizeram o sinal luminoso cair. Diante dessa triagem, identificaram quatro candidatos promissores, com um — E9 — destacando‑se pela inibição forte e consistente. Medições posteriores usando uma técnica chamada termoforese em microescala mostraram que E9 se ligava firmemente ao domínio pirina em concentrações muito baixas (submicromolares), confirmando que seu efeito não era um artefato aleatório, mas sim resultado de uma interação específica.
Vendo o efeito dentro de células vivas
Para testar se E9 também poderia funcionar em um sistema vivo, a equipe recorreu a células humanas do tipo imune, geneticamente modificadas para produzir uma versão fluorescente de ASC. Quando essas células são estimuladas com componentes bacterianos e um segundo gatilho, o NLRP3 é ativado e as proteínas ASC se agrupam em pontos brilhantes que podem ser contados ao microscópio. Na presença de E9, o número desses pontos caiu de forma marcante, comparável ou superior a alguns bloqueadores conhecidos do NLRP3. Isso mostrou que interferir nos contatos entre domínios pirina é suficiente para reduzir a montagem do inflamassoma e os passos iniciais da morte celular inflamatória, ao menos em condições laboratoriais.
Como E9 remodela a estrutura do inflamassoma
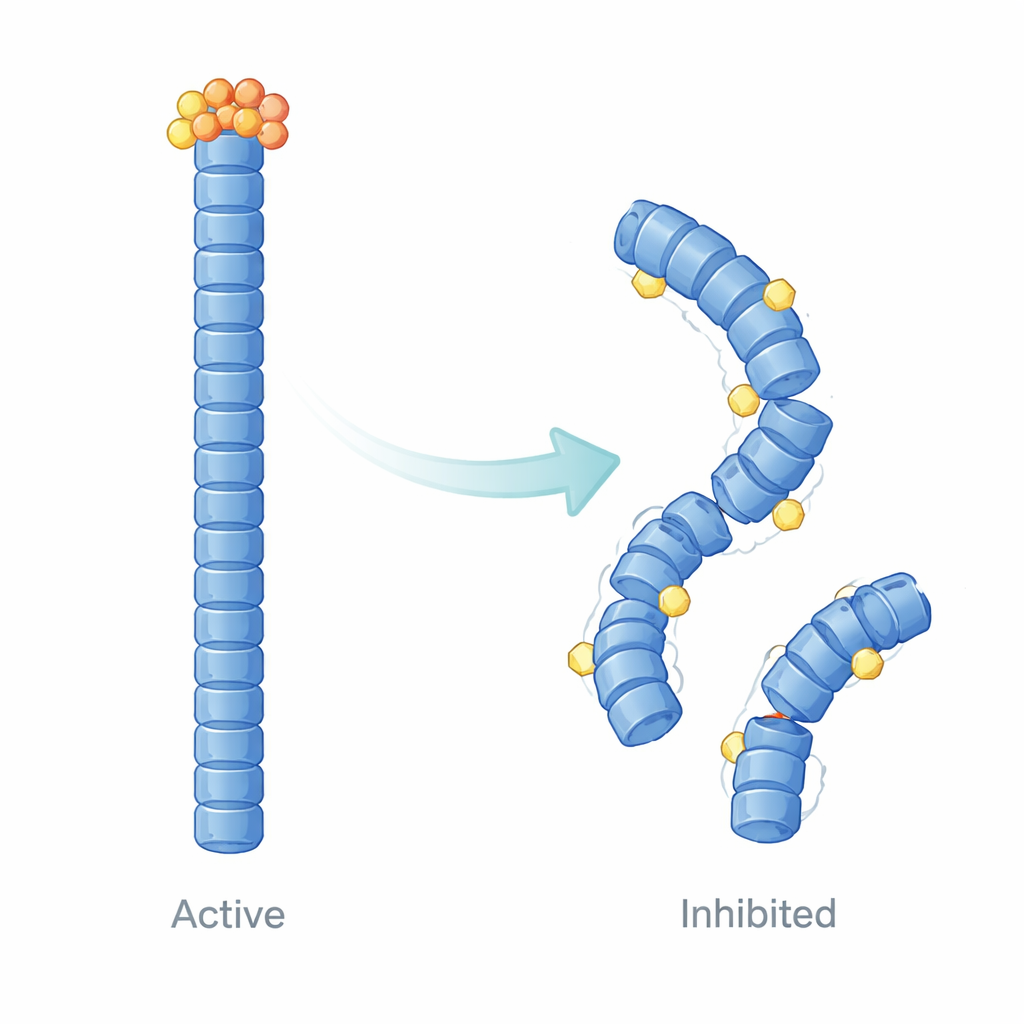
Além de simplesmente medir a ligação, os autores usaram modelagem estrutural por computador e simulações de dinâmica molecular para visualizar como E9 altera o comportamento dos filamentos de NLRP3 ao longo do tempo. Seus cálculos sugerem que E9 se aloja em superfícies de contato específicas onde domínios pirina se tocam, afrouxando e remodelando sutilmente o filamento. Em vez de uma estrutura cooperativa uniformemente estável, o filamento torna‑se desigual: regiões próximas à E9 ligada tornam‑se mais flexíveis e perdem seu alinhamento preciso, enquanto outras partes ficam dinamicamente isoladas. Essas mudanças atenuam os movimentos em grande escala e a comunicação estreita necessários para um recrutamento eficiente de ASC, oferecendo uma explicação física para a redução da formação de pontos observada nas células.
O que isso pode significar para terapias futuras
Em conjunto, os achados posicionam E9 como um protótipo de uma nova classe de fármacos que miram o inflamassoma agindo ao interromper as interfaces entre os blocos de construção do NLRP3, em vez de bloquear seu uso de energia ou produtos finais. Embora o trabalho atual se limite a ensaios em tubo de ensaio, simulações computacionais e células em cultura — e sejam necessários estudos adicionais em animais e humanos —, demonstra que pequenas moléculas bem projetadas podem remodelar o próprio andaime do inflamassoma. Para pacientes com doenças impulsionadas por inflamação descontrolada, fármacos focados em interfaces poderiam algum dia oferecer um controle mais preciso, reduzindo a ativação imune nociva enquanto mantêm as defesas essenciais amplamente intactas.
Citação: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Palavras-chave: inflamassoma NLRP3, domínio pirina, inibidor de pequena molécula, imunidade inata, piropoptose