Clear Sky Science · pt
Base estrutural para diosgenina como agonista inverso do receptor órfão relacionado ao ácido retinóico γ
Por que um composto vegetal e um interruptor imunológico importam
Muitas condições crônicas — desde doenças autoimunes como esclerose múltipla e psoríase até obesidade e diabetes tipo 2 — são impulsionadas por sinais imunológicos hiperativos e por sinais metabólicos desregulados. Cientistas há muito procuram medicamentos mais seguros que possam ajustar esses sinais para cima ou para baixo com precisão. Este estudo explora como a diosgenina, uma molécula natural presente em certas plantas medicinais e inhames, se liga a uma proteína reguladora do sistema imune chamada RORγ e a converte para um estado menos ativo. Compreender essa interação em nível atômico pode abrir caminho para terapias mais suaves e direcionadas, construídas a partir de um arcabouço derivado de plantas bem conhecido.
Um dossel mestre para imunidade e metabolismo
RORγ faz parte de uma grande família de “receptores nucleares” — proteínas dentro das células que ligam ou desligam genes em resposta a pequenas moléculas. Essa proteína em particular é um controlador chave de um grupo de células imunes conhecidas como células Th17, que produzem o sinal inflamatório IL-17A e têm sido associadas a doenças autoimunes como esclerose múltipla, psoríase, artrite reumatoide e doença de Crohn. RORγ também influencia como os adipócitos se desenvolvem e como o corpo responde à insulina, conectando-o à obesidade e ao diabetes. Por causa desse alcance amplo, RORγ tornou-se um alvo atrativo para fármacos, mas muitas moléculas sintéticas que se ligam a ele enfrentaram problemas de segurança, seletividade ou eficácia em humanos.
Um remédio tradicional gera um candidato promissor
A diosgenina é uma molécula do tipo esteroide extraída de plantas, incluindo espécies de Dioscorea (inhame selvagem) e várias ervas medicinais tradicionais. Ela tem sido estudada por benefícios anti-inflamatórios, anticâncer, antidiabéticos e cardiovasculares em modelos celulares e animais. Trabalhos anteriores sugeriram que a diosgenina poderia influenciar a via RORα/γ e suprimir respostas Th17 prejudiciais, mas não estava claro se ela atuava diretamente em RORγ ou como poderia modular o comportamento da proteína. Para responder a isso, os autores triaram uma biblioteca de compostos naturais usando um ensaio sensível de ligação e identificaram a diosgenina como um forte ligante da região de ligação ao ligante de RORγ.
Como a diosgenina empurra RORγ para a marcha à ré
Os pesquisadores examinaram como a diosgenina afeta a habilidade de RORγ de recrutar proteínas auxiliares que ou aumentam (coativadores) ou atenuam (correpressoras) a atividade gênica. Surpreendentemente, a diosgenina incentivou RORγ a se ligar a ambos os tipos de parceiros, um padrão diferente do de um antagonista natural conhecido chamado ácido ursólico. Em testes celulares com repórteres que acompanham a ativação gênica, a diosgenina reduziu consistentemente a atividade dirigida por RORγ de forma dependente da dose, com potência na faixa submicromolar. Esse comportamento se encaixa no perfil de um “agonista inverso”: um composto que não apenas bloqueia a atividade basal, mas ativamente empurra o receptor para um estado desligado, mesmo quando ele estaria normalmente ativado.
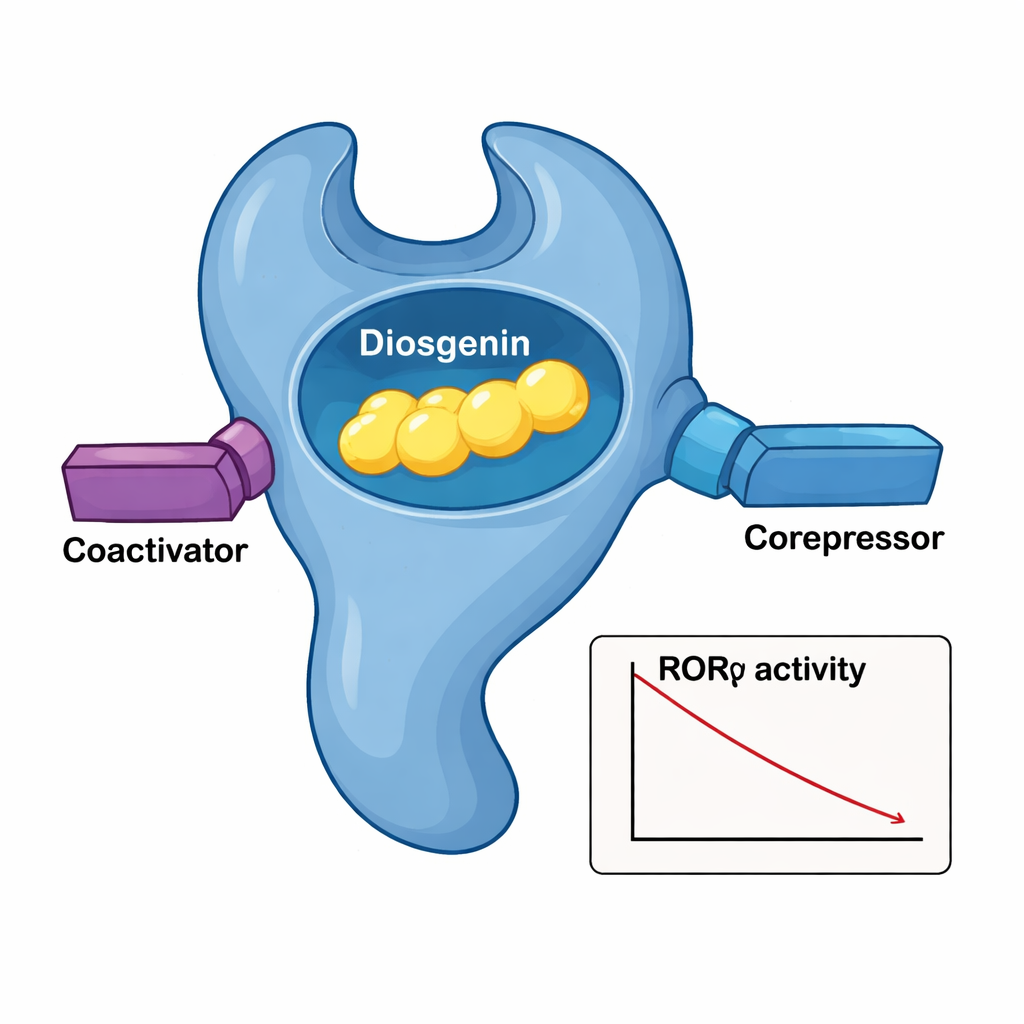
Um close do aperto molecular
Para ver exatamente como a diosgenina se encaixa em RORγ, a equipe resolveu a estrutura cristalina tridimensional do domínio de ligação ao ligante da proteína com diosgenina alojada em seu interior. O receptor se dobra em um feixe em camadas de hélices, formando um bolso que acolhe o corpo do tipo esteroide da diosgenina. Uma rede de contatos hidrofóbicos ajustados por vários aminoácidos age como uma luva sob medida em torno do esqueleto da molécula, enquanto um grupo hidroxila crítico na diosgenina forma ligações de hidrogênio mediadas por água com duas argininas. Quando esses resíduos do bolso foram alterados um a um, a capacidade da diosgenina de silenciar RORγ diminuiu, confirmando sua importância. Comparações estruturais com o complexo RORγ–ácido ursólico mostraram que a diosgenina mantém uma hélice terminal chave (AF‑2) em uma posição “semelhante à ativa” mesmo enquanto reduz a transcrição geral, explicando por que ela pode ao mesmo tempo recrutar coativadores e correpressoras.
Da estrutura cristalina a futuros medicamentos
O retrato detalhado da interação diosgenina–RORγ destaca duas vantagens notáveis para o desenho de fármacos. Primeiro, o bolso do receptor mostra flexibilidade suficiente para reconhecer diferentes formas de ligantes, o que significa que químicos podem ajustar o arcabouço da diosgenina para aprimorar a seletividade por RORγ e reduzir a ligação indesejada a outros receptores nucleares. Segundo, a origem natural da diosgenina e sua toxicidade inerente conhecida como baixa em modelos pré-clínicos tornam-na um ponto de partida atraente em comparação com alguns compostos totalmente sintéticos que fracassaram em ensaios. Em termos simples, este trabalho revela como uma molécula derivada de plantas pode se prender a um interruptor central imunometabólico e empurrá‑lo para a marcha à ré, oferecendo um modelo estrutural para desenvolver tratamentos mais seguros e eficazes para doenças relacionadas a RORγ.
Citação: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Palavras-chave: ROR gamma, diosgenina, doença autoimune, receptor nuclear, agonista inverso