Clear Sky Science · pt
Caracterização transcriptômica do splicing alternativo aberrante em músculos esqueléticos de pacientes com sarcopenia
Por que os músculos envelhecidos perdem força
Sarcopenia — a perda gradual de massa e força muscular com a idade — é uma das principais razões pelas quais adultos mais velhos têm dificuldade em tarefas cotidianas, desde subir escadas até carregar compras. Este estudo investiga o interior do músculo envelhecido ao nível do RNA, as mensagens que dizem às células quais proteínas produzir. Os autores mostram que, na sarcopenia, muitas dessas mensagens de RNA são cortadas e emendadas de maneiras anormais, potencialmente perturbando a produção de energia no músculo e apontando para novos alvos terapêuticos.
Perda muscular e o sistema de “edição” genético do corpo
Nossos genes estão escritos em DNA, mas as células trabalham a partir de cópias em RNA desses genes. Antes que uma mensagem de RNA seja utilizada, as células normalmente a apararam e emendaram — muito parecido com a edição de um filme — de modo que um único gene possa produzir várias versões de uma proteína. Esse processo, chamado splicing alternativo, é especialmente ativo no músculo, que precisa de proteínas finamente ajustadas para contrair, reparar-se e adaptar-se ao exercício. Quando o splicing falha, versões erradas de proteínas podem ser produzidas ou importantes isoformas podem se perder, contribuindo para doenças como distrofia muscular e alguns distúrbios cerebrais. Os autores suspeitaram que uma camada semelhante de má edição de RNA poderia estar impulsionando a sarcopenia.
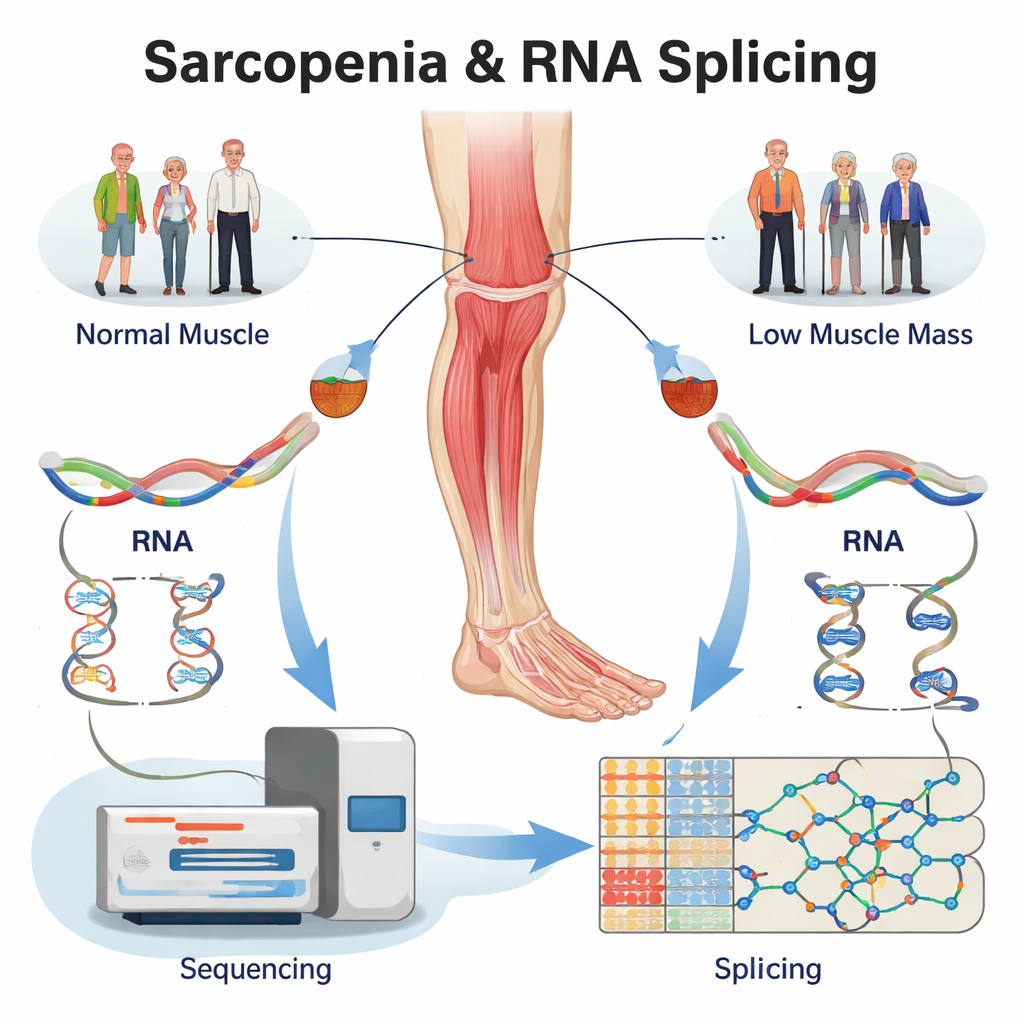
Reanalisando dados existentes para encontrar erros ocultos no RNA
Em vez de recrutar novos voluntários, a equipe reanalisou um grande conjunto de dados de sequenciamento de RNA já disponível de biópsias do músculo da coxa humana. As amostras vieram de quatro grupos: idosos com sarcopenia estabelecida, pessoas com apenas baixa massa muscular, pessoas com apenas baixa força muscular, e controles saudáveis pareados por idade. Usando software especializado, eles primeiro confirmaram que centenas de genes estavam regulados para cima ou para baixo nos músculos doentes. Ainda mais importante, em seguida analisaram como o RNA de cada gene era emendado, catalogando mais de 5.000 alterações de splicing nos três grupos com problemas em comparação com o músculo saudável. Essas alterações concentraram-se em alguns tipos básicos — como a omissão de um éxon ou a escolha de um sítio de corte alternativo — padrões conhecidos por alterar fortemente a estrutura proteica.
Fábricas de energia e vias reguladoras do “medidor de combustível” celular são perturbadas
As alterações de splicing surgiram em genes centrais para a biologia muscular. Muitos genes afetados codificam partes das mitocôndrias, as pequenas fábricas de energia que alimentam a contração muscular. No músculo sarcopênico, 16 genes envolvidos na fosforilação oxidativa — o processo que transforma nutrientes em energia utilizável — mostraram splicing alterado, especialmente componentes dos complexos mitocondriais que lidam com o transporte de elétrons e a bomba de prótons. Outras mudanças apareceram em genes que sintetizam ou utilizam NAD⁺, uma molécula-chave para a energia e reparo celular. Em vez de simplesmente variar em abundância, enzimas importantes como CD38, PARP2 e várias sirtuínas produziram variantes de RNA diferentes, sugerindo que o equilíbrio entre produção e consumo de NAD⁺ está distorcido ao nível do splicing. Os genes afetados também se agruparam em vias de sinalização muscular bem conhecidas, incluindo as vias AMPK e FoxO, que atuam como medidores de combustível celular e respondedores ao estresse.
Padrões compartilhados em diferentes estágios — e entre espécies
De forma marcante, muitos dos mesmos genes exibiram alterações de splicing não apenas em pessoas com sarcopenia estabelecida, mas também naquelas que apresentavam apenas baixa massa muscular ou apenas baixa força. Isso sugere que o splicing anômalo começa cedo e atravessa as diferentes manifestações clínicas da doença. Para testar se essas mudanças poderiam ser reproduzidas em um modelo animal, os pesquisadores induziram desgaste muscular em camundongos com dexametasona, um esteroide usado rotineiramente para mimetizar algumas características da sarcopenia. Os camundongos desenvolveram força de preensão reduzida e desempenho pior em testes de corrida e equilíbrio. Quando a equipe sequenciou o RNA muscular dos camundongos, novamente encontrou centenas de genes com splicing alterado. Cerca de um quinto desses genes se sobrepunha aos genes humanos associados à sarcopenia, e muitos estavam envolvidos no controle da transcrição, da estrutura da cromatina e do próprio splicing — interruptores de nível superior que podem remodelar toda a produção proteica de uma célula.
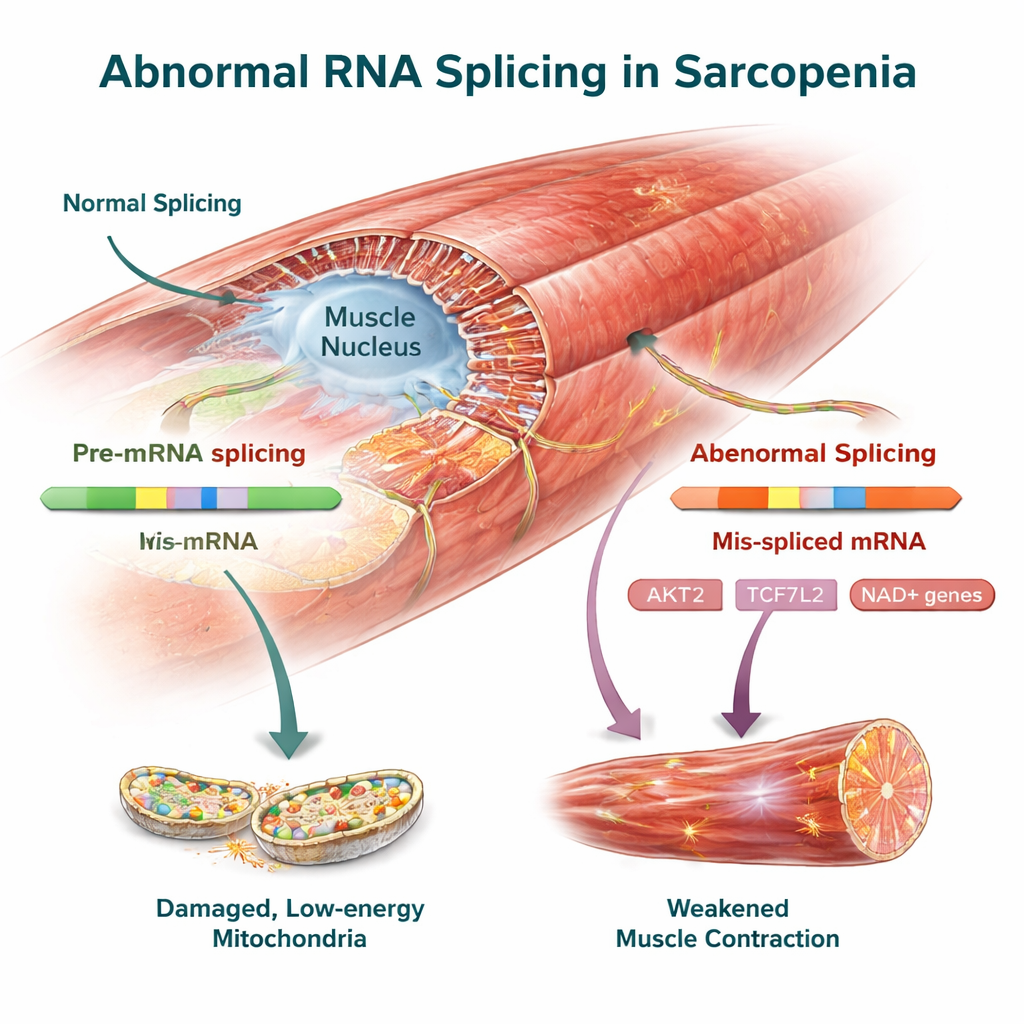
Genes-chave de controle muscular como potenciais alvos terapêuticos
Entre as mudanças conservadas entre espécies estavam vários genes já ligados à saúde muscular. AKT2, um regulador central do crescimento e da síntese proteica no músculo, exibiu mudanças de splicing distintas em humanos e em camundongos que podem reduzir sua capacidade de manter a massa muscular. TCF7L2, parte da via de sinalização Wnt, junto com FMNL2 e USP40, que ajudam a organizar o andaime interno do músculo e a controlar a qualidade proteica, também apresentaram variantes de RNA alteradas. A equipe confirmou essas alterações de splicing experimentalmente em músculo de camundongo, reforçando a hipótese de que são características reais da doença e não artefatos da análise de dados.
O que isso significa para prevenir a fragilidade
Para não especialistas, a mensagem é que a sarcopenia não é apenas sobre músculos “se desgastando” ou genes sendo simplesmente ativados ou desativados. Envolve também uma ampla má-edição das mensagens de RNA que orientam como as células musculares fabricam e mantêm sua maquinaria, especialmente os sistemas que geram energia e detectam estresse. Como o splicing pode, em princípio, ser corrigido com medicamentos baseados em RNA projetados com precisão, os erros de splicing conservados descobertos aqui — particularmente em genes como AKT2 e TCF7L2 — oferecem um novo conjunto de pistas para terapias que ajudem músculos envelhecidos a permanecerem mais fortes por mais tempo.
Citação: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Palavras-chave: sarcopenia, envelhecimento muscular, splicing de RNA, mitocôndrias, AKT2