Clear Sky Science · pt
Modelo fenomenológico da estabilização da transtirretina
Por que isso importa para pacientes e famílias
A amiloidose por transtirretina é uma condição grave em que uma proteína normal do sangue, a transtirretina (TTR), se desfaz e seus fragmentos podem se aglutinar em depósitos nocivos no coração e nos nervos. Novos medicamentos, como tafamidis e acoramidis, foram desenvolvidos para manter essa proteína em sua forma segura de quatro partes, e já melhoraram os desfechos de muitas pessoas. Ainda assim, os médicos observam um efeito intrigante em pacientes tratados: os níveis sanguíneos de TTR aumentam em mais de 30%, e não é óbvio por que isso ocorre. Este artigo usa um modelo matemático simplificado para explorar o que pode estar acontecendo no organismo e o que isso significa para o modo de ação real desses medicamentos. 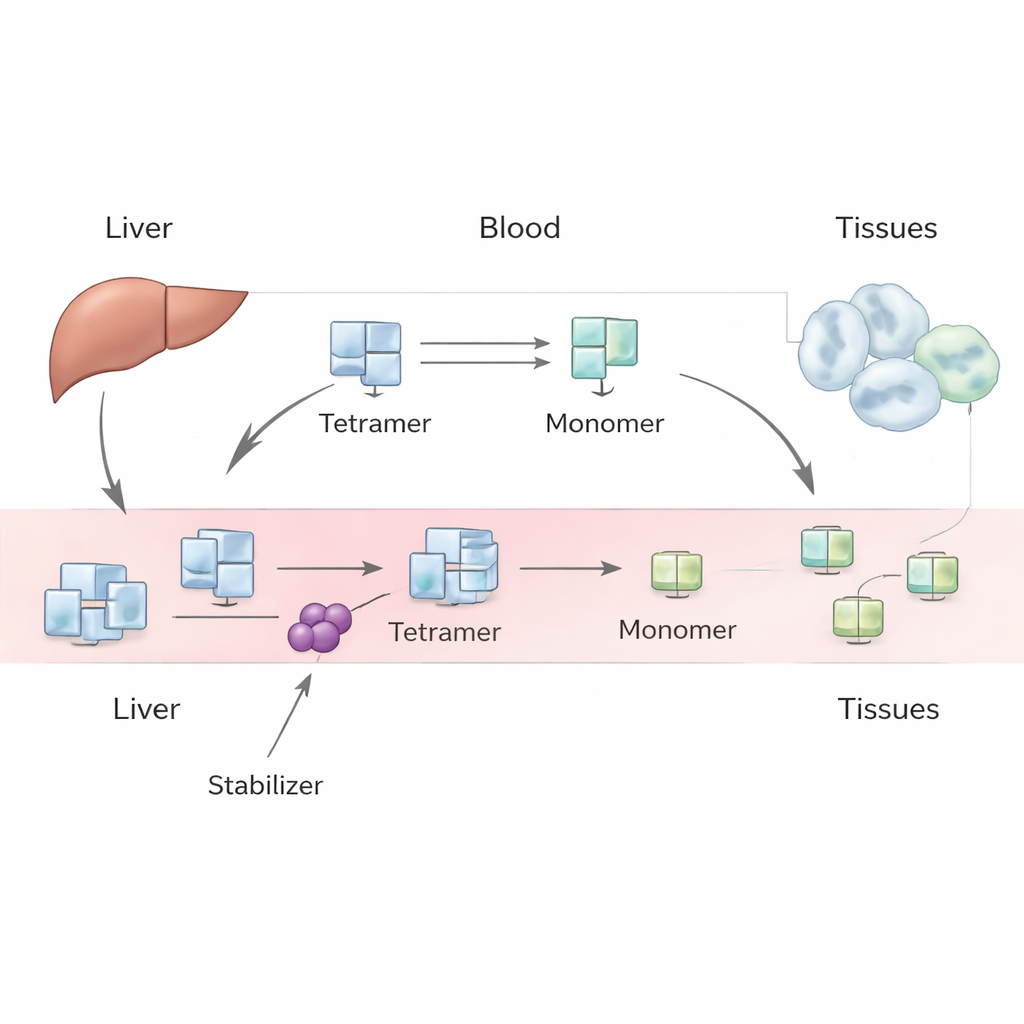
Uma proteína que pode ajudar ou prejudicar
A TTR é produzida principalmente no fígado e normalmente circula no sangue como um conjunto estável de quatro subunidades idênticas, conhecido como tetrâmero. Ela transporta hormônio tireoidiano e vitamina A. Em certas condições, incluindo envelhecimento ou variantes genéticas herdadas, esse tetrâmero pode se separar em subunidades únicas, ou monômeros. Esses monômeros podem se dobrar de forma inadequada e se agregar em fibrilas amiloides, que danificam tecidos e levam à amiloidose por transtirretina no coração (cardiomiopatia) ou nos nervos (neuropatia). Drogas como tafamidis e acoramidis foram projetadas para se ligar ao tetrâmero e dificultar sua dissociação, retardando a progressão da doença. Porém, quando os pacientes começam esses medicamentos, os níveis medidos de TTR no sangue aumentam de forma consistente, e esse aumento é maior do que experimentos simples de laboratório sugeririam.
Construindo um quadro simples de um sistema complexo
Os autores enfrentam esse enigma com um modelo fenomenológico — que se concentra no comportamento observável global em vez de em cada detalhe microscópico. Em seu enquadramento, o fígado produz tetrâmeros de TTR a uma taxa constante, que então entram na corrente sanguínea. Uma vez em circulação, os tetrâmeros podem se dissociar em monômeros e se reorganizar, e tanto tetrâmeros quanto monômeros podem ser removidos do sangue por captação nos tecidos e degradação. Escrevendo um par de equações de balanço de massa para tetrâmeros e monômeros, a equipe explora diferentes cenários: um em que os monômeros maiormente retornam a tetrâmeros, outro em que são rapidamente removidos, e um caso intermediário em que ambos os processos importam. Eles usam estudos históricos em humanos com traçadores e dados laboratoriais modernos para estimar quantidades-chave, como a rapidez com que tetrâmeros são eliminados, a velocidade de sua dissociação e o quanto os medicamentos retardam essa quebra.
Por que apenas estabilizar o tetrâmero não é suficiente
Munidos dessas estimativas, os pesquisadores fazem uma pergunta direta: se um medicamento pudesse impedir perfeitamente que tetrâmeros se desintegrassem, o quanto os níveis de TTR no sangue aumentariam? Em todos os regimes plausíveis, a resposta é modesta — na ordem de 15% no máximo para valores de parâmetros típicos, e muitas vezes menos, dependendo de como os monômeros são eliminados. Isso está muito aquém do aumento >30% observado em pacientes tratados. A discrepância persiste mesmo permitindo ampla incerteza nos parâmetros conhecidos. O modelo, portanto, sugere que simplesmente desacelerar a quebra do tetrâmero não pode, por si só, explicar o efeito clínico completo. Outros processos que controlam com que rapidez a TTR é produzida, captada pelas células ou degradada também devem estar mudando quando os medicamentos estabilizadores estão presentes. 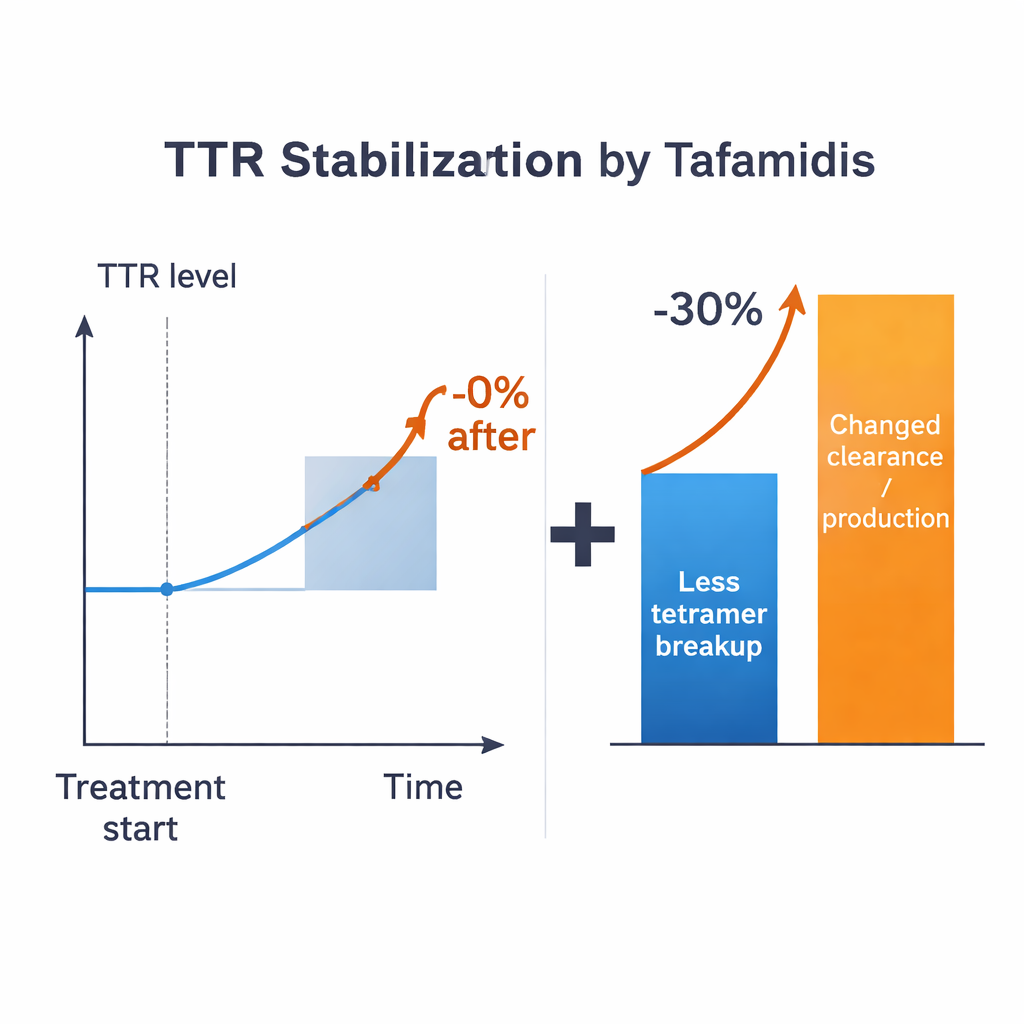
Pistas a partir dos níveis de droga e experimentos inteligentes
Para conectar a exposição ao fármaco ao comportamento da TTR, os autores combinam um modelo farmacocinético básico do tafamidis (como o medicamento se move pelo corpo ao longo do tempo) com ensaios especializados de “troca de subunidades”. Nesses experimentos, tetrâmeros de TTR marcados e não marcados são misturados em plasma humano, e a troca gradual de subunidades revela com que frequência os tetrâmeros se desfazem. Medir esse processo em diferentes concentrações de droga fornece uma ligação direta e orientada por dados entre o nível de tafamidis e a estabilidade efetiva do tetrâmero, sem precisar saber quanto do fármaco está ligado à albumina ou ao hormônio tireoidiano. Essa ligação fenomenológica alimenta o modelo e contorna de maneira elegante muitas incógnitas bioquímicas. Ainda assim, mesmo com essa vantagem, os cálculos limitam o aumento esperado de TTR a cerca da metade do incremento observado clinicamente, reforçando a ideia de que alterações na depuração, internalização, degradação ou mesmo na síntese devem fazer parte da explicação.
O que isso significa para o futuro
Para não especialistas, a mensagem principal é que esses medicamentos estabilizadores provavelmente fazem mais do que apenas “colar” os tetrâmeros de TTR. Eles provavelmente também afetam como o organismo produz, remove ou recicla a proteína. Os autores argumentam que modelos simples e transparentes como o deles são poderosos porque expõem lacunas no nosso entendimento e indicam experimentos concretos — por exemplo, medir diretamente a velocidade de eliminação dos monômeros, com que rapidez diferentes formas de TTR são captadas pelas células, ou se a TTR ligada ao fármaco é tratada de maneira distinta da proteína não ligada. Respostas melhores a essas perguntas não apenas refinariam o tratamento da amiloidose por transtirretina, mas também poderiam revelar regras gerais sobre outras doenças nas quais proteínas normais se transformam em agregados prejudiciais.
Citação: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Palavras-chave: amiloidose por transtirretina, estabilização de proteínas, tafamidis, modelagem farmacocinética, doenças amiloides