Clear Sky Science · pt
Estabilização direcionada do fator induzível por hipóxia 1‑alfa (HIF1A) durante a maturação in vitro de complexos cúmulo‑óvulo bovinos aumenta as taxas de blastocisto
Por que ajustar a detecção de oxigênio nos óvulos importa
A pecuária moderna depende amplamente de embriões produzidos em laboratório, mas o sucesso está longe de ser garantido: apenas cerca de um terço dos oócitos atinge o estágio crucial de blastocisto, quando estão prontos para serem transferidos para uma vaca. Este estudo aborda uma pergunta aparentemente simples, com ampla relevância para melhoramento animal e reprodução assistida: se imitarmos mais de perto as condições de baixo oxigênio que os óvulos experimentam naturalmente dentro do ovário — aumentando suavemente uma proteína chave que detecta oxigênio — conseguimos ajudar mais embriões a se desenvolverem com sucesso?
A vida começa em um nicho de baixa oxigenação
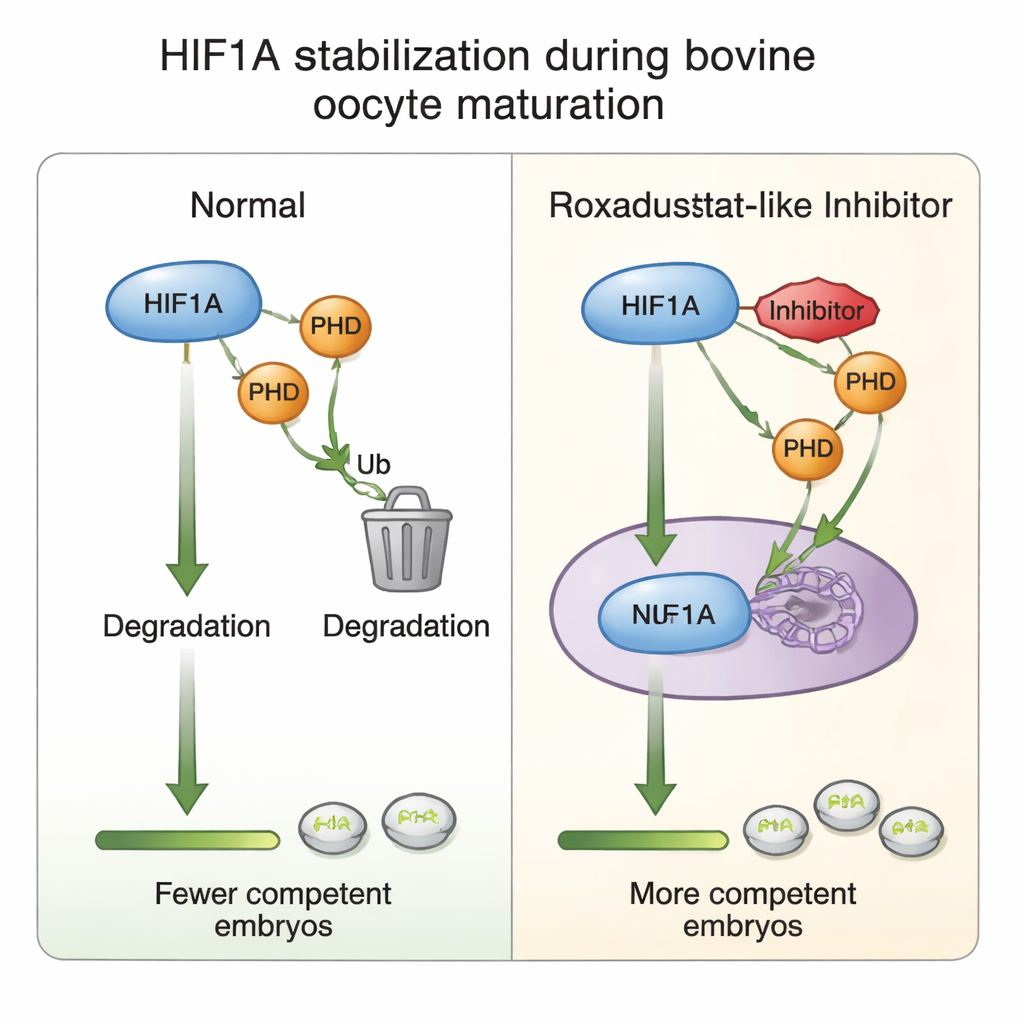
Dentro do ovário, cada óvulo em desenvolvimento está envolto por um grupo de células de suporte conhecido como cúmulo, formando em conjunto o complexo cúmulo‑oócito. Embora o suprimento sanguíneo do ovário aumente conforme os folículos crescem, os vasos sanguíneos não alcançam as vizinhanças imediatas do óvulo. O oxigênio precisa difundir, criando um bolsão levemente hipóxico ao redor do óvulo em maturação. Nesse nicho, um sensor intracelular chamado HIF1A ajuda as células a se adaptarem ajustando o metabolismo e a produção hormonal. Trabalhos anteriores mostraram que bloquear o HIF1A prejudica a maturação do óvulo e reduz drasticamente a formação de embriões, destacando essa proteína como um coordenador central da competência do óvulo — a capacidade do óvulo de ser fecundado e desenvolver‑se em um embrião saudável.
Usando um medicamento para afinar o sensor de oxigênio do óvulo
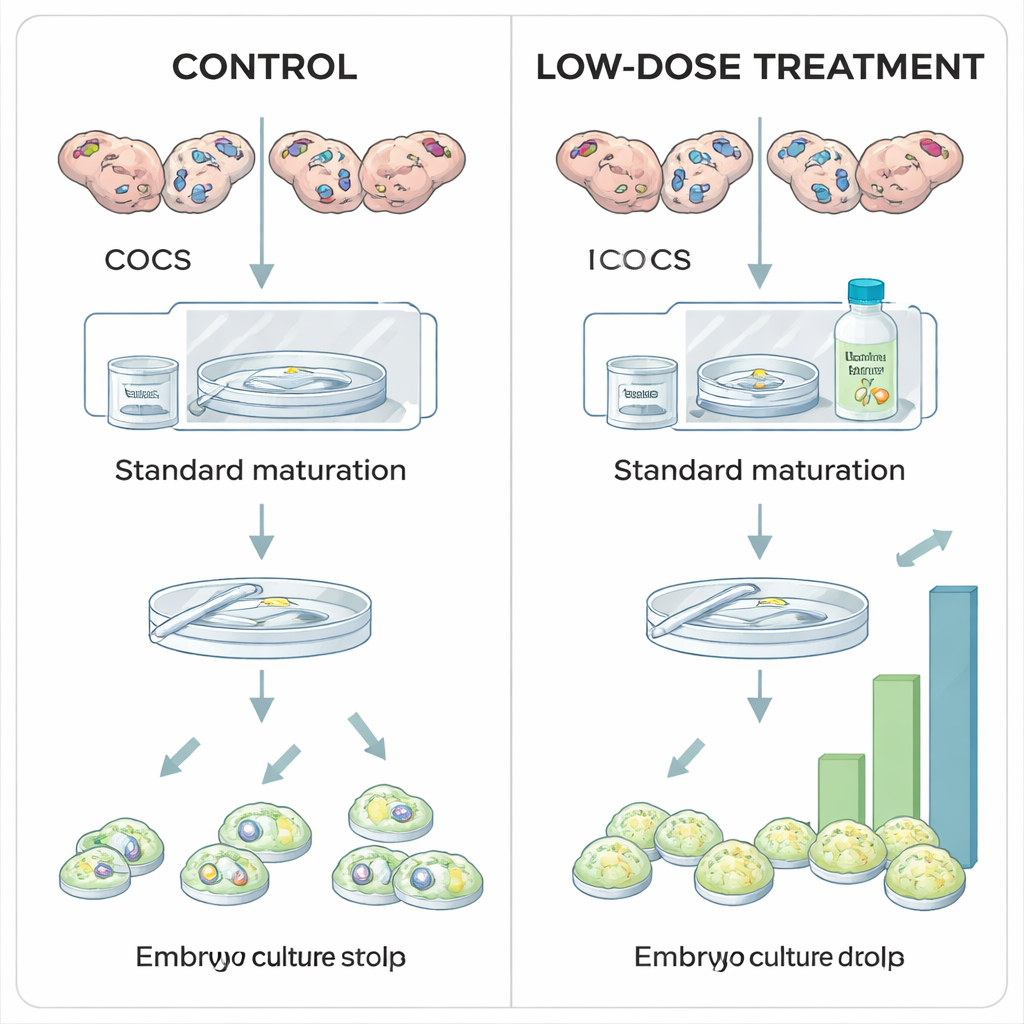
Os pesquisadores investigaram se a estabilização moderada do HIF1A durante a maturação laboratorial de oócitos bovinos poderia aumentar a produção de embriões. Em protocolos in vitro padrão, os complexos cúmulo‑oócito são maturados sob níveis de oxigênio do ar ambiente, em grande parte por razões práticas e não biológicas. Aqui, oócitos coletados de ovários de abatedouro foram divididos em grupos e expostos durante o período de maturação de 24 horas a diferentes doses de Roxadustat, um fármaco já usado na medicina humana para tratar anemia. O Roxadustat atua bloqueando uma família de enzimas chamadas prolil hidroxilases (PHDs) que, normalmente, marcam o HIF1A para degradação quando o oxigênio é abundante. Ao inibir as PHDs, o Roxadustat permite o acúmulo da proteína HIF1A mesmo em níveis mais altos de oxigênio, recriando parcialmente o sinal de hipóxia que o óvulo percebe in vivo.
Mais blastocistos na dose certa, dano em níveis mais altos
Quando a equipe examinou como os oócitos e embriões se saíram após o tratamento, um padrão claro surgiu. Uma baixa dose de Roxadustat (25 micromolar) não alterou quantos oócitos completaram a maturação nem quantos oócitos fecundados iniciaram a divisão, mas aumentou significativamente a proporção que alcançou o estágio de blastocisto. Em outras palavras, as etapas iniciais não foram afetadas, mas mais embriões concluíram com sucesso a jornada exigente até se tornarem blastocistos — sugerindo que a estabilização moderada de HIF1A melhora a qualidade intrínseca do oócito. Em contraste, a dose mais alta (100 micromolar) reduziu a porcentagem de oócitos que maturaram, e quando o mesmo inibidor foi aplicado mais tarde, durante o período de cultivo embrionário de oito dias, doses altas cortaram drasticamente a formação de blastocistos sem alterar a divisão celular inicial. Esses achados indicam que “o suficiente” de atividade de HIF1A durante a maturação é benéfico, enquanto quantidades excessivas ou ativação prolongada são prejudiciais.
O que acontece dentro das células de suporte do óvulo
Para entender como esse ajuste químico funciona, os autores investigaram as células do cúmulo que envolvem cada óvulo. Eles descobriram que a maturação, em geral, aumenta a atividade do gene HIF1A, mas a adição de Roxadustat paradoxalmente diminuiu o RNA mensageiro de HIF1A enquanto mantinha os níveis da proteína HIF1A estáveis — uma pista de que as células podem reduzir a produção gênica depois que a proteína está suficientemente estabilizada, uma espécie de freio interno contra a superativação. Os níveis de PHD2, a mais sensível ao oxigênio entre as enzimas PHD, aumentaram em resposta ao fármaco, reforçando seu papel como parte do circuito de detecção de oxigênio. Em doses mais altas do fármaco, marcadores de proliferação celular e da matriz adesiva que ajuda as células do cúmulo a se expandirem ao redor do óvulo foram reduzidos, em consonância com o declínio observado na maturação e na formação de embriões. Tudo isso apoia a ideia de que a atividade de HIF1A cuidadosamente equilibrada ajusta a comunicação entre o óvulo e as células do cúmulo que sustenta o sucesso do desenvolvimento posterior.
Implicações para o melhoramento animal e além
Este trabalho mostra que estabilizar levemente o sensor de oxigênio do óvulo durante a breve janela de maturação in vitro pode aumentar e tornar mais estáveis as taxas de blastocisto em bovinos, sem alterar a fertilização ou as clivagens iniciais. Em termos práticos, isso pode se traduzir em uma produção de embriões mais confiável para programas de melhoramento, usando um fármaco direcionado em vez de mudanças grosseiras nos níveis de oxigênio ou produtos químicos mais tóxicos. O estudo também ressalta uma lição mais ampla, relevante para tratamentos de fertilidade humana: imitar o ambiente nuanceado e de baixa oxigenação do ovário não é simplesmente uma questão de aumentar ou diminuir o oxigênio, mas de respeitar o delicado equilíbrio de moléculas sinalizadoras como o HIF1A. Afinar esse equilíbrio, em vez de levá‑lo a extremos, pode ser uma rota chave para embriões mais saudáveis.
Citação: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Palavras-chave: produção de embriões in vitro, maturação do oócito, sinalização por hipóxia, estabilização de HIF1A, reprodução bovina