Clear Sky Science · pt
Rumo a gêmeos digitais da eletrofisiologia cardíaca com um solucionador escalável de código aberto eficiente em clusters de GPU
Por que construir corações virtuais importa
Quando os médicos tratam problemas do ritmo cardíaco, frequentemente atuam parcialmente às cegas: conseguem medir sinais elétricos na superfície do corpo, mas não conseguem ver facilmente como esses sinais se propagam profundamente dentro do coração. Este estudo descreve novas ferramentas computacionais poderosas que podem simular o batimento de um coração em detalhe, rápido o bastante para explorar muitos cenários “e se”. Ao combinar anatomia cardíaca realista com processadores gráficos de ponta, os autores nos aproximam de experimentos virtuais seguros e de baixo custo em cópias digitais dos corações de pacientes individuais.
De modelos simples a gêmeos digitais
Simulações cardíacas modernas podem representar a atividade desde o nível de células individuais até o órgão inteiro, mas reproduzir fielmente como a eletricidade se move pelo coração é matematicamente complexo e computacionalmente custoso. Um objetivo central para a medicina é o “gêmeo digital cardíaco”: um modelo computacional personalizado que imite o coração de um paciente específico e possa ser usado para testar medicamentos, dispositivos ou estratégias de estimulação antes de serem aplicados na clínica. Para viabilizar isso, o software que executa essas simulações deve ser rápido e preciso, deve incluir estruturas anatômicas importantes e deve ser disponibilizado abertamente para que pesquisadores no mundo todo possam checar, melhorar e reutilizar o código.
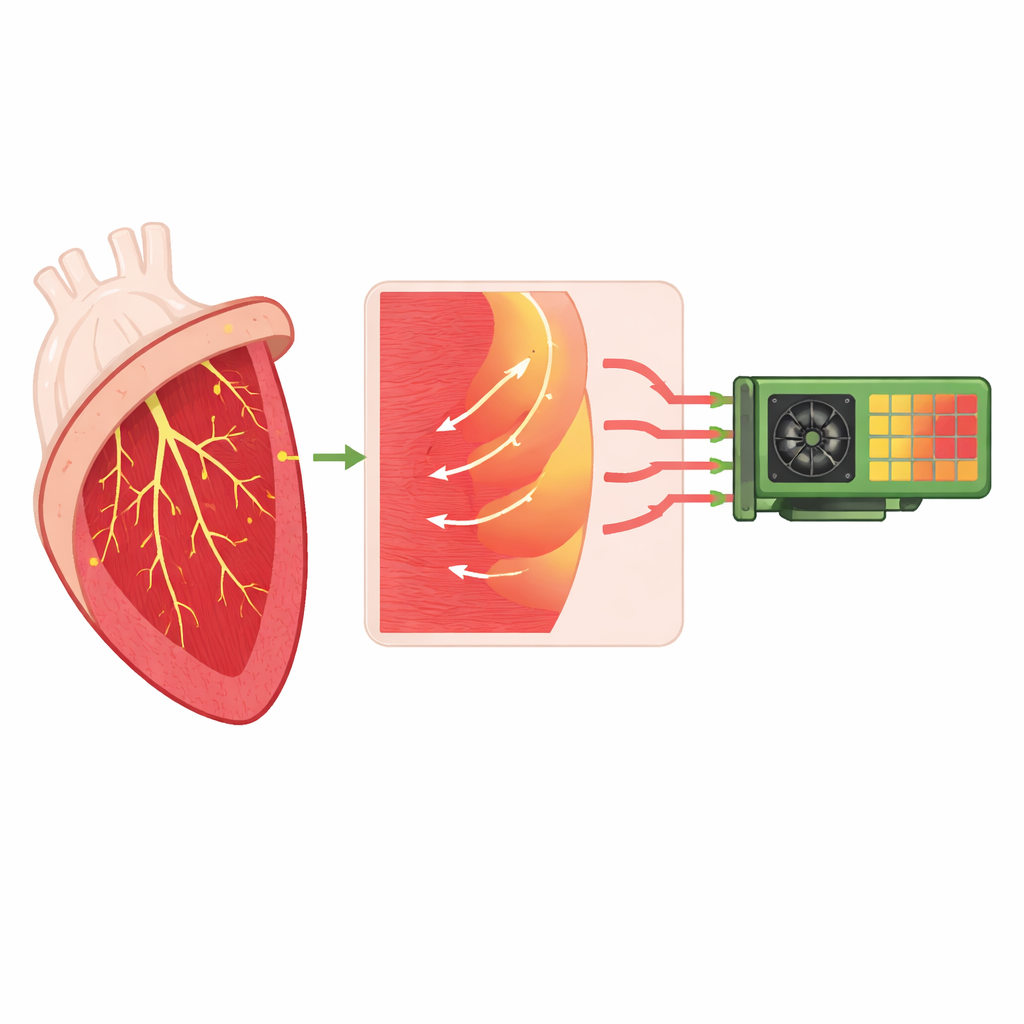
Capturando a fiação oculta do coração
O trabalho se concentra em um simulador de código aberto chamado monoalg3d, que modela como os sinais elétricos percorrem o músculo cardíaco e sua rede de fiação especializada. Essa rede, conhecida como sistema de Purkinje, entrega rapidamente o sinal que dispara o batimento das vias de condução superiores para muitos pontos de conexão minúsculos distribuídos pela superfície interna dos ventrículos. Em cada uma dessas junções, uma fibra de Purkinje fina precisa excitar uma massa muito maior de músculo cardíaco, introduzindo um atraso natural e, em certas condições, um risco de bloqueio ou condução anormal. Os autores aprimoram o monoalg3d para representar essa fiação e suas junções de forma mais realista, incluindo a assimetria entre sinais que vão de Purkinje para o músculo e os que retornam do músculo para a rede.
Transformando supercomputadores e GPUs em laboratórios cardíacos
Para executar modelos tão detalhados rapidamente, a equipe reengenharia como o simulador utiliza o hardware. Redesenharam o núcleo numérico para que tanto a dinâmica local das células quanto a propagação de voltagem através do coração sejam resolvidas diretamente nas unidades de processamento gráfico (GPUs), dispositivos originalmente criados para renderizar imagens e agora amplamente usados em computação científica. Ao organizar cuidadosamente os dados para bibliotecas de GPU e evitando transferências frequentes entre CPU e GPU, mostram que uma configuração totalmente baseada em GPU pode acelerar um benchmark padrão em quase onze vezes em comparação com uma versão tradicional somente em CPU. Também introduzem um novo formato de saída compacto para reduzir drasticamente as necessidades de armazenamento e um recurso de passagem de mensagens que pode lançar centenas de simulações em paralelo em um supercomputador, cada uma explorando um conjunto diferente de parâmetros fisiológicos.
Ensinar corações virtuais a corresponder a pacientes reais
Além da velocidade bruta, os autores testam se seu solucionador aprimorado pode sustentar simulações realistas específicas de pacientes. Usando uma reconstrução tridimensional de um coração humano a partir de imagens médicas, eles anexam uma rede sintética de Purkinje e ajustam parâmetros-chave das junções: a resistência em cada conexão e quantas regiões musculares vizinhas cada terminal de Purkinje excita. Eles varrem automaticamente centenas de combinações desses valores, rodando simulações que começam a partir de um estímulo no feixe de condução principal, e medem tanto os pequenos atrasos em cada junção quanto os sinais de eletrocardiograma (ECG) resultantes no tórax. Para uma malha cardíaca de alta resolução, identificam escolhas de parâmetro que produzem tempos de ativação fisiologicamente plausíveis e traçados de ECG que se correlacionam bem com gravações de um paciente real, tudo mantendo tempos individuais de simulação dentro de algumas horas mesmo quando 512 execuções são realizadas simultaneamente.
Muitos corações possíveis que parecem iguais externamente
Um resultado intrigante é que diferentes configurações internas de fiação e forças nas junções podem levar a ECGs muito semelhantes na superfície do corpo. Em outras palavras, vários corações digitais distintos podem parecer igualmente consistentes com os mesmos dados clínicos. Os autores mostram que algumas junções de Purkinje são especialmente influentes, com seus atrasos locais variando substancialmente entre simulações igualmente bem ajustadas, enquanto o tempo geral de ativação através dos ventrículos permanece estável. Essa não unicidade sugere que futuros frameworks de gêmeos digitais precisarão de dados ou restrições adicionais — como imagens mais detalhadas ou medições invasivas — para determinar uma única configuração interna mais provável para um dado paciente.
O que isso significa para o cuidado futuro
Em resumo, este estudo entrega um simulador acelerado por GPU, de livre acesso, capaz de lidar com anatomia cardíaca detalhada, fiação de condução realista e grandes lotes de simulações personalizadas em clusters de computação modernos. Para não especialistas, a mensagem chave é que está se tornando prático executar experimentos virtuais cardíacos rápidos e de alta fidelidade que se assemelham a pacientes individuais, incluindo atrasos sutis nas junções da fiação interna do coração. Embora mais trabalho seja necessário para personalizar totalmente esses modelos e resolver incertezas internas, as ferramentas aqui introduzidas formam um bloco de construção importante para o futuro diagnóstico, avaliação de risco e planejamento de tratamento em cardiologia baseado em gêmeos digitais.
Citação: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
Palavras-chave: gêmeo digital cardíaco, simulação da eletrofisiologia do coração, sistema de condução de Purkinje, computação em GPU, cardiologia personalizada