Clear Sky Science · pt
Diagnóstico assistido por computador da encefalopatia bilirrubínica aguda neonatal com imagens de RM multimodais e redes neurais convolucionais
Por que isso importa para recém-nascidos e suas famílias
A icterícia é comum em recém-nascidos e geralmente é inofensiva, mas em alguns bebês o acúmulo de um pigmento amarelo chamado bilirrubina pode lesar silenciosamente o cérebro. Os médicos têm dificuldade em discernir, apenas por exames de imagem e de sangue, quais bebês ictéricos correm risco real. Este estudo investiga se ferramentas computacionais inteligentes podem interpretar exames cerebrais com mais precisão que o olhar humano, ajudando os médicos a proteger os bebês de sequelas permanentes ao mesmo tempo em que evitam alarmes e tratamentos desnecessários.
O perigo oculto por trás da icterícia neonatal
A maioria dos bebês desenvolve algum grau de icterícia enquanto seus fígados imaturos aprendem a eliminar a bilirrubina do sangue. Quando os níveis de bilirrubina ficam muito altos, o pigmento pode infiltrar-se em estruturas profundas e sensíveis do cérebro e desencadear uma condição chamada encefalopatia bilirrubínica aguda, que pode levar a problemas motores, auditivos e de aprendizagem a longo prazo se não for tratada a tempo. A dificuldade é que lesões cerebrais precoces podem ser sutis e reversíveis, e os escores clínicos e exames laboratoriais atuais são imperfeitos. A ressonância magnética (RM) oferece uma janela não invasiva para o cérebro do recém-nascido, mas mesmo especialistas frequentemente acham que bebês acometidos e não acometidos parecem surpreendentemente semelhantes nas imagens padrão.
Olhando o cérebro com mais de um par de lentes
A RM tradicional para esses bebês foca principalmente em um tipo de imagem, conhecido como sequência ponderada em T1, onde o globo pálido — uma pequena região profunda envolvida no movimento — pode aparecer incomumente brilhante quando lesionado pela bilirrubina. Trabalhos anteriores mostraram que interpretar apenas essas imagens, mesmo com medidas computacionais simples ou modelos iniciais de aprendizado profundo, deixava ampla margem para erro. Os autores supuseram que outras “variações” de RM, como imagens ponderadas em T2 e mapas baseados em difusão que rastreiam o movimento da água pelo tecido cerebral, poderiam conter pistas adicionais. Em vez de pedir aos médicos que medíssem manualmente regiões específicas, eles propuseram alimentar a riqueza completa desses três tipos de imagem em algoritmos modernos de reconhecimento de imagem.
Ensinando computadores a identificar lesão cerebral precoce
A equipe de pesquisa coletou exames cerebrais de 150 recém-nascidos com níveis elevados de bilirrubina: metade apresentava sinais de envolvimento cerebral agudo e metade não. Para cada bebê, foram obtidas três séries de RM — T1, T2 e um mapa baseado em difusão chamado coeficiente aparente de difusão (ADC). Primeiro, as imagens foram cuidadosamente alinhadas e recortadas para que permanecesse apenas o cérebro, depois redimensionadas e normalizadas em brilho para que pudessem ser processadas por softwares padrão de análise de imagem. Os cientistas testaram duas estratégias amplas. Uma baseou-se em um método clássico de aprendizado de máquina chamado máquina de vetor de suporte, usando razões simples de brilho calculadas manualmente entre uma estrutura profunda vulnerável (globo pálido) e a substância branca adjacente. A outra utilizou poderosos modelos de aprendizado profundo, InceptionV3 e EfficientNetB0, que aprendem suas próprias características visuais diretamente das imagens brutas.
Combinar tipos de exame oferece a imagem mais clara
Quando a equipe comparou os métodos, a abordagem mais simples, com medidas manuais, melhorou um pouco quando vários tipos de exame foram combinados, mas seu melhor desempenho ainda ficou aquém do que seria confortável para decisões clínicas. Em contraste, os modelos de aprendizado profundo melhoraram dramaticamente à medida que mais tipos de RM foram fundidos. Ao empilhar imagens T1, T2 e ADC como três canais de cor em uma fotografia, a rede com melhor desempenho (InceptionV3) distinguiu corretamente bebês acometidos dos não acometidos em mais de 96% dos casos, com uma medida de poder discriminativo quase perfeita. Mapas visuais das regiões que a rede utilizou mostraram que ela se concentrava nas mesmas áreas cerebrais profundas — globo pálido, núcleos subtalâmicos e hipocampo — que especialistas humanos consideram mais vulneráveis à lesão por bilirrubina, sugerindo que o computador estava aprendendo padrões clinicamente significativos em vez de peculiaridades aleatórias.
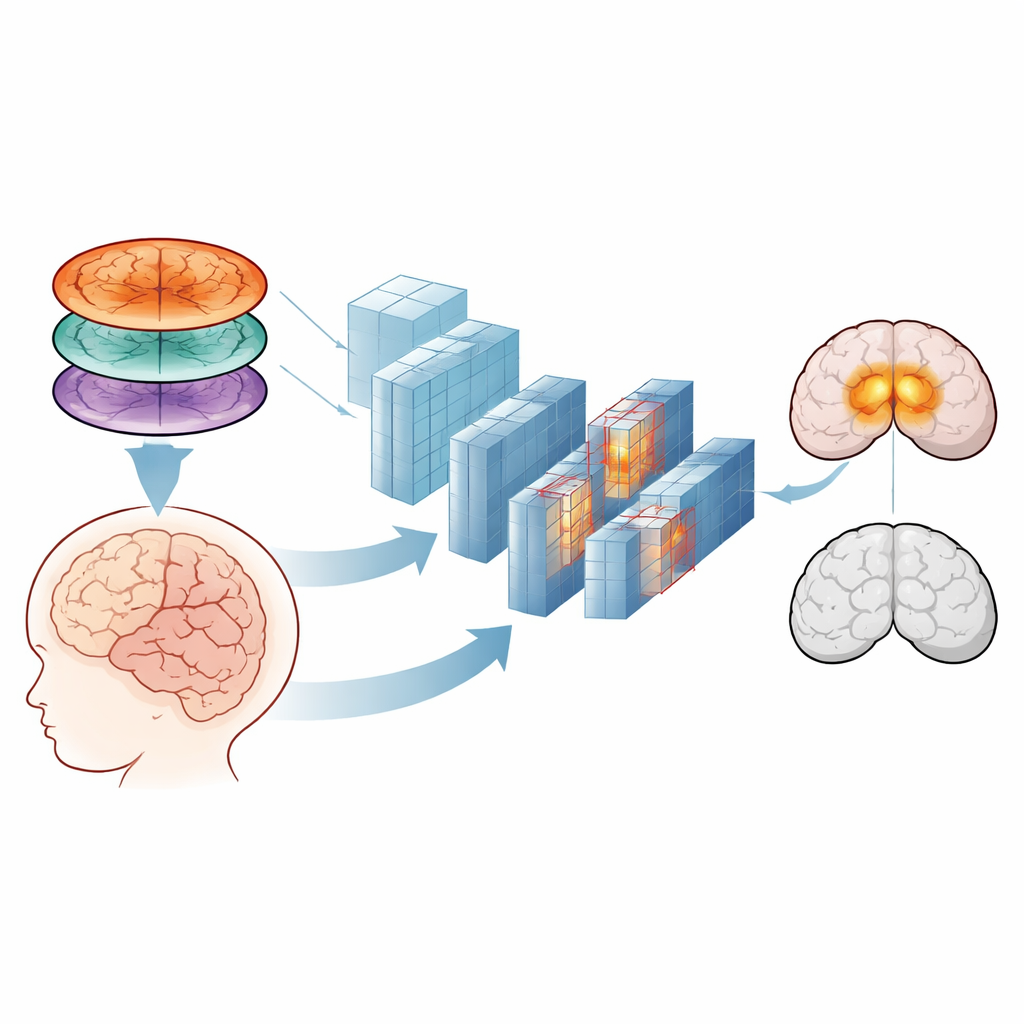
De ferramenta de pesquisa a auxiliar à beira do leito
O estudo conclui que um sistema de diagnóstico assistido por computador cuidadosamente treinado, alimentado com vários tipos complementares de RM em vez de uma única sequência, pode sinalizar com impressionante precisão lesão cerebral precoce relacionada à bilirrubina em recém-nascidos. Embora o trabalho tenha sido realizado em um único hospital e ainda enfrente obstáculos como sobreajuste e a necessidade de testes em grupos maiores e mais diversos de bebês, aponta para um futuro no qual algoritmos avançados de leitura de imagem atuem como um segundo par de olhos para pediatras e radiologistas. Usadas com prudência, essas ferramentas poderiam ajudar a identificar quais bebês ictéricos precisam de tratamento urgente — e, igualmente importante, tranquilizar famílias quando o cérebro do bebê provavelmente está seguro.
Citação: Wu, M., Liu, Q. Computer-aided diagnosis of neonatal acute bilirubin encephalopathy with multi-modal MRI images and convolutional neural networks. Sci Rep 16, 9611 (2026). https://doi.org/10.1038/s41598-025-33337-4
Palavras-chave: icterícia neonatal, encefalopatia bilirrubínica, RM cerebral, aprendizado profundo, diagnóstico assistido por computador