Clear Sky Science · pt
Intermediários G-quádruplex teloméricos revelados por análise complexa de redes de Markov
Nós ocultos nas extremidades do nosso DNA
Nas pontas de nossos cromossomos existem tampas protetoras chamadas telômeros, muitas vezes comparadas às ponteiras plásticas dos cadarços. Nessas regiões, o DNA pode se organizar em nós incomuns de quatro fitas conhecidos como G-quádruplexos. Essas pequenas estruturas podem influenciar o comportamento de nossos genes e o modo como as células envelhecem ou se tornam cancerosas. Este estudo espreita os bastidores de como um desses nós se desfaz gradualmente, usando simulações computacionais detalhadas e análise de dados avançada para revelar formas fugazes que são quase impossíveis de capturar em experimentos.
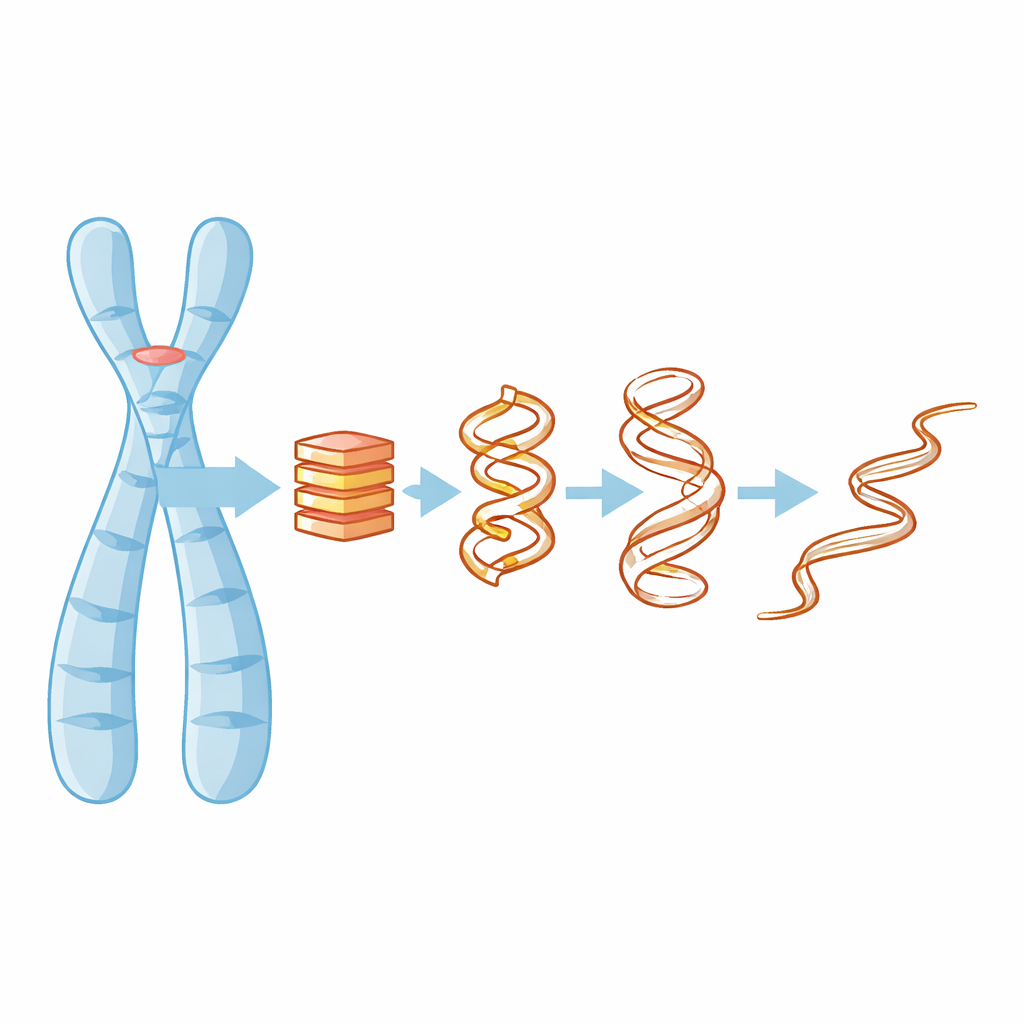
Por que os nós de DNA de quatro fitas importam
A maioria de nós aprende que o DNA é uma dupla hélice, mas em trechos ricos em guanina — como os presentes nos telômeros — a molécula pode se dobrar em pilhas compactas de quatro fitas chamadas G-quádruplexos. Essas pilhas são mantidas unidas por camadas planas de bases guanina e por pequenos íons carregados positivamente, como o potássio, que se acomodam no centro e ajudam a colar tudo. Quando um G-quádruplex se forma ou se desfaz, ele pode bloquear ou expor partes do genoma, afetando a atividade gênica, a replicação do DNA e até como células cancerosas mantêm seus telômeros. Entender como essas estruturas perdem sua forma é, portanto, fundamental para descobrir como direcioná-las com fármacos ou prever quando podem falhar.
Observando um nó molecular se desfazer
Os pesquisadores focaram em um G-quádruplex telomérico humano no qual quatro segmentos de uma única fita de DNA se alinham em paralelo e empilham-se em uma coluna compacta. Eles usaram simulações de dinâmica molecular com todos os átomos — experimentos virtuais que acompanham o movimento de cada átomo — para aquecer oito cópias dessa estrutura a temperaturas próximas ao seu ponto de fusão. Para ajudar o sistema a explorar diferentes conformações, usaram uma estratégia chamada replica exchange, na qual simulações em temperaturas distintas trocam configurações ocasionalmente. Em sete dos oito casos o G-quádruplex permaneceu intacto; em um, ele se desdobrou completamente. Esse raro evento de desdobramento tornou-se um estudo de caso detalhado, mostrando não apenas o antes e o depois, mas toda uma sequência de formas intermediárias ao longo do processo.
O papel crucial dos pequenos íons
Uma descoberta central é que os pequenos íons dentro do G-quádruplex agem como pivôs. Enquanto ao menos um íon permanecer aninhado entre as camadas de guanina, a estrutura permanece majoritariamente intacta, talvez um pouco afrouxada, mas ainda reconhecível. Quando ambos os íons finalmente deixam o canal central, contudo, a pilha se desestabiliza rapidamente. As camadas de guanina deformam-se e fitas individuais se desprendem, e o DNA no conjunto torna-se mais estendido e flexível. Outras moléculas simuladas que perderam apenas um íon entraram em estados bambos, mas ainda parcialmente ordenados, sugerindo que o desdobramento completo exige a perda dos dois íons estabilizadores — uma pista do porquê alguns G-quádruplexos são tão teimosamente robustos na célula.
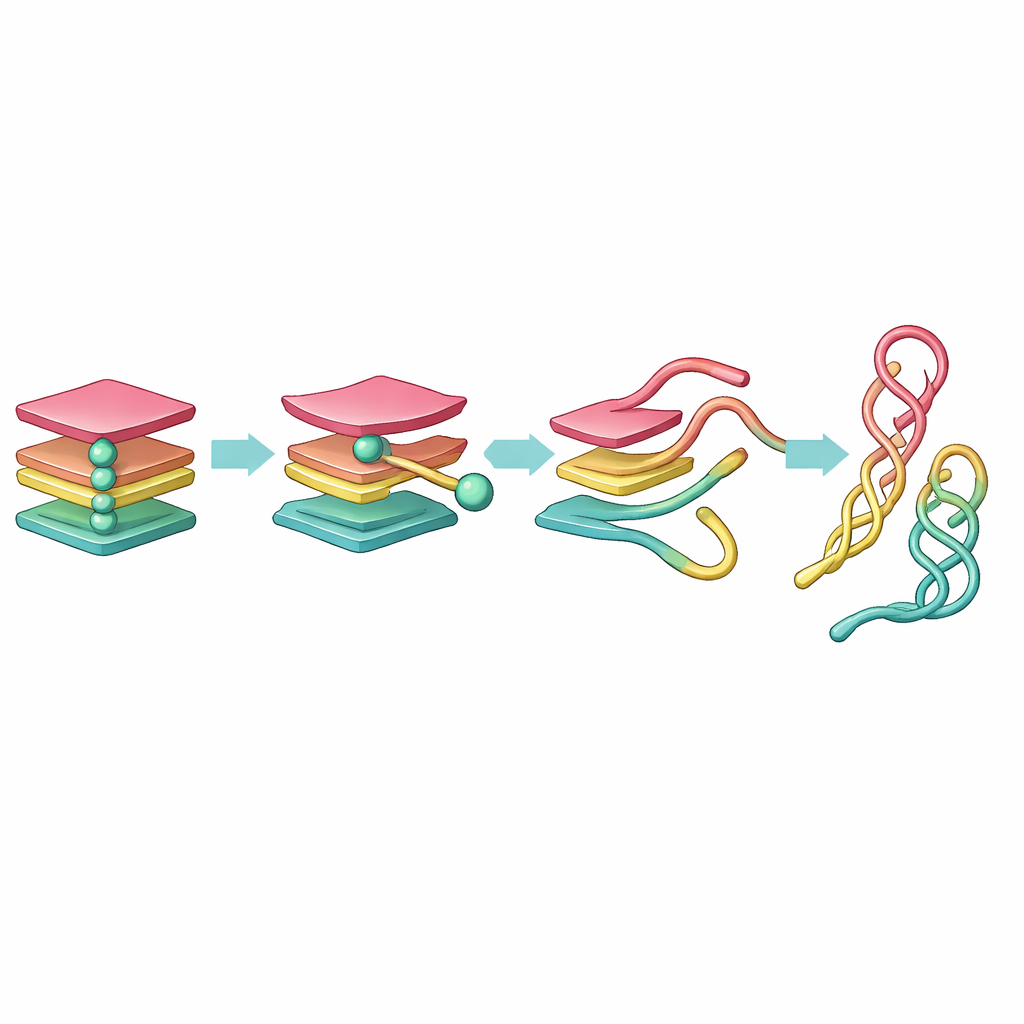
Descobrindo pontos de passagem ocultos na jornada
As simulações brutas produziram uma quantidade enorme de dados, longe de ser interpretável a olho nu. Para domar isso, a equipe primeiro simplificou o DNA representando cada base como uma única esfera, em seguida usou ferramentas matemáticas para reduzir o movimento a apenas algumas coordenadas-chave. Aplicaram dois métodos: Análise de Componentes Principais (PCA), que destaca direções de maior movimento, e Análise de Componentes tempo-independentes (tICA), que filtra as mudanças lentas e de longa duração que marcam verdadeiras transições estruturais. A partir dessas coordenadas reduzidas, construíram as chamadas redes conformacionais de Markov, nas quais cada nó é uma forma típica do DNA e as ligações mostram como a molécula salta de uma conformação para outra.
Uma rota preferida do nó para a fita solta
Essa visão em rede revelou um caminho claro de desdobramento. Partindo de um G-quádruplex totalmente dobrado, uma fita primeiro se destaca, formando um estado tríplice de três fitas, o “triplex”. Esse triplex então se reorganiza em um “hairpin” de duas fitas e em um conjunto de fitas soltas próximas. O hairpin e uma disposição relacionada em “cross-hairpin” mostram-se surpreendentemente duradouros, atuando como pontos de parada estáveis na jornada de um nó apertado para uma configuração de DNA mais relaxada. Enquanto a PCA dividiu essa progressão em muitos estados de aparência similar, a tICA a destilou em um pequeno conjunto de passos distintos e cineticamente significativos, mostrando que formas tipo triplex são de curta duração, enquanto formas tipo hairpin persistem por muito mais tempo.
O que isso significa para a biologia e a medicina
Para um não especialista, a mensagem principal é que os G-quádruplexos teloméricos não simplesmente mudam de dobrados para desdobrados. Em vez disso, eles se desfazem através de uma série de estados de curta e de longa duração, com pequenos íons atuando como guardiões da estabilidade. As simulações sugerem que intermediários de três fitas são fugazes, enquanto hairpins de duas fitas e formas em cruz são pontos de repouso mais estáveis. Como esses estados intermediários também podem surgir na direção inversa, de dobramento, eles provavelmente são cruciais para como os G-quádruplexos se formam, se transformam e interagem com potenciais fármacos. Mapear essa paisagem oculta de formas aproxima os cientistas de projetar moléculas que estabilizem ou desestabilizem seletivamente esses nós de DNA na luta contra o câncer e outras doenças.
Citação: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Palavras-chave: G-quádruplex, DNA telomérico, dinâmica molecular, dobramento de DNA sem proteínas, terapêutica do câncer