Clear Sky Science · pt
Sequenciamento do genoma completo pareado de sangue (10×) e cinco espermatozoides individuais (1×) por indivíduo em 53 homens
Por que este estudo importa para as famílias
Para muitos casais com dificuldade para engravidar, a atenção costuma recair sobre níveis hormonais ou a saúde geral, enquanto os detalhes finos dentro dos espermatozoides permanecem um mistério. Este estudo abre uma nova janela para esses detalhes ao ler cuidadosamente o DNA completo tanto do sangue quanto de espermatozoides individuais em dezenas de homens. Ao combinar essas informações genéticas com medições precisas do movimento dos espermatozoides, os pesquisadores criaram um recurso compartilhado que pode ajudar cientistas no mundo todo a entender melhor a infertilidade masculina e, eventualmente, aprimorar diagnóstico e tratamento.
Observando de perto espermatozoides rápidos e lentos
Homens podem ser inférteis por muitos motivos, mas uma das causas mais comuns é a astenozoospermia, uma condição em que os espermatozoides estão vivos, mas se movem devagar ou com pouca força para alcançar e fertilizar um óvulo. Neste projeto, a equipe recrutou 53 homens Han chineses: 37 com qualidade seminal típica e fertilidade comprovada, e 16 cujos espermatozoides apresentavam movimento reduzido, mas contagens normais. Todos os participantes foram cuidadosamente triados para excluir outros problemas médicos e infecção recente por COVID‑19, para que as diferenças no movimento espermático fossem menos propensas a confusão com doenças não relacionadas. Para cada homem, os médicos registraram um conjunto amplo de dados de saúde, incluindo idade, tamanho corporal, hábitos de tabagismo e consumo de álcool, histórico reprodutivo, níveis hormonais e uma grande gama de medidas seminais, como motilidade total, velocidade de nado e padrões de movimento.
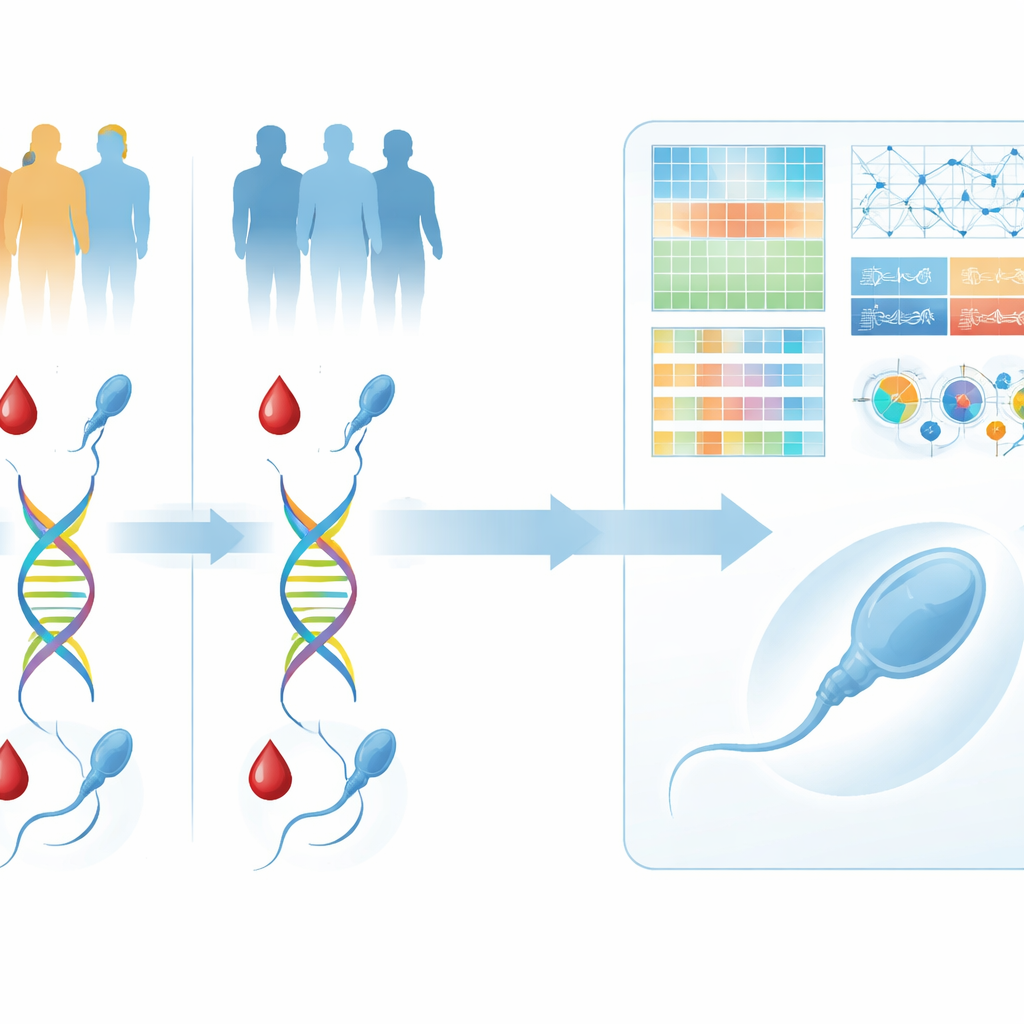
Construindo um mapa de DNA a partir de sangue e espermatozoides individuais
O que diferencia este trabalho é seu foco duplo: os pesquisadores não se limitaram a observar o sêmen ao microscópio, eles também coletaram informação genética completa tanto do sangue quanto de espermatozoides individuais. Amostras de sangue forneceram uma visão do plano genético geral de cada homem com aproximadamente dez vezes de cobertura, o que significa que a maioria das posições no genoma foi lida várias vezes para maior confiabilidade. De cada participante, os técnicos então isolaram cuidadosamente vários espermatozoides únicos, um a um, ao microscópio, evitando aqueles que pareciam obviamente anormais. Essas células únicas foram processadas com um método especializado que consegue copiar e sequenciar quase todo o seu DNA, oferecendo um retrato de baixa, porém utilizável, cobertura do genoma de cada espermatozoide.
Transformando leituras brutas em um recurso de dados de alta qualidade
Por se tratar de um estudo orientado por dados, em vez de um experimento típico com uma hipótese específica, o resultado-chave é a qualidade e a estrutura do próprio conjunto de dados. A equipe verificou a concentração e integridade do DNA, eliminou ruído técnico e certificou-se de que tanto as sequências do sangue quanto dos espermatozoides atendiam aos padrões comuns usados em genética humana. Em média, o DNA do sangue foi lido a uma profundidade pouco acima de dez vezes, enquanto o DNA dos espermatozoides alcançou cerca de 1,7× de cobertura por célula, um nível adequado para detectar padrões em larga escala entre muitas células. Importante, eles confirmaram que níveis hormonais como testosterona e estrogênio eram semelhantes entre homens com espermatozoides lentos e aqueles com fertilidade típica. As diferenças reais residiam em quão bem os espermatozoides se moviam: os homens do grupo fértil apresentaram aproximadamente o dobro da motilidade total e medidas mais altas de trajetória e comportamento de curvas, ressaltando que os dois grupos são distintamente diferentes em função mesmo quando seus perfis hormonais parecem semelhantes.
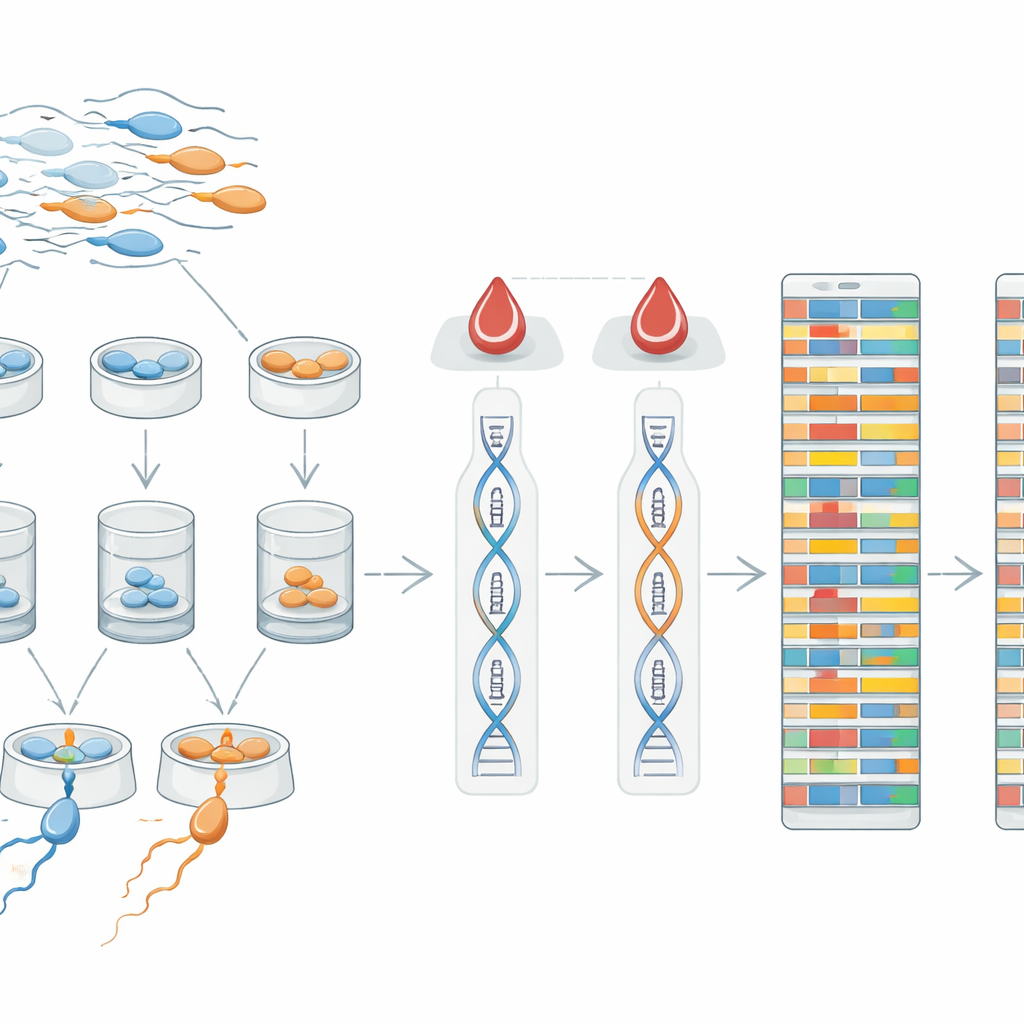
Um novo banco de testes para algoritmos de fertilidade
Tornando todos esses dados publicamente acessíveis, os autores pretendem acelerar o desenvolvimento de métodos em várias áreas de ponta. Como os espermatozoides carregam apenas uma cópia de cada cromossomo, seus genomas oferecem uma maneira limpa de rastrear como o DNA é embaralhado durante a formação dos espermatozoides e como combinações específicas de variantes genéticas podem se relacionar ao desempenho espermático. As sequências pareadas de sangue e espermatozoide também fornecem um benchmark para testar novas ferramentas computacionais que tentam preencher informações faltantes em dados de baixa cobertura ou reconstruir longos trechos de DNA herdado a partir de pistas dispersas. Pesquisadores podem usar este conjunto de dados para aprimorar métodos de detecção de mutações raras, rastreamento de eventos de crossing‑over onde cromossomos parentais trocam segmentos, e comparação de padrões genéticos entre homens com e sem problemas de movimento.
O que isso significa para pacientes no futuro
Para pacientes hoje, esse conjunto de dados ainda não se traduz em um novo teste clínico, nem identifica um único “gene da infertilidade”. Em vez disso, oferece uma base cuidadosamente curada sobre a qual muitos estudos futuros podem se apoiar. Ao combinar medidas detalhadas do comportamento espermático com DNA pareado de células somáticas e espermatozoides individuais, o recurso dá aos cientistas uma plataforma poderosa para explorar como diferenças genéticas sutis podem moldar a fertilidade masculina. Com o tempo, à medida que mais grupos analisarem esses dados e adicionarem os seus, este trabalho pode ajudar a transformar rótulos vagos como “infertilidade masculina inexplicada” em diagnósticos mais claros, informados pelo DNA, e, por fim, orientar escolhas reprodutivas mais personalizadas.
Citação: Chen, W., Yu, L., Li, R. et al. Matched whole-genome sequencing of blood (10×) and five single sperm cells (1×) per individual in 53 men. Sci Data 13, 405 (2026). https://doi.org/10.1038/s41597-026-06808-0
Palavras-chave: infertilidade masculina, motilidade espermática, sequenciamento do genoma completo, genômica de célula única, saúde reprodutiva