Clear Sky Science · pt
Um conjunto de dados de TC com medidas RECIST e máscaras de segmentação abrangentes para tumores e linfonodos
Por que este recurso de imagens do câncer é importante
O tratamento do câncer depende cada vez mais de imagens médicas para decidir se as terapias estão funcionando. Ainda assim, as medições cuidadosas, fatia a fatia, que os médicos fazem em tomografias são demoradas e podem variar entre especialistas. Este artigo apresenta uma nova coleção de tomografias computadorizadas de pacientes com câncer, disponibilizada abertamente, com tumores e linfonodos minuciosamente delineados e medidos segundo um conjunto de normas clínicas amplamente usado. O objetivo é ajudar pesquisadores a desenvolver e testar programas de computador que, no futuro, possam assumir grande parte desse trabalho repetitivo e tornar o acompanhamento do tratamento oncológico mais rápido e consistente globalmente.
Como os médicos atualmente acompanham os tumores
Para avaliar se um tratamento oncológico está sendo eficaz, radiologistas frequentemente seguem um padrão chamado RECIST 1.1. Na prática, isso significa escolher alguns tumores “alvo” nas tomografias do paciente e registrar o maior diâmetro visível de cada um em milímetros. Ao longo do tempo, comparam a soma desses diâmetros com varreduras anteriores para decidir se a doença encolheu, permaneceu estável ou cresceu. Embora essa abordagem tenha trazido ordem necessária aos ensaios clínicos, ela também tem limitações: depende fortemente de quais tumores o médico seleciona, baseia-se em medidas unidimensionais em vez do verdadeiro tamanho 3-D e normalmente leva mais de 10 minutos por paciente a cada avaliação. À medida que os casos de câncer aumentam no mundo, essas restrições pressionam os serviços de radiologia.
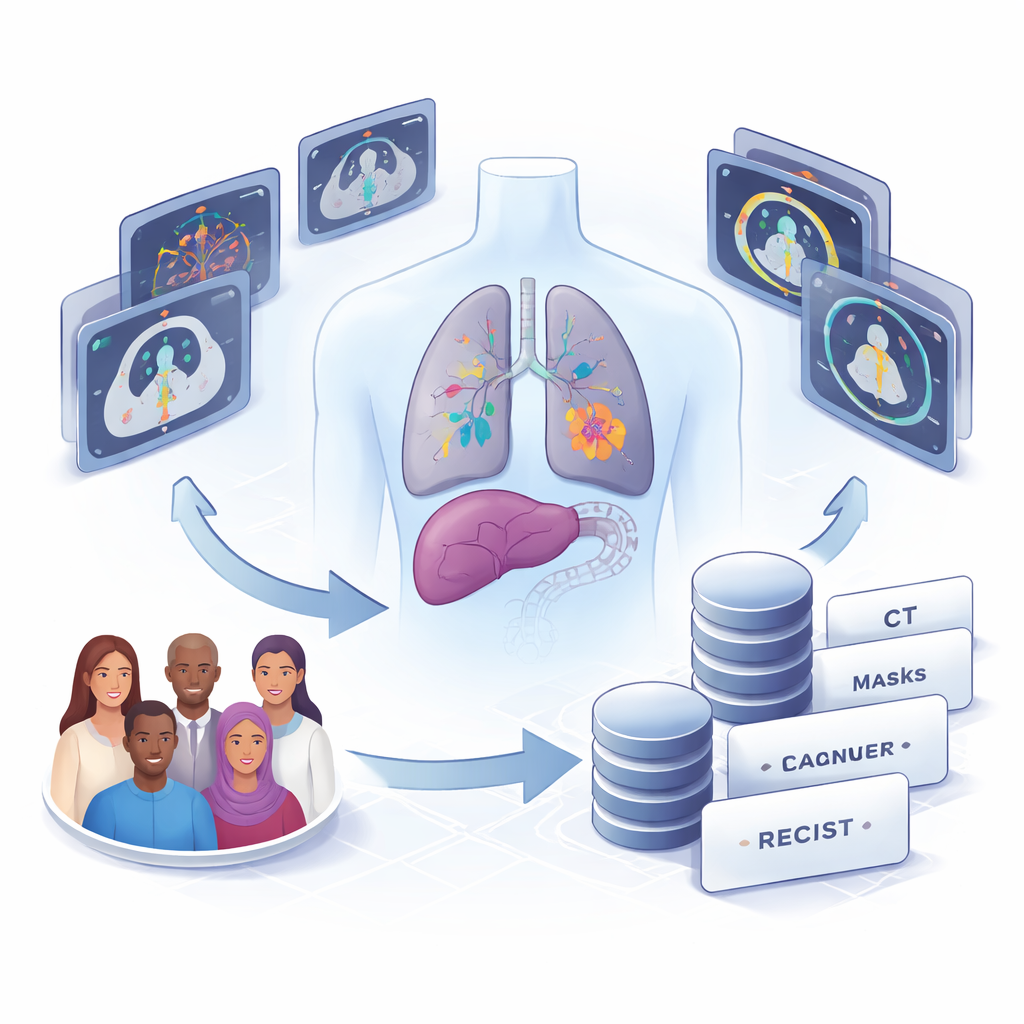
O que o novo conjunto de dados de TC contém
Os autores reuniram tomografias de 22 adultos tratados por diversos tipos de câncer no Hospital Clínico da Universidade do Chile, incluindo cânceres de pulmão, fígado, colorretal, mama, ovário, estômago, vesícula biliar, bexiga e melanoma. A partir de 58 séries de exames torácicos e abdominais realizadas entre 2017 e 2023, eles identificaram todo tumor sólido ou linfonodo aumentado com tamanho suficiente para medição. Ao todo, delinearam manualmente 1.246 lesões individuais: 1.148 metástases (tumores que se espalharam), 93 linfonodos aumentados e 5 tumores primários. Para 82 dessas lesões, também incluíram as medidas RECIST oficiais registradas em relatórios clínicos, permitindo comparação lado a lado entre a prática rotineira e métodos automatizados.
Como especialistas e IA trabalharam juntos
Produzir contornos tão detalhados seria normalmente excessivamente lento, então a equipe usou uma estratégia de “humano no loop”. Radiologistas experientes e residentes desenharam caixas 3-D aproximadas ao redor de tumores suspeitos, e um poderoso modelo de segmentação chamado MedSAM propôs fronteiras iniciais. Em seguida, residentes corrigiram essas fronteiras e radiologistas seniores fizeram a revisão final. Depois de cada lote de exames concluído, o modelo de IA foi re-treinado com os contornos aprimorados e usado para auxiliar o próximo lote. A cada ciclo, seu desempenho aproximou-se do aceitável para especialistas humanos, reduzindo o esforço necessário para correções futuras enquanto preservava a precisão.
O que os dados revelam sobre os tumores
Como cada lesão nas tomografias foi delineada em três dimensões, os autores puderam estudar seus tamanhos e densidades em detalhe. A maioria dos tumores estava nos pulmões e no fígado. Tumores pulmonares tendiam a ter pequeno volume, mas frequentemente apresentavam diâmetros relativamente longos, enquanto linfonodos exibiam volumes maiores, porém diâmetros principais um pouco mais curtos do que tumores hepáticos. A equipe também examinou quão claras ou escuras essas regiões apareciam na TC, uma propriedade relacionada à densidade tecidual. Tumores pulmonares, rodeados por ar, mostraram padrões de intensidade muito diferentes dos tumores hepáticos e dos linfonodos, sugerindo que características numéricas simples extraídas de imagens de TC podem ajudar a distinguir tipos de lesão. Importante, o estudo confirmou uma relação forte entre o maior diâmetro de uma lesão e seu verdadeiro volume 3‑D, apoiando a ideia de que regras baseadas em diâmetro, como o RECIST, podem servir como substituto prático para medidas volumétricas completas quando aplicadas com cuidado.
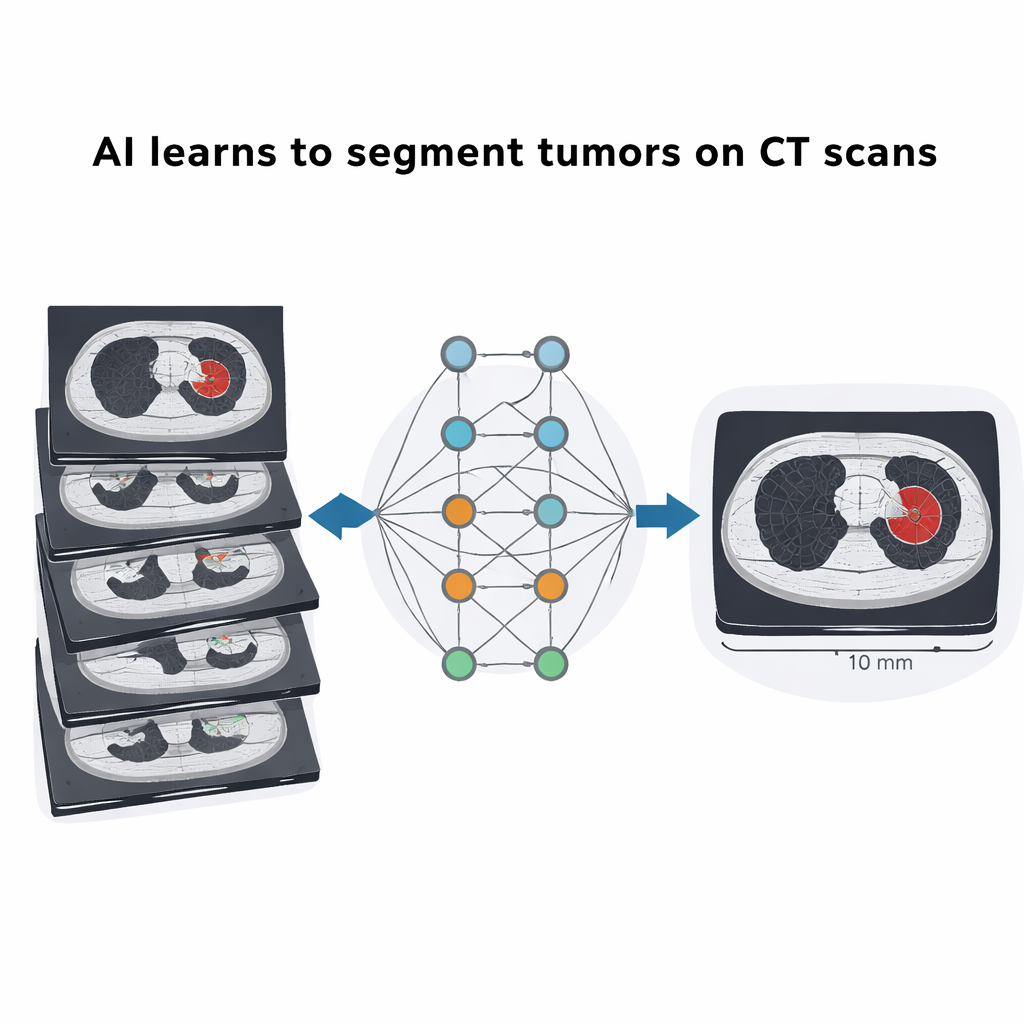
Testando o conjunto de dados com aprendizado profundo
Para demonstrar como o conjunto de dados pode ser usado, os pesquisadores treinaram e refinaram dois tipos de sistemas de aprendizado profundo. Primeiro, ajustaram finamente o MedSAM para segmentar tumores automaticamente a partir de caixas delimitadoras simples, alcançando índices de sobreposição com contornos de especialistas em uma faixa semelhante à relatada em conjuntos de dados internacionais muito maiores. Segundo, adaptaram uma estrutura amplamente usada chamada nnUNet, partindo de modelos treinados em desafios globais de imagem de pulmão e fígado e depois ajustando‑os finamente com estes novos dados chilenos. Após o ajuste, os sistemas igualaram ou superaram seu desempenho original, especialmente para tumores pulmonares, apesar da coorte de pacientes ser relativamente pequena. Isso demonstra que dados locais cuidadosamente curados podem aumentar significativamente a confiabilidade de ferramentas de IA em um ambiente hospitalar específico.
O que isso significa para o futuro do cuidado oncológico
Para não especialistas, a mensagem chave é que este conjunto de dados é uma ferramenta possibilitadora, não um produto diagnóstico por si só. Ao compartilhar abertamente tomografias nas quais todo tumor e linfonodo visíveis foram delineados e, em muitos casos, medidos com precisão, os autores oferecem um campo de treinamento realista para algoritmos que visam automatizar o acompanhamento de tumores. Tais ferramentas podem ajudar radiologistas a gastar menos tempo em medições manuais e mais tempo em julgamentos complexos, ao mesmo tempo reduzindo a variação entre leitores. Como os dados vêm de um hospital latino‑americano e são liberados sob uma licença permissiva, eles também contribuem para que a futura IA médica seja testada em pacientes mais diversos, aumentando as chances de que o monitoramento oncológico automatizado funcione de forma confiável para pessoas ao redor do mundo.
Citação: Rojas-Pizarro, R., Vásquez-Venegas, C., Pereira, G. et al. A CT Dataset with RECIST Measurements and Comprehensive Segmentation Masks for Tumors and Lymph Nodes. Sci Data 13, 270 (2026). https://doi.org/10.1038/s41597-026-06597-6
Palavras-chave: imagens do câncer, tomografias computadorizadas, segmentação de tumores, RECIST, conjuntos de dados de IA médica