Clear Sky Science · pt
O metabolismo da vitamina B2 promove a estabilidade da FSP1 para prevenir a ferroptose
Como uma vitamina comum ajuda as células a decidir entre viver e morrer
Nossas células caminham constantemente numa corda bamba entre a sobrevivência e a autodestruição. Uma forma dramática de morte celular, chamada ferroptose, atraiu atenção porque pode matar seletivamente células cancerosas que resistem a outros tratamentos. Este estudo revela que um nutriente corriqueiro — a vitamina B2, ou riboflavina — inclina discretamente essa balança ao estabilizar uma proteína protetora chave. Entender essa conexão oculta entre dieta, metabolismo celular e morte de células cancerosas pode ajudar pesquisadores a projetar terapias mais inteligentes e aprimorar futuras recomendações nutricionais.
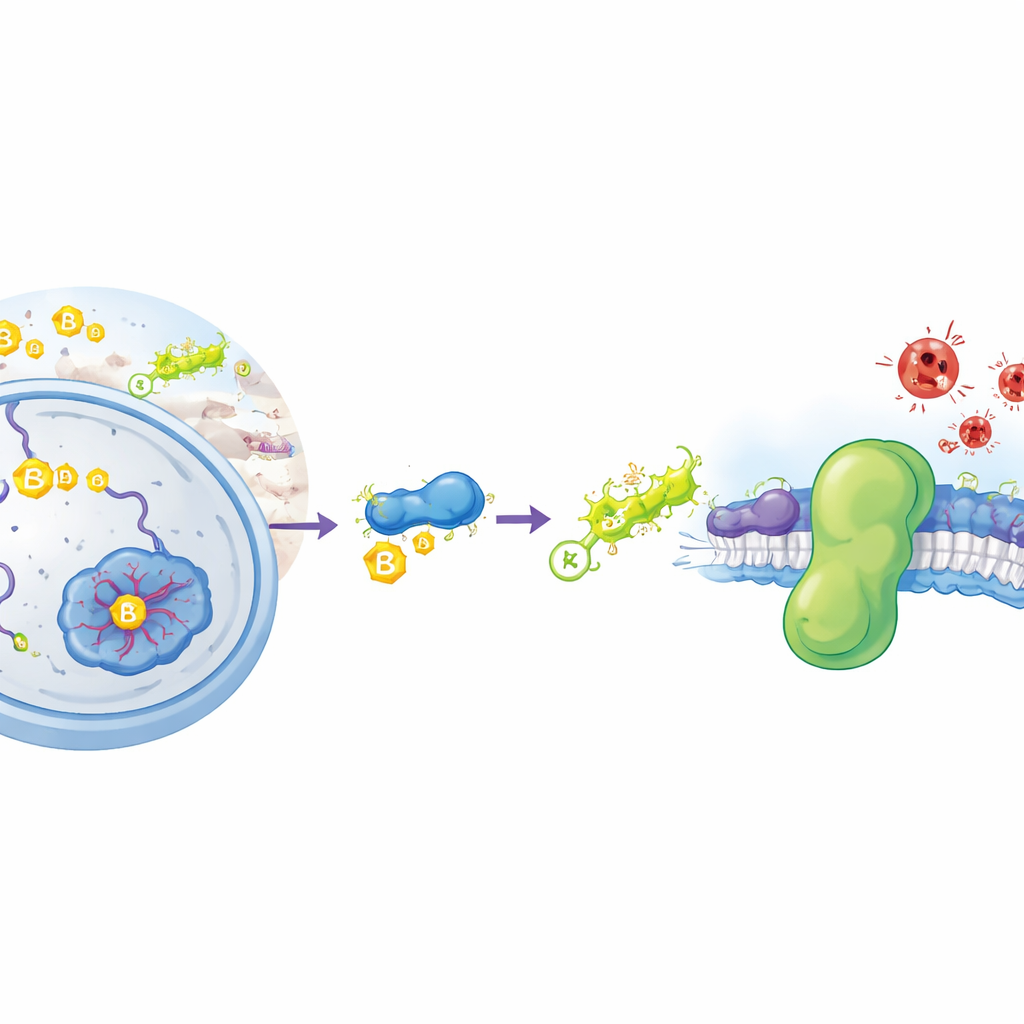
Um tipo especial de ferrugem dentro das células
A ferroptose é um tipo de morte celular impulsionada por um processo químico não muito diferente da ferrugem em metais: a oxidação descontrolada de gorduras nas membranas celulares. Quando essas gorduras se degradam, as membranas perdem integridade e as células estouram. Nossas células normalmente dispõem de várias defesas para evitar que isso aconteça. Um escudo importante é uma enzima chamada GPX4, que usa uma pequena molécula, o glutationa, para desintoxicar peróxidos lipídicos nocivos. Um segundo escudo, paralelo, é uma proteína chamada FSP1, que se associa às membranas celulares e usa moléculas lipofílicas para interceptar radicais destrutivos antes que se espalhem. Células cancerosas frequentemente aumentam a expressão de FSP1 para evitar a ferroptose, tornando essa proteína um alvo promissor para novos fármacos anticâncer. Ainda assim, até agora os cientistas não sabiam como as células controlam quanto FSP1 é produzido e por quanto tempo ele sobrevive.
Construindo um “medidor de combustível” celular para um bloqueador de morte
Para descobrir os gestores ocultos da FSP1, os pesquisadores primeiro modificaram células humanas de câncer de osso para carregar um repórter fluorescente. Eles marcaram a proteína FSP1 natural com um sinal de luz verde e o ligaram a um sinal azul que informa quanto RNA mensageiro de FSP1 a célula está produzindo. Esse desenho inteligente permitiu distinguir mudanças na atividade gênica (azul) de mudanças na estabilidade da proteína (verde). Com esse sistema bicromático, usaram CRISPR–Cas9 para interromper sistematicamente quase todos os genes do genoma e então selecionaram células com níveis altos ou baixos de FSP1. Ao comparar quais RNAs guia foram enriquecidos em cada grupo, mapearam centenas de genes que aumentam ou reduzem a FSP1, atuando ao nível do controle gênico ou da degradação proteica.
O trabalho oculto da vitamina B2: criar uma alça estabilizadora
Entre os achados mais marcantes estavam duas enzimas, riboflavina quinase (RFK) e sintetase de FAD (FLAD1), que convertem a vitamina B2 em um cofator chamado FAD. A FSP1 é uma flavoproteína que normalmente se liga firmemente ao FAD para realizar suas reações químicas. Quando RFK ou FLAD1 foram removidos, ou quando as células foram cultivadas em meio deficiente em vitamina B2, os níveis da proteína FSP1 caíram acentuadamente, embora a atividade gênica permanecesse similar. A equipe mostrou que essa perda tornou as células muito mais vulneráveis à ferroptose quando a GPX4 era bloqueada. Importante, a própria vitamina B2 não atuou como um antioxidante clássico: em um ensaio sensível em tubo de ensaio ela falhou em impedir a oxidação lipídica, ao contrário da vitamina E. Em vez disso, adicionar FAD (e em parte seu precursor FMN) a células deficientes restabeleceu tanto os níveis de FSP1 quanto a resistência à morte por ferroptose, enquanto vitamina B2 extra sozinha não ajudou se as enzimas de processamento estavam ausentes.
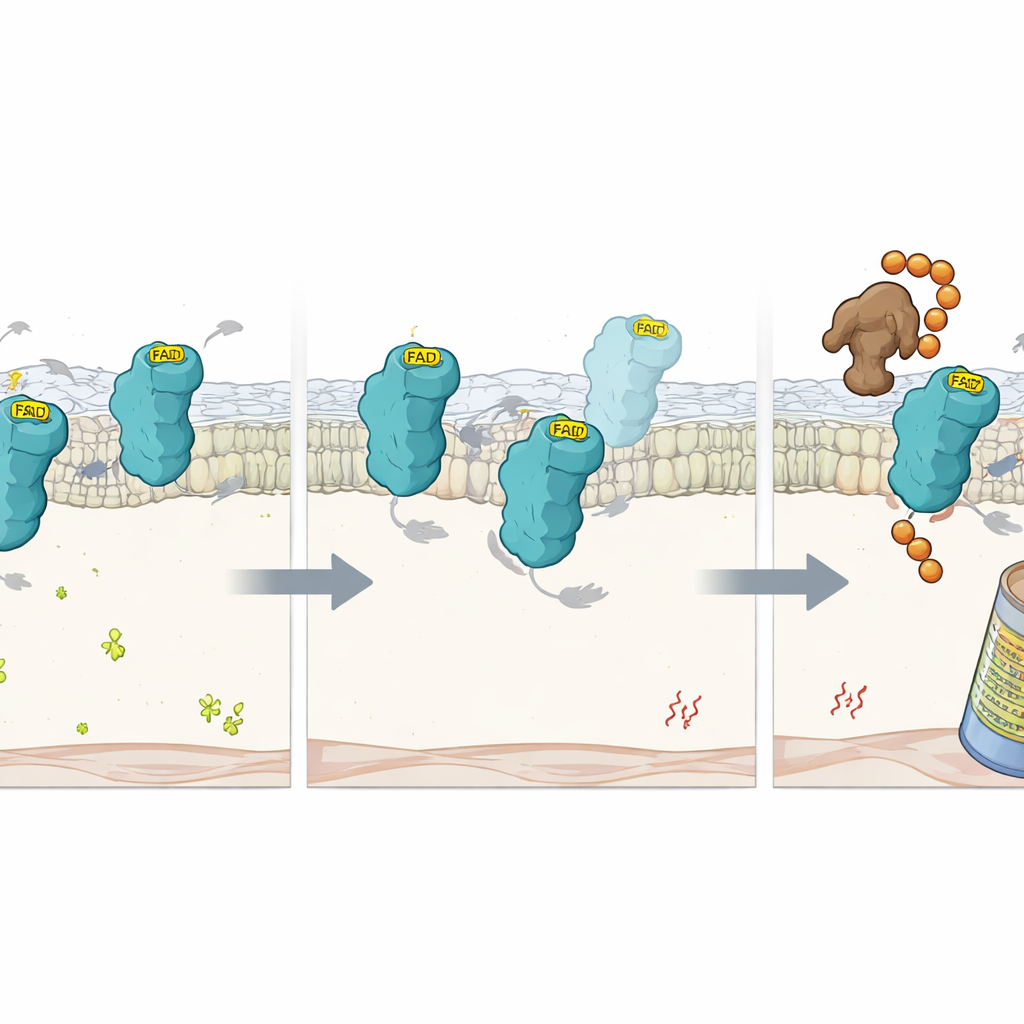
O que acontece quando o cofator falta
Para aprofundar, os cientistas estudaram mutações precisas na FSP1 que prejudicam sua capacidade de reter FAD. Essas proteínas mutantes ainda se dobravam em formas majoritariamente normais, mas perderam seu FAD e atividade catalítica. Dentro das células, elas decaíam muito mais rapidamente do que a FSP1 normal, a menos que o proteassoma — a maquinaria celular de degradação de proteínas — fosse bloqueado. Isso sugeriu que a ligação ao FAD age como uma alça estabilizadora que protege a FSP1 de ser marcada como defeituosa. Usando outra triagem CRISPR focalizada sob condições de baixo FAD, a equipe identificou uma ligase E3 chamada RNF8 como um fator chave que reconhece a FSP1 sem FAD. Quando RFK foi deletado, a RNF8 anexou cadeias de ubiquitina à proteína vazia, direcionando-a para destruição pelo proteassoma. Remover a RNF8 retardou a rotatividade da FSP1 em células pobres em FAD, embora não pudesse restaurar sua função protetora perdida sem o cofator.
Da circuitaria molecular a ideias para terapia do câncer
Ao juntar essas peças, os autores propõem um modelo simples, porém poderoso. A vitamina B2, após ser convertida em FAD por RFK e FLAD1, liga-se à FSP1 e é essencial tanto para sua atividade bioquímica quanto para sua longevidade. Quando o suprimento de vitamina B2 ou seu processamento falham, a FSP1 recém-sintetizada não consegue assegurar o FAD, é sinalizada pela RNF8 e rapidamente desmontada pelo proteassoma, deixando as células mais expostas ao dano por ferroptose. Dados de câncer sugerem que tumores com maior expressão de RFK são mais resistentes a fármacos que induzem ferroptose, sublinhando a relevância desse caminho no mundo real. Para não especialistas, a mensagem-chave é que uma vitamina familiar faz muito mais do que atuar como um antioxidante simples: ela ajuda a decidir se uma potente proteína anti-morte permanece de guarda ou é eliminada. Ao ajustar o metabolismo da vitamina B2 ou a estabilidade da FSP1, tratamentos futuros podem aproveitar melhor a ferroptose para eliminar células cancerosas preservando os tecidos saudáveis.
Citação: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Palavras-chave: ferroptose, vitamina B2, FSP1, morte de células cancerosas, metabolismo celular