Clear Sky Science · pt
Cartografia, origem e papel da quimera elemento transponível–gene na ampliação da plasticidade do transcriptoma
Passageiros ocultos em nosso DNA
Grande parte do nosso DNA é composta por remanescentes virais antigos chamados elementos transponíveis — trechos de código genético que no passado saltavam pelos genomas como parasitas carona. Este estudo mostra que esses fragmentos virais antigos não são apenas lixo silencioso: eles podem se emendar aos nossos próprios genes para criar mensagens híbridas, ajudar as células a se adaptar a condições mutáveis e, às vezes, alimentar doenças. Ao mapear esses híbridos ao longo do desenvolvimento, do envelhecimento e do câncer, os autores revelam uma maneira surpreendente pela qual o DNA viral continua a moldar a biologia humana hoje.
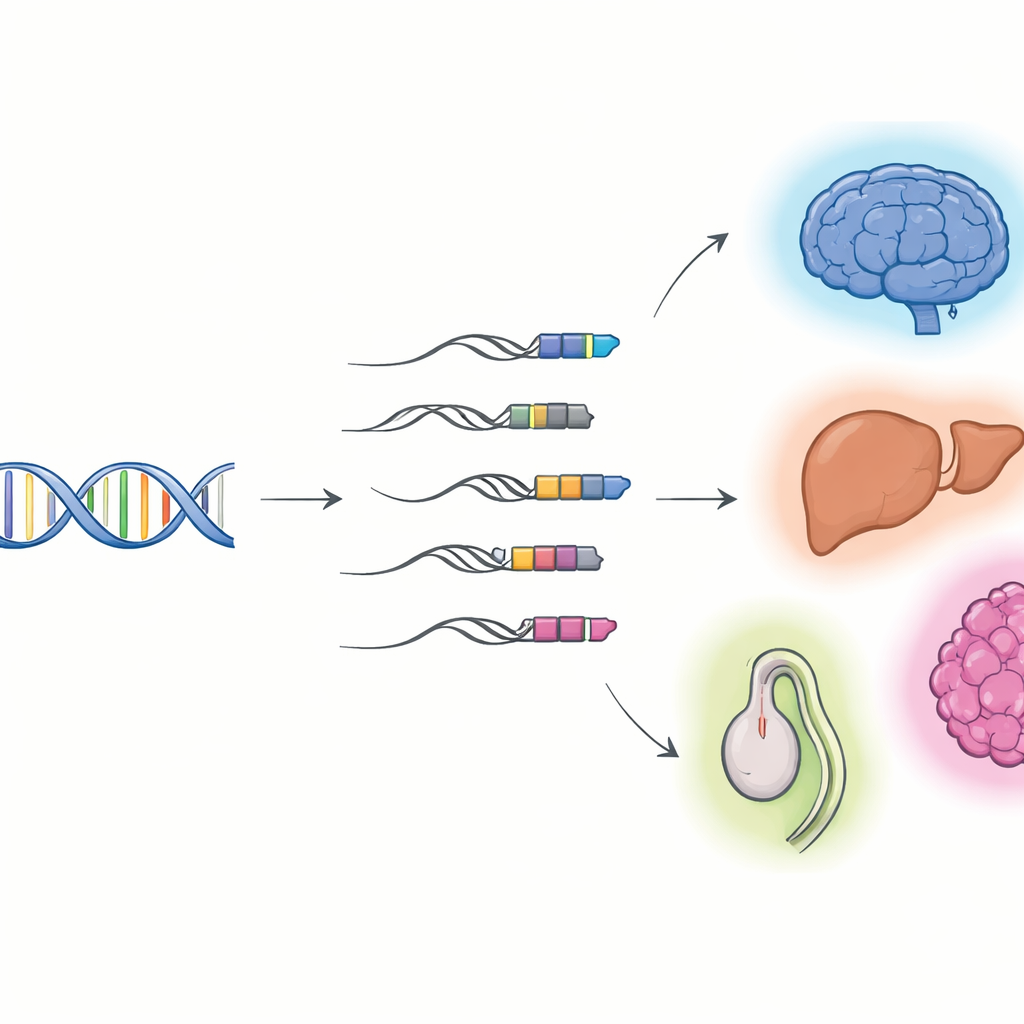
Quando o DNA viral se torna parte dos nossos genes
Os pesquisadores concentraram-se nas “quimeras TE–gene”: moléculas de RNA que começam em um elemento transponível e então seguem para um gene hospedeiro. Usando sequenciamento de leituras longas, que pode capturar moléculas de RNA inteiras de ponta a ponta, combinado com o sequenciamento padrão de leituras curtas, eles construíram catálogos detalhados desses híbridos em células e órgãos de camundongos e humanos. Encontraram milhares de transcritos quiméricos antes desconhecidos, a maioria deles RNAs não codificantes em vez de moldes para proteínas. Muitos começam em uma classe de remanescentes virais chamada long terminal repeats (LTRs), que frequentemente se situam na frente de genes e podem atuar como interruptores alternativos de liga/desliga. Tecidos e órgãos diferentes usam conjuntos distintos dessas quimeras, com atividade especialmente rica no cérebro, fígado e testículo, e seu uso muda conforme os tecidos se desenvolvem do estágio fetal ao adulto.
Quimeras no envelhecimento e no câncer
Para entender como esses híbridos viral–hospedeiro se comportam em populações reais, a equipe vasculhou grandes conjuntos de dados humanos cobrindo dezenas de tecidos de centenas de pessoas, bem como amostras tumorais. Identificaram várias centenas de quimeras de alta confiança que reaparecem em diferentes indivíduos. Sua expressão varia não apenas entre órgãos, mas também com a idade: em tecidos como sangue e cérebro, algumas quimeras dirigidas por LTR declinam em adultos mais velhos, enquanto em certos tecidos periféricos aumentam. Em muitos tipos de câncer, esses híbridos baseados em LTR estão amplamente aumentados em tumores em comparação com o tecido normal adjacente, e pacientes cujos tumores expressam mais desses elementos tendem a ter pior prognóstico. Em conjuntos de dados de pessoas resistentes à quimioterapia ou imunoterapia, os genes afetados por novos éxons dirigidos por LTR frequentemente participam de vias relacionadas ao modo de ação desses medicamentos, sugerindo que quimeras de TE podem ajudar tumores a se reconfigurarem sob pressão do tratamento.
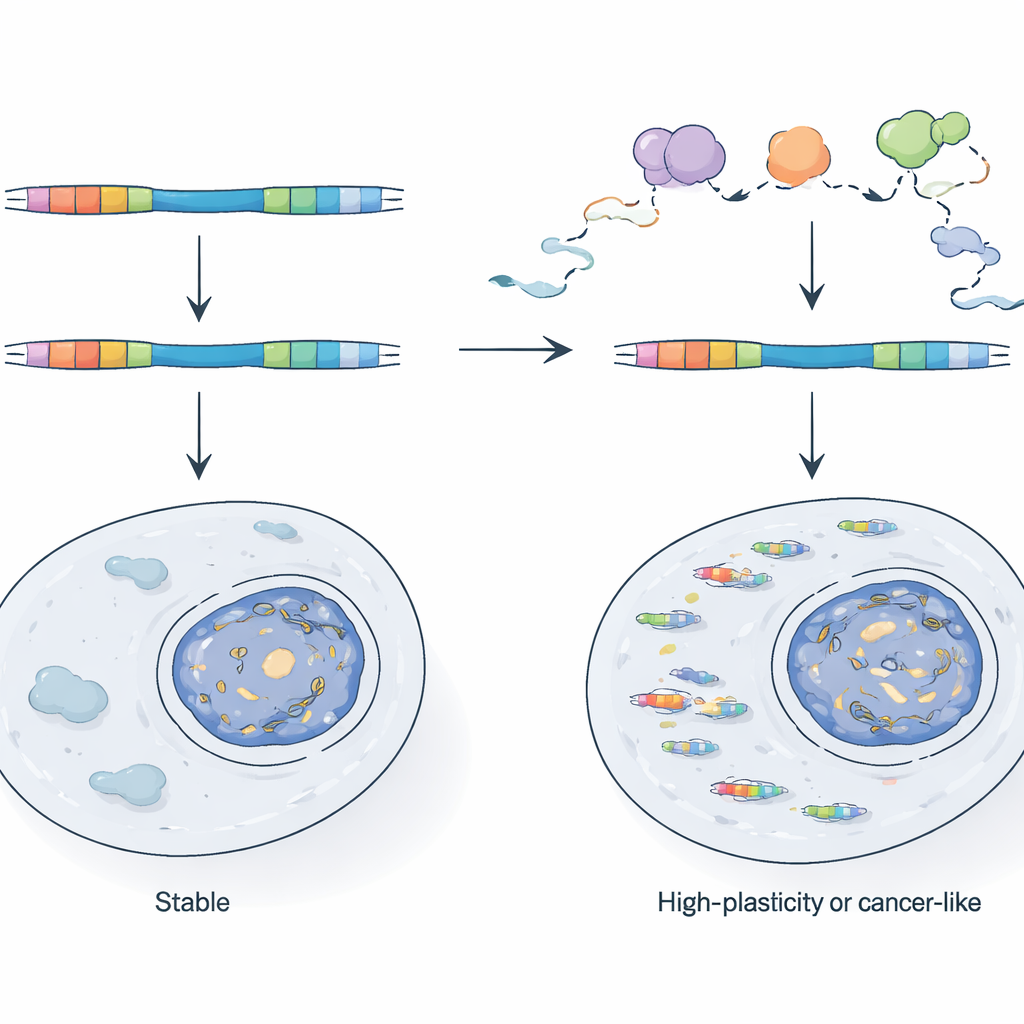
Como as células controlam os híbridos virais
Dada sua potência, por que as quimeras de TE não dominam as células normais? Os autores mostram que as células dependem de um sistema de controle de qualidade do RNA, centrado no complexo nuclear exossoma, para vigiar e destruir muitos desses transcritos enquanto estão sendo produzidos. Quando eles tornam geneticamente disfuncional um componente chave do exossoma em células-tronco de camundongo, promotores dirigidos por LTR tornam-se muito mais ativos e os RNAs quiméricos disparam. Ao comparar RNA recém-sintetizado com RNA estável, mostram que alguns LTRs são normalmente mantidos sob controle porque seus transcritos são rapidamente degradados, enquanto outros são regulados no nível da frequência de iniciação da transcrição. Esses LTRs ativos tendem a se localizar em regiões do genoma já acessíveis e frequentemente transcritas, indicando que simplesmente estar próximo a um gene ativo ou a um transcrito em antissenso pode ajudar um fragmento viral a escapar do silenciamento epigenético tradicional.
Splicing, plasticidade de células-tronco e um “interruptor mestre” viral
A história fica mais intrincada quando a maquinaria de splicing da célula é perturbada. Os autores silenciaram vários fatores centrais de splicing ou inibiram quimicamente o espliceossomo e observaram um desfecho compartilhado com a perda do exossoma: um forte aumento em quimeras dirigidas por LTR e em genes curtos, pobres em íntrons. Entre os vencedores está o MERVL, um retrovírus endógeno ativo em embriões de camundongo muito precoces. Quando a sequência interna do MERVL e seus fatores de transcrição a jusante são regulados para cima, células-tronco migram para um estado mais parecido com a “totipotência”, assemelhando-se a células embrionárias iniciais capazes de formar todos os tecidos. Inversamente, degradar o RNA do MERVL com oligonucleotídeos antisenso diminui essa transição e reduz a atividade de promotores LTR, indicando que o MERVL age como um interruptor mestre capaz de disparar uma rede mais ampla de quimeras de TE e plasticidade do estado celular.
Inovação viral ao longo da evolução
Ao examinar muitos genomas de mamíferos, a equipe traça quando diferentes famílias de TE começaram a doar éxons para genes hospedeiros. Tanto em humanos quanto em camundongos, famílias de LTR relativamente jovens são especialmente propensas a formar quimeras na orientação “sense” que podem ser lidas como parte dos transcritos do hospedeiro. Esse padrão sugere que novas ondas de inserções de TE repetidamente alimentaram material bruto nas redes regulatórias gênicas ao longo do tempo evolutivo. Em vez de serem puramente prejudiciais, essas inserções podem ser testadas pela maquinaria de transcrição e degradação da célula: a maioria é silenciada ou degradada, mas uma minoria encontra-se no lugar e contexto certos para ser cooptada como elementos regulatórios úteis ou novos inícios gênicos.
Por que esses remanescentes virais importam
Para um não especialista, este trabalho mostra que uma porção grande e antes desprezada do nosso genoma está ativamente moldando como os genes são lidos, como as células mudam de identidade e como as doenças evoluem. Sequências virais antigas podem ser transformadas em “portas de entrada” alternativas de genes, produzindo RNAs híbridos que normalmente são policiados por sistemas celulares de limpeza. Quando esse policiamento ou o splicing normal falham, esses híbridos podem explodir em número, empurrando células-tronco para estados mais flexíveis ou ajudando tumores a se adaptar e resistir à terapia. Ao longo de milhões de anos, a evolução repetidamente mexeu com esses fragmentos virais, transformando muitos deles de parasitas genômicos em blocos de construção da complexidade regulatória — e deixando-nos com um transcriptoma muito mais plástico e dinâmico do que uma simples lista de genes sugeriria.
Citação: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Palavras-chave: elementos transponíveis, transcritos quiméricos, vigilância do RNA, plasticidade de células-tronco, evolução do câncer