Clear Sky Science · pt
Adaptação ao estresse da importação de proteínas mitocondriais pela degradação de DNAJC15 mediada por OMA1
Como nossas células lidam quando suas usinas ficam sob estresse
Cada célula do seu corpo depende de pequenas estruturas chamadas mitocôndrias para transformar alimento em energia utilizável. Como fábricas em miniatura, as mitocôndrias importam constantemente novas peças — proteínas recém-sintetizadas em outras partes da célula — para manter suas máquinas em funcionamento. Este artigo revela como, quando as mitocôndrias estão sob estresse ou danificadas, as células deliberadamente reduzem esse fluxo de importação de proteínas. Ao fazer isso, protegem-se contra sobrecarga e coordenam uma resposta mais ampla ao estresse que envolve não só as mitocôndrias, mas também outro compartimento-chave, o retículo endoplasmático.
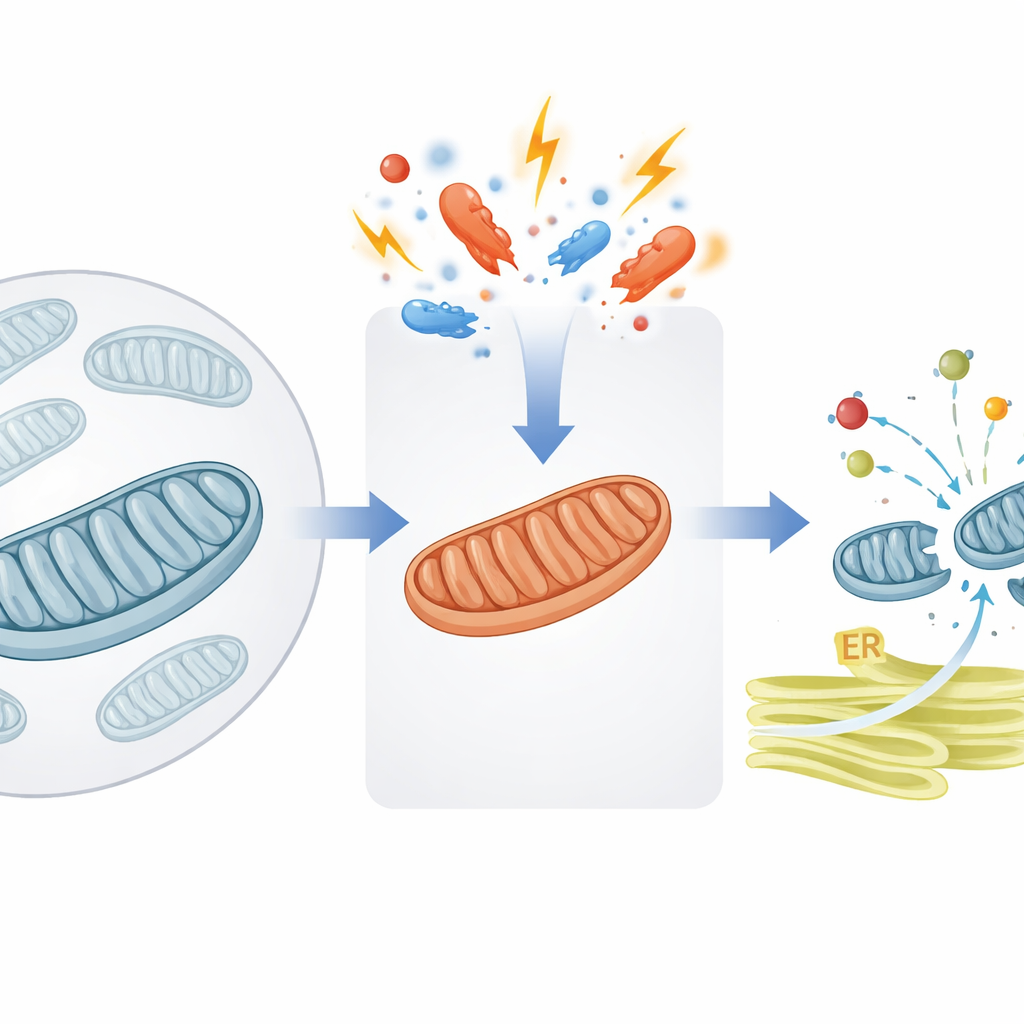
Uma válvula de segurança para o tráfego de proteínas mitocondriais
As mitocôndrias dependem de milhares de proteínas que são primeiro construídas no compartimento principal da célula e depois enviadas para dentro. Os autores concentram-se em um portal crucial na membrana interna mitocondrial, apoiado por uma proteína auxiliar chamada DNAJC15. Em condições normais, DNAJC15 ajuda a puxar os “pacotes” de proteínas recém-sintetizadas através do canal de importação e para o interior mitocondrial, onde muitas passam a integrar a maquinaria produtora de energia conhecida como fosforilação oxidativa (OXPHOS). O estudo mostra que, quando as mitocôndrias sofrem estresse — como produção de energia prejudicada ou alterações nas propriedades da membrana — a célula aciona um interruptor molecular que altera quanto de proteína o organelo está disposto a importar.
OMA1: o cortador ativado pelo estresse
No centro desse interruptor está uma enzima sensível ao estresse chamada OMA1, localizada na membrana interna mitocondrial. Quando as mitocôndrias enfrentam problemas, a OMA1 torna-se ativa e corta o DNAJC15 em uma posição específica próxima ao seu início. Esse corte produz uma versão mais curta do DNAJC15 que é rapidamente degradada por outro complexo enzimático mitocondrial chamado protease m-AAA. Como resultado, perde-se a forma de comprimento total e capaz de promover a importação de DNAJC15. Os autores mostram que células sem DNAJC15, ou nas quais DNAJC15 é rapidamente destruída após a ativação da OMA1, têm capacidade reduzida de trazer novas proteínas para as mitocôndrias, especialmente aquelas necessárias para montar e manter os complexos de OXPHOS.
Desacelerando a montagem energética para corresponder à saúde mitocondrial
Usando medições proteômicas em larga escala e ensaios de importação, a equipe descobriu que DNAJC15 é particularmente importante para abastecer o interior mitocondrial com proteínas envolvidas na expressão gênica e na montagem da cadeia respiratória. Quando DNAJC15 está ausente, essas proteínas se acumulam mais lentamente dentro das mitocôndrias, e a capacidade dos organelos de consumir oxigênio e alimentar a produção de energia — medida em mitocôndrias isoladas — declina, especialmente para o complexo I da cadeia respiratória. Outro componente do canal de importação, TIMM17A, atua em conjunto com DNAJC15: a perda de ambos causa defeitos especialmente pronunciados nos níveis de proteínas ribossomais mitocondriais e componentes de OXPHOS. Em conjunto, esses achados sugerem que a destruição de DNAJC15 mediada por OMA1 é uma forma de reduzir temporariamente a construção de nova maquinaria energética até que o organelo se recupere.
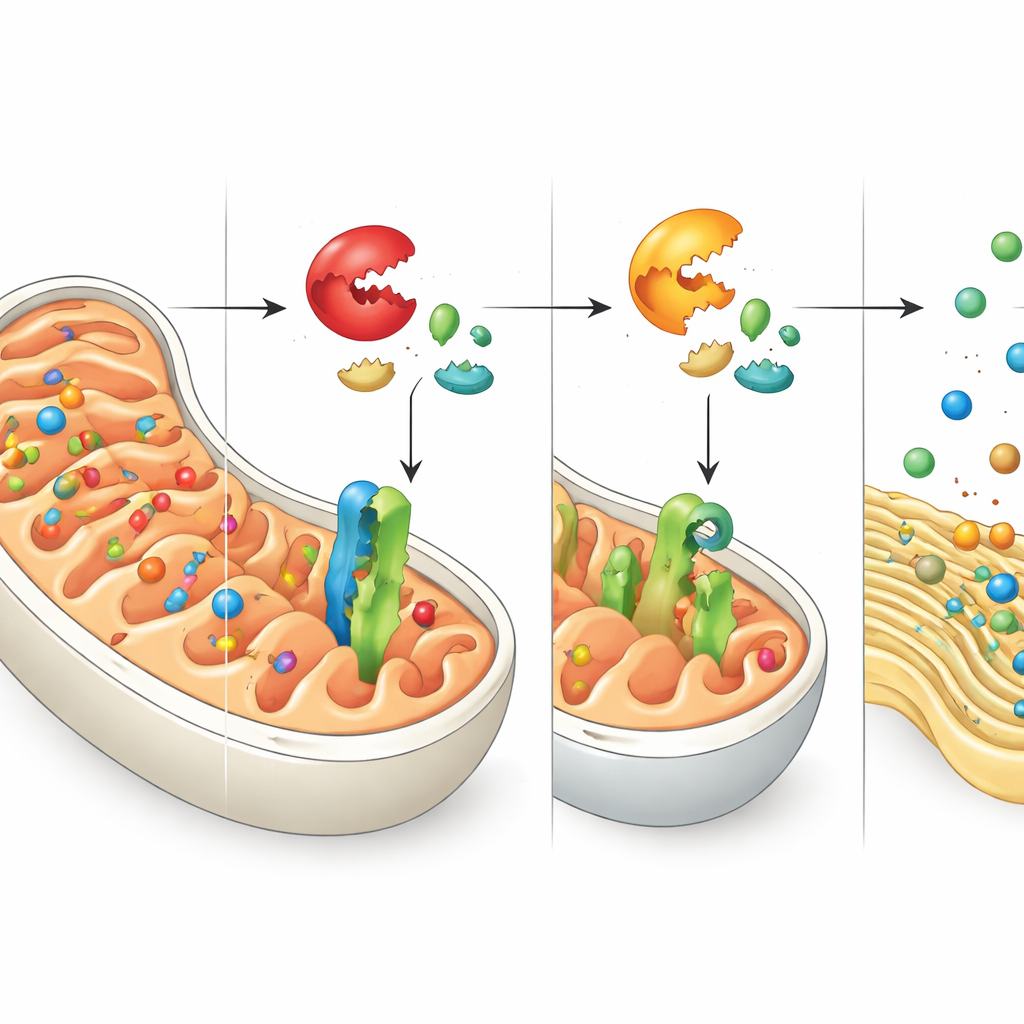
Pacotes desviados e um pedido de socorro ao ER
Desligar o DNAJC15 não impede a célula de produzir proteínas mitocondriais — isso principalmente impede que elas cheguem ao destino pretendido. Os autores rastrearam para onde vão essas proteínas encalhadas e descobriram que muitas acabam no retículo endoplasmático (ER), uma rede de membranas que normalmente ajuda a dobrar e processar diferentes conjuntos de proteínas. Essas proteínas mitocondriais errantes ficam incorporadas nas membranas do ER, perturbando o equilíbrio de controle de qualidade do próprio ER. Em resposta, a célula ativa um programa protetor conhecido como resposta a proteínas desnaturadas (unfolded protein response), especificamente por meio de um ramo controlado pelo sensor ATF6. Essa resposta aumenta a capacidade do ER de lidar com proteínas mal dobradas ou deslocadas, revelando uma coordenação estreita entre os sistemas de estresse mitocondrial e do ER.
Uma desaceleração coordenada para proteger a célula
Em conjunto, o estudo descreve um sistema de freio embutido para a biogênese mitocondrial. Quando as mitocôndrias estão sob estresse, a OMA1 aparará e indiretamente destruirá DNAJC15, reduzindo o fluxo de novas proteínas relacionadas à energia para organelos comprometidos. Algumas dessas proteínas são temporariamente armazenadas no ER, que monta sua própria resposta protetora. Ao acoplar a capacidade de importação mitocondrial à saúde do organelo e ao empregar o ER como um local de reserva para proteínas em excesso, as células podem evitar entupir mitocôndrias danificadas e ganhar tempo tanto para repará-las quanto para removê-las completamente. Para um leitor leigo, este trabalho mostra quão profundamente integrados estão nossos sistemas de controle de qualidade celular: mesmo os menores deslizes em um compartimento são detectados e compensados por outros para manter a produção de energia — e a própria vida — em curso.
Citação: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Palavras-chave: estresse mitocondrial, importação de proteínas, controle de qualidade celular, fosforilação oxidativa, retículo endoplasmático