Clear Sky Science · pt
Estrutura e mecanismo da retron antífago Eco2
Como bactérias usam um “autodestruir” embutido para combater vírus
Vírus que infectam bactérias, chamados fágos, estão por toda parte — dos oceanos ao nosso próprio intestino. Este estudo revela como um pequeno dispositivo genético presente em algumas bactérias, conhecido como retron Eco2, as ajuda a sobreviver a ataques de fágos. Ao desvendar a estrutura 3D do Eco2 e como ele é ativado, o trabalho explica um novo tipo de defesa emergencial: quando a infecção é detectada, a célula deliberadamente interrompe sua própria produção de proteínas para impedir a propagação do vírus.
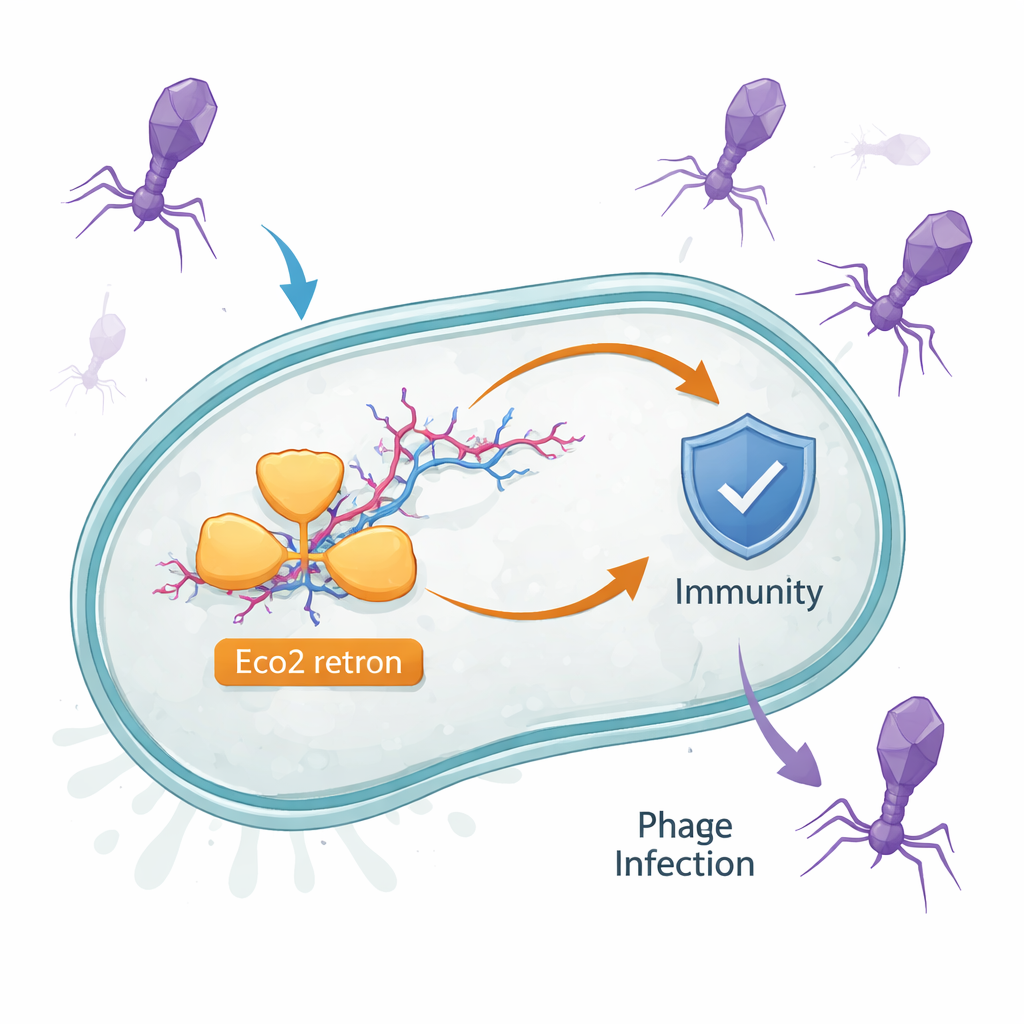
Um dispositivo DNA–RNA oculto nas células bacterianas
Bactérias carregam muitos pequenos sistemas de defesa que só entram em ação durante a infecção. O Eco2 é um deles. Ele vive em Escherichia coli e consiste em uma única proteína que tanto copia RNA em DNA quanto pode cortar ácidos nucleicos. Essa proteína trabalha em conjunto com uma molécula estranha chamada msDNA, um híbrido de RNA e DNA de fita simples que se ramifica como um pequeno galho bifurcado. Indícios anteriores sugeriam que retrons como o Eco2 defendem contra fágos, mas não se entendia como uma única proteína e seu parceiro msDNA detectam a infecção e respondem.
Proteção ampla contra muitos vírus
Os pesquisadores primeiro perguntaram quão bem o Eco2 protege as bactérias contra uma ampla gama de fágos. Ao desafiar células portadoras de Eco2 com uma grande e diversa coleção de vírus, descobriram que o Eco2 bloqueia muitas famílias de fágos, mas não todas. Quando alguns fágos conseguiam escapar, seus genomas mostravam mutações em genes que codificam enzimas virais que cortam DNA, especialmente uma chamada DenB. Esse padrão sugeriu que o Eco2 é ativado por nucleases virais específicas: quando essas enzimas são inativadas por mutação, o vírus consegue passar pela defesa.
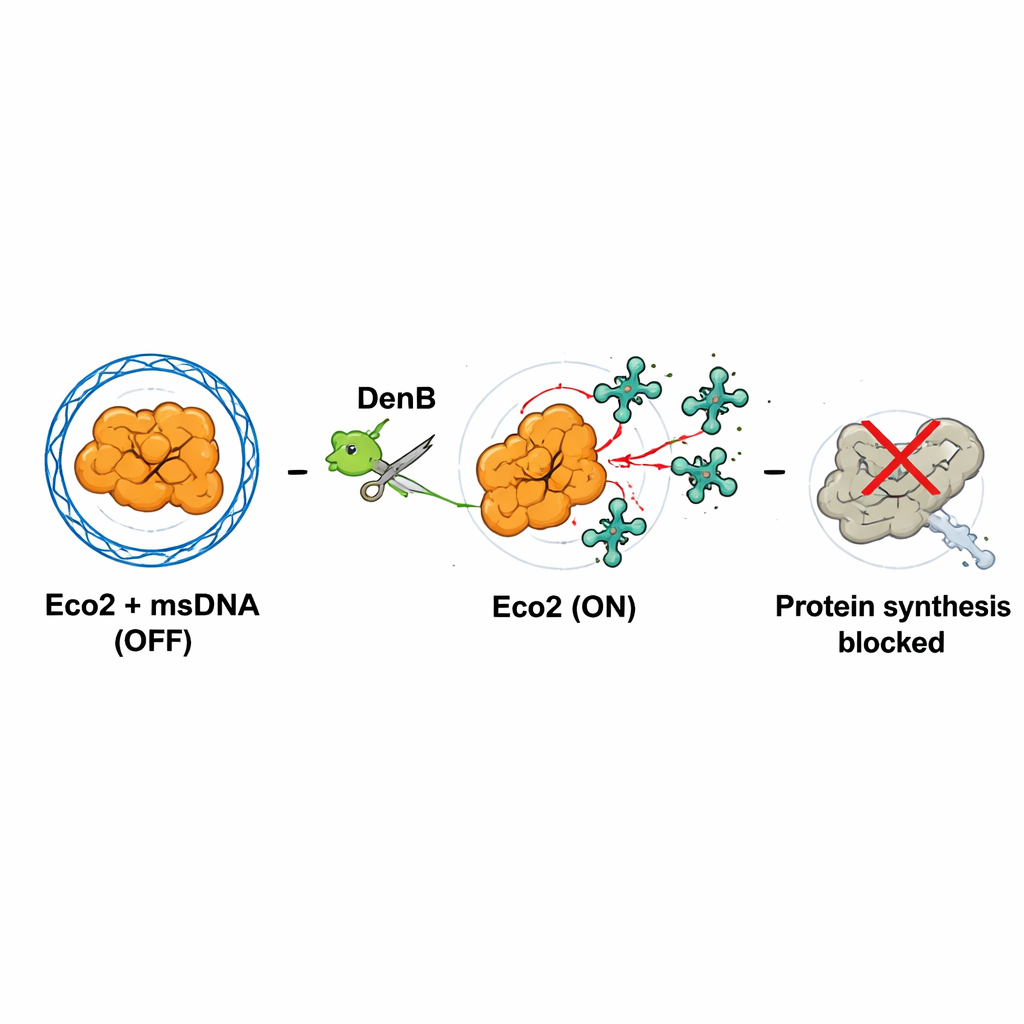
Um escudo molecular de três braços
Para ver como o Eco2 é montado, a equipe usou microscopia crioeletrônica para visualizar o complexo em detalhe quase atômico. O Eco2 não age sozinho: três cópias da proteína Eco2 se montam em uma estrutura de três braços, parecida com uma shuriken. O msDNA ramificado passa por dentro e ao redor dessas três proteínas, atando-as entre si. Ao fazer isso, o msDNA forma uma junção tripla no centro e “cápsula” fisicamente a parte nucleolítica do Eco2, bloqueando seu sítio de corte. Experimentos de troca hidrogênio–deutério, que acompanham quão flexíveis são diferentes regiões, mostraram que a ligação do msDNA torna o complexo mais rígido e estável. Nesse estado de repouso, o Eco2 está efetivamente travado na posição DESLIGADA.
O ataque viral liga o sistema
A chave para a ativação é a destruição do msDNA. A enzima viral DenB, que normalmente ajuda o fago a processar DNA, também corta o msDNA que aprisiona o Eco2. Os autores imitaram esse processo usando tanto DenB purificada quanto uma enzima padrão de corte de DNA e observaram que, uma vez que o msDNA é fatiado, o sítio nucleolítico do Eco2 fica exposto e se rearranja para uma configuração ativa. Estruturas de alta resolução desse “estado LIGADO” mostraram que um aminoácido crítico no bolso nucleolítico move-se para uma posição onde pode coordenar adequadamente um íon magnésio, essencial para cortar RNA. Assim, a atividade da nuclease viral, destinada a remodelar o DNA do hospedeiro, involuntariamente puxa o pino de segurança do Eco2.
Cortando os próprios tRNAs da célula para deter o vírus
O que o Eco2 ativado corta? Usando sistemas sem célula, marcação radioativa e sequenciamento de RNA durante infecções reais, a equipe descobriu que o Eco2 fende primariamente RNAs de transferência (tRNAs), as moléculas adaptadoras que entregam aminoácidos ao ribossomo. O Eco2 corta esses tRNAs perto de suas extremidades em cauda, especialmente em locais ricos na base citosina. Quando muitos tRNAs são danificados, os ribossomos da célula não conseguem mais sintetizar proteínas de forma eficiente. Na presença de DenB e Eco2 ativo, a produção de proteína verde fluorescente caiu acentuadamente, e tanto RNAs bacterianos quanto virais foram degradados. Esse desligamento provavelmente representa uma “infecção abortiva”: a célula bacteriana infectada sacrifica seu próprio crescimento para que o vírus não consiga replicar-se e se disseminar.
Por que isso importa além das bactérias
Este trabalho mostra como uma retron mínima pode detectar uma enzima viral, mudar de uma forma inativa para uma ativa e, então, prejudicar a síntese proteica ao mirar em tRNAs. Para um público não especializado, a ideia central é que bactérias às vezes vencem vírus não por alvo de precisão, mas puxando a tomada de sua própria maquinaria celular no momento certo. Além de aprofundar nossa compreensão da imunidade microbiana, as estruturas detalhadas do Eco2 e de sua plataforma de msDNA oferecem um mapa para engenheiros que desejam reaproveitar retrons como ferramentas para edição genômica e biologia sintética.
Citação: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Palavras-chave: imunidade a bacteriófagos, retron Eco2, defesa antiviral bacteriana, clivagem de tRNA, msDNA