Clear Sky Science · pt
Estrutura e função do supercomplexo sensível a aminoácidos SEAC–EGOC em leveduras
Como as células decidem quando crescer
Cada célula precisa decidir continuamente se pode crescer ou deve conservar recursos. Essa decisão depende fortemente dos aminoácidos, blocos de construção das proteínas e uma fonte chave de nitrogênio. Este artigo revela, com notável detalhe estrutural, como células de levedura detectam a disponibilidade de aminoácidos por meio de um enorme conjunto molecular e usam essa informação para ligar ou desligar um importante controlador do crescimento, chamado TORC1. Como a mesma circuitaria é conservada em células humanas e está ligada ao câncer e ao metabolismo, os achados em levedura oferecem uma janela sobre como nossas próprias células avaliam quando as condições são favoráveis ao crescimento.
Um centro intricado no centro de reciclagem da célula
Em leveduras, um complexo central de tomada de decisão chamado SEAC posiciona-se na membrana do vacúolo, um organelo que funciona como centro de reciclagem celular. Ali encontra outro complexo, o EGOC, que transmite informações sobre os níveis de aminoácidos. Juntos, eles enviam sinais ao TORC1, o principal interruptor do crescimento. O SEAC tem duas metades funcionais: SEACIT, que pode desligar o TORC1, e SEACAT, considerado por muito tempo como um inibidor de SEACIT. Os autores usaram crio–microscopia eletrônica de alta resolução para visualizar o SEAC completo ligado ao EGOC, capturando um retrato desse centro molecular exatamente onde a sinalização ocorre, na superfície do vacúolo. 
Vendo a arquitetura molecular de perto
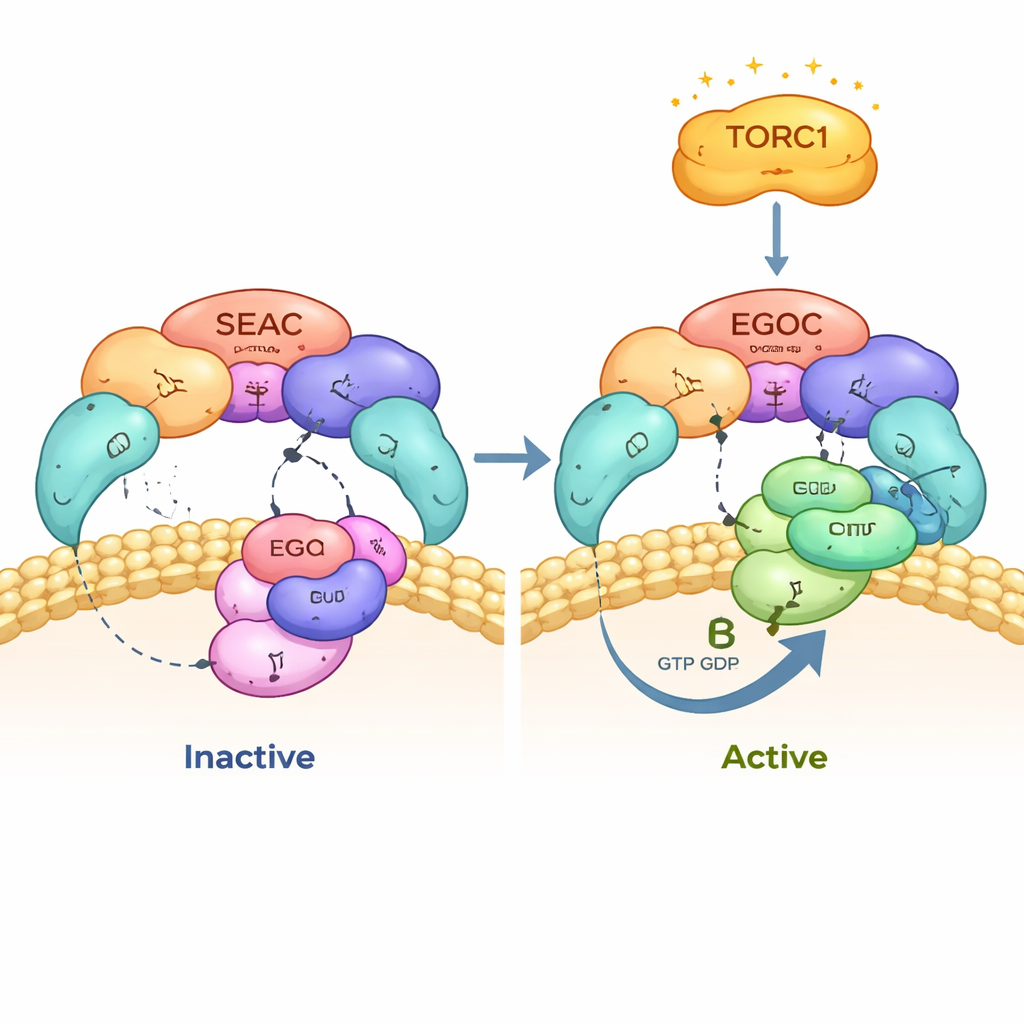
A estrutura revela o SEAC como um grande núcleo formado por subunidades do SEACAT, do qual se estendem duas “asas” flexíveis do SEACIT. Cada asa pode ligar-se a um complexo EGOC, o que significa que um único SEAC pode receber dois sinais simultaneamente. De maneira notável, o EGOC se anexa apenas às asas e não ao núcleo, e a forma geral do SEAC quase não muda quando o EGOC está presente. Isso indica que o SEACAT não bloqueia fisicamente o sítio ativo do SEACIT e não impede a ligação do EGOC. A orientação do complexo na membrana do vacúolo também posiciona o núcleo do SEAC voltado ao citoplasma, onde pode interagir com reguladores adicionais, enquanto as asas ficam próximas à membrana, idealmente colocadas para contactar o EGOC e outros parceiros ancorados na membrana.
Como o SEAC escolhe o sinal certo
Os autores detalharam os contatos entre SEAC e EGOC e descobriram que o SEAC reconhece apenas a versão “ativa” do EGOC, na qual uma de suas pequenas GTPases, Gtr1, carrega um nucleotídeo tipo GTP, enquanto sua parceira, Gtr2, contém GDP. O SEACIT fornece um “dedo” catalítico que alcança o bolso de nucleotídeo de Gtr1 e acelera a quebra do GTP, convertendo o EGOC do estado ativo para o inativo. Mapas detalhados de crio-EM e experimentos de mutação mostram que esse dedo catalítico e um resíduo auxiliar vizinho são essenciais para a interação e para a leitura correta do estado do nucleotídeo. Quando os autores alteraram esses resíduos-chave, o SEAC deixou de se localizar adequadamente no vacúolo, e o EGOC não pôde se engajar de forma produtiva.
Controle rápido versus lento do interruptor de crescimento
Para entender o que isso significa para a célula viva, os pesquisadores acompanharam a atividade do TORC1 ao longo do tempo quando os aminoácidos foram removidos e depois reintroduzidos. Em células normais, o TORC1 desliga rapidamente em poucos minutos após a privação de nitrogênio e então religa rapidamente quando os aminoácidos retornam. Quando o dedo catalítico no SEACIT foi desativado, ou subunidades do SEACIT foram deletadas, o TORC1 praticamente não respondeu nessa janela temporal inicial. O mesmo aconteceu quando tanto Gtr1 quanto Gtr2 foram removidos, mostrando que o par SEAC–EGOC é a via dominante e rápida para o controle de TORC1 por aminoácidos. No entanto, em tempos mais tardios — cerca de meia hora — a atividade do TORC1 ajustou-se lentamente mesmo nesses mutantes, indicando que uma via separada e mais lenta para o TORC1, independente desse sistema de GTPases, também opera nas células.
Um papel surpreendente para uma subunidade distante
Uma descoberta particularmente intrigante refere-se à Sea2, um componente do SEACAT com um domínio “hélice” flexível que se projeta para fora do núcleo. Remover a Sea2, ou apenas sua hélice, produziu defeitos de sinalização quase idênticos aos observados quando a atividade catalítica do SEAC foi perdida: o TORC1 respondeu de maneira lenta tanto à retirada quanto ao reabastecimento de aminoácidos. Ainda assim, a Sea2 situa-se distante do sítio catalítico e não toca diretamente a asa do SEACIT, tornando improvável um mecanismo simples de bloqueio. Experimentos genéticos combinando a perda de Sea2 com uma variante cataliticamente inativa do SEAC sugerem que ter a atividade GAP totalmente ligada ou totalmente desligada perturba a resposta rápida, enquanto uma regulação intermediária é necessária. Os autores propõem que a hélice da Sea2 atua como uma plataforma de ancoragem para um fator desconhecido que modera a atividade do SEACIT, permitindo que as células ajustem finamente o TORC1 em vez de simplesmente desligá-lo permanentemente.
O que isso significa para as decisões de crescimento celular
No geral, o estudo reconstrói a imagem do SEAC não como duas unidades opostas, mas como uma única máquina integrada cuja asa catalítica (SEACIT) e núcleo estrutural (SEACAT) trabalham em conjunto para detectar aminoácidos e ajustar rapidamente o interruptor de crescimento TORC1. A ação enzimática do SEACIT sobre o EGOC fornece o controle rápido e preciso, enquanto a hélice da Sea2 provavelmente recruta reguladores que modulam essa atividade. Ao mesmo tempo, vias paralelas mais lentas asseguram que o TORC1 acabe refletindo o estado nutricional mesmo se o sensor primário estiver perturbado. Como complexos estreitamente relacionados realizam a mesma função em células humanas, esses insights da levedura esclarecem como nossas próprias células equilibram crescimento e disponibilidade de nutrientes, com implicações para entender doenças em que a sinalização do TORC1 está desregulada.
Citação: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Palavras-chave: detecção de aminoácidos, sinalização TORC1, complexo SEAC GATOR, controle do crescimento celular, crio-microscopia eletrônica