Clear Sky Science · pt
Mecanismo e reconstituição da transcrição circadiana em cianobactérias
Por que os relógios biológicos importam, mesmo para bactérias
Todos os seres vivos, de humanos a microrganismos minúsculos, marcam o tempo. Esses relógios internos ajudam os organismos a antecipar o nascer e o pôr do sol, programando atividades como alimentação, reparo e crescimento. Este artigo explora como uma bactéria fotossintética simples, Synechococcus elongatus, usa um relógio proteico para ligar e desligar genes com notável precisão ao longo de um ciclo de 24 horas. Ao reconstruir esse sistema temporal em um tubo de ensaio, os pesquisadores revelam uma versão reduzida de um relógio biológico que pode inspirar novas ferramentas para biotecnologia e biologia sintética.
Um relógio minúsculo que funciona com química
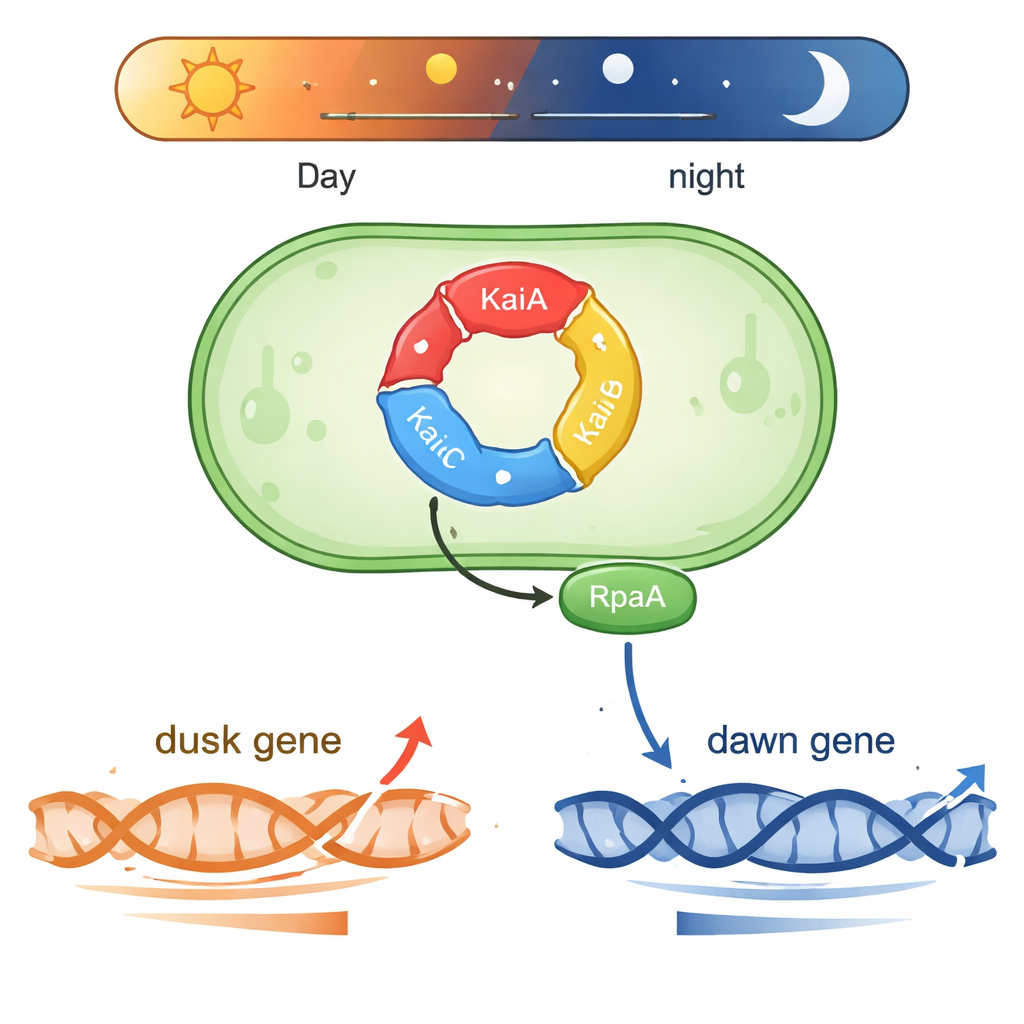
Synechococcus vive em águas iluminadas pelo sol e precisa prever as mudanças diárias de luz. No seu núcleo há uma máquina proteica de três partes composta por KaiA, KaiB e KaiC. Essas proteínas transferem grupos fosfato em um ciclo repetitivo que dura cerca de 24 horas, formando um “trem de engrenagens” bioquímico que marca o tempo mesmo fora da célula. Outras duas proteínas, SasA e CikA, leem o estado de fosforilação de KaiC e o utilizam para controlar outra proteína, RpaA. Quando RpaA está fosforilada, ela se liga ao DNA e atua como um interruptor mestre para centenas de genes que aumentam e diminuem sua expressão em torno do “amanhecer” ou do “anoitecer” subjetivos em luz constante.
Uma proteína, dois cronogramas de genes opostos
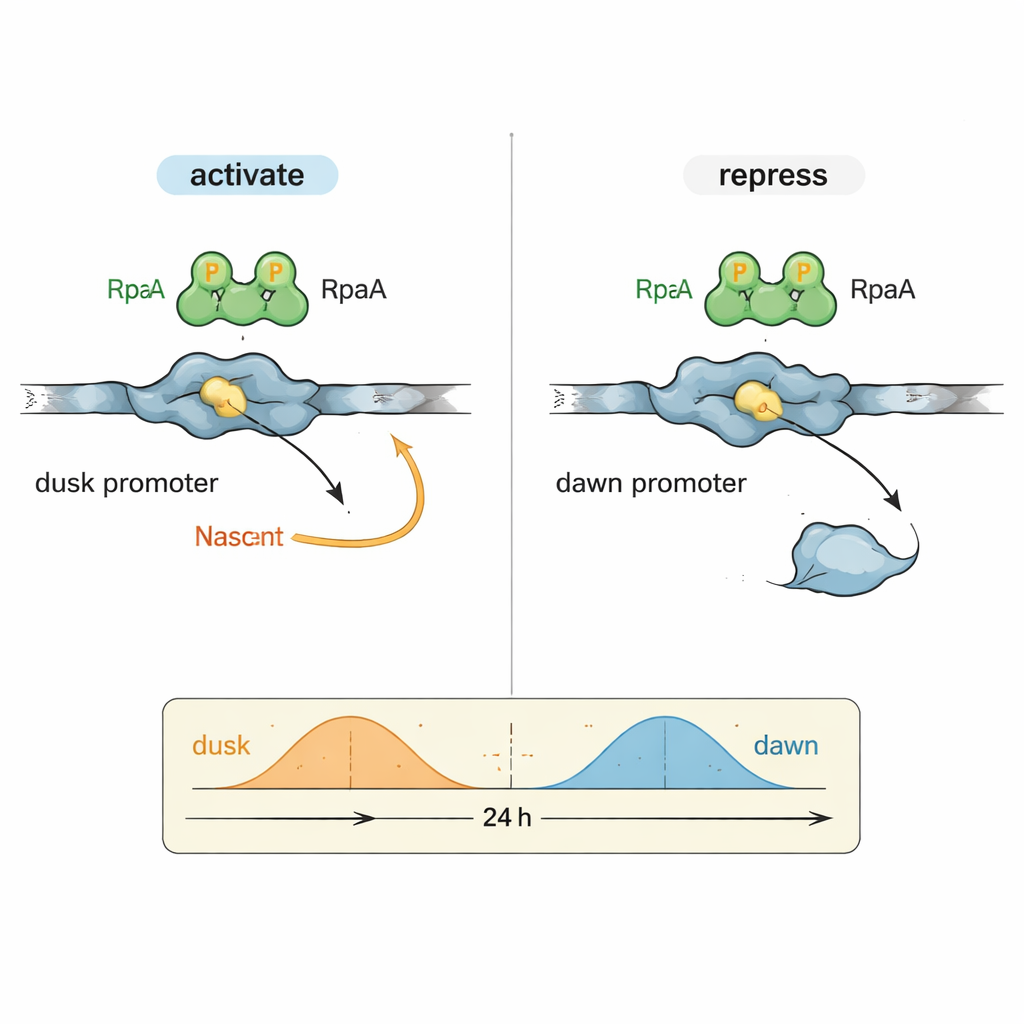
Um enigma na biologia circadiana foi como um único fator de saída, RpaA, pode coordenar genes que atingem pico em momentos muito diferentes do dia. Os autores se concentraram em duas regiões representativas de controle do DNA (promotores): kaiBC, que é mais ativo ao anoitecer, e purF, que atinge pico ao amanhecer. Em reações controladas usando RNA polimerase cianobacterial purificada e RpaA, eles mostraram que RpaA fosforilada aumenta a transcrição a partir do promotor kaiBC enquanto, ao mesmo tempo, reduz a transcrição do promotor purF. Experimentos detalhados de footprinting mapearam exatamente onde RpaA se liga em cada trecho de DNA, revelando que sua posição relativa aos elementos padrão do promotor determina se age como um acelerador ou como um freio.
Vendo o interruptor do relógio em detalhe atômico
Para entender esse comportamento duplo em nível molecular, a equipe usou microscopia crioeletrônica de alta resolução para capturar a estrutura de RpaA ligada ao promotor kaiBC juntamente com a RNA polimerase. As imagens mostram RpaA agarrando o DNA como um par assimétrico e fazendo contato com duas partes-chave da enzima: a cauda da subunidade alfa e uma região do fator sigma que normalmente reconhece sequências promotoras. Esses contatos dobram o DNA e ajudam a posicionar a RNA polimerase em um local de início de transcrição ligeiramente redefinido. Mutações cuidadosamente escolhidas que enfraquecem qualquer um desses pontos de contato reduzem ou abolam a ativação de kaiBC, tanto in vitro quanto em células vivas, confirmando que o recrutamento físico da RNA polimerase explica a ativação gênica na fase do anoitecer.
Construindo um gene dirigido por relógio do zero
Como a RNA polimerase nativa das cianobactérias é complexa e difícil de manter ativa por dias, os pesquisadores recorreram à muito mais simples polimerase do bacteriófago T7, amplamente usada em laboratórios. RpaA não consegue recrutar essa enzima não relacionada, mas ainda pode bloqueá-la ao se sentar sobre o DNA. A equipe projetou um molde de DNA sintético onde um promotor T7 dirige um repórter de RNA fluorescente “Broccoli”, com um sítio de ligação de RpaA colocado a jusante. Quando combinaram esse molde com o relógio KaiA–KaiB–KaiC, a quinase/fosfatase CikA, RpaA e a T7 polimerase em um único tampão otimizado, observaram taxas de transcrição que aumentavam e diminuíam com um período de cerca de 24 horas. O ritmo pôde ser reiniciado alterando a proporção ATP/ADP e manteve quase o mesmo período em uma faixa de temperaturas — características clássicas de um verdadeiro relógio circadiano.
De relógios simples a marcação temporal programada
O estudo mostra que apenas seis proteínas são suficientes para conectar um marca-passo químico a uma leitura gênica rítmica: as três proteínas Kai do relógio, CikA, RpaA e uma RNA polimerase. Ao mudar onde RpaA se posiciona no DNA, a mesma molécula pode fazer com que alguns genes atinjam pico ao anoitecer e outros ao amanhecer, ajudando a explicar as ondas complexas de atividade gênica observadas em cianobactérias. Como o desenho baseado em repressão funciona mesmo com uma polimerase estrangeira como a T7, deve ser possível transplantar este módulo de relógio minimalista para outros micróbios ou sistemas sem célula, permitindo que cientistas programem genes para ligar e desligar com ritmos diários para pesquisa, produção industrial ou futuras aplicações terapêuticas.
Citação: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Palavras-chave: relógio circadiano, cianobactérias, regulação da transcrição, RpaA, biologia sintética